Иммуноглобулин А
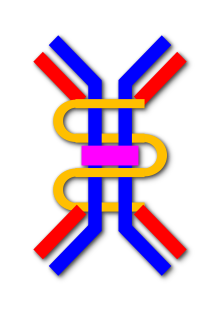

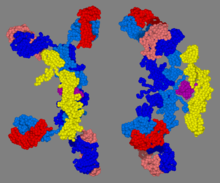
Иммуноглобулин А ( Ig A , также называемый sIgA в секреторной форме) представляет собой антитело , которое играет роль в иммунной функции слизистых оболочек . Количество IgA, вырабатываемого слизистыми оболочками, больше, чем количество всех других типов антител вместе взятых. [3] кишечника выделяется от трех до пяти граммов . в просвет В абсолютном выражении ежедневно [4] Это составляет до 15% от общего количества иммуноглобулинов, вырабатываемых в организме. [5]
IgA имеет два подкласса ( IgA1 и IgA2 ) и может производиться как в мономерной, так и в димерной форме. Димерная форма IgA является наиболее распространенной и, если она связана с секреторным компонентом, ее также называют секреторным IgA (sIgA). sIgA является основным иммуноглобулином , обнаруживаемым в слизистых выделениях , включая слезы , слюну , пот , молозиво и секреты мочеполового тракта , желудочно-кишечного тракта , предстательной железы и респираторного эпителия . Он также содержится в небольших количествах в крови. Секреторный компонент sIgA защищает иммуноглобулин от разрушения протеолитическими ферментами; таким образом, sIgA может выживать в суровых условиях желудочно-кишечного тракта и обеспечивать защиту от микробов , размножающихся в выделениях организма. [6] sIgA также может ингибировать воспалительные эффекты других иммуноглобулинов. [7] IgA является плохим активатором системы комплемента и опсонизирует . слабо [ нужна ссылка ]
Формы
[ редактировать ]IgA1 против IgA2
[ редактировать ]IgA существует в двух изотипах : IgA1 и IgA2. Оба они являются сильно гликозилированными белками. [8] Хотя IgA1 преобладает в сыворотке (~80%), процентное содержание IgA2 в секрете выше, чем в сыворотке (~35% в секрете); [9] Соотношение клеток, секретирующих IgA1 и IgA2, варьирует в разных лимфоидных тканях организма человека: [10]
- IgA1 является преобладающим подклассом IgA, обнаруженным в сыворотке. В большинстве лимфоидных тканей преобладают клетки, продуцирующие IgA1. [11]
- В IgA2 тяжелая и легкая цепи связаны не дисульфидными , а нековалентными связями. В секреторных лимфоидных тканях (например, лимфоидной ткани кишечника , или GALT) доля продукции IgA2 больше, чем в несекреторных лимфоидных органах (например, селезенке, периферических лимфатических узлах).
И IgA1, и IgA2 были обнаружены во внешних выделениях, таких как молозиво , материнское молоко, слезы и слюна , где IgA2 более выражен, чем в крови. [9] Полисахаридные антигены имеют тенденцию индуцировать больше IgA2, чем белковые антигены. [10]
И IgA1, и IgA2 могут находиться в мембраносвязанной форме. [12] ( см. рецептор B-клеток )
Сыворотка против. секреторный IgA
[ редактировать ]Также можно различать формы IgA в зависимости от их местоположения: сывороточный IgA и секреторный IgA. [ нужна ссылка ]
В секреторном IgA, форме, обнаруженной в секрете, полимеры из 2–4 мономеров IgA связаны двумя дополнительными цепями; как таковая, молекулярная масса slgA составляет 385 кДа. Одной из них является J-цепь (соединительная цепь), которая представляет собой полипептид с молекулярной массой 15 кДа, богатый цистеином и структурно совершенно отличающийся от других цепей иммуноглобулина. Эта цепь образуется в клетках, секретирующих IgA. [ нужна ссылка ]
Олигомерные формы IgA во внешних (слизистых) секретах содержат также полипептид значительно большей молекулярной массы (70 кДа), называемый секреторным компонентом , который продуцируется эпителиальными клетками . Эта молекула происходит от рецептора поли-Ig (130 кДа), который отвечает за поглощение и трансклеточный транспорт олигомерного (но не мономерного) IgA через эпителиальные клетки и в такие секреты, как слезы, слюна, пот и кишечная жидкость. [ нужна ссылка ]
Физиология
[ редактировать ]Сывороточный IgA
[ редактировать ]В крови IgA взаимодействует с рецептором Fc, называемым FcαRI (или CD89 ), который экспрессируется на иммунных эффекторных клетках, инициируя воспалительные реакции. [13] Лигирование FcαRI с помощью иммунных комплексов, содержащих IgA, вызывает клеточно-опосредованную цитотоксичность (ADCC), дегрануляцию эозинофилов и базофилов , фагоцитоз моноцитами антителозависимую , макрофагами и нейтрофилами , а также запуск активности респираторного взрыва полиморфно-ядерными лейкоцитами . [13]
Секреторный IgA
[ редактировать ]Высокая распространенность IgA в участках слизистой оболочки является результатом сотрудничества между плазматическими клетками , продуцирующими полимерный IgA (pIgA), и эпителиальными клетками слизистой оболочки, экспрессирующими полимерный рецептор иммуноглобулина (pIgR). [13] Полимерный IgA (в основном секреторный димер) продуцируется плазматическими клетками собственной пластинки слизистой оболочки, прилегающей к поверхности слизистой оболочки. Он связывается с pIgR на базолатеральной поверхности эпителиальных клеток и попадает в клетку посредством эндоцитоза . Комплекс рецептор-IgA проходит через клеточные компартменты, а затем секретируется на просветной поверхности эпителиальных клеток, все еще прикрепленных к рецептору. Происходит протеолиз рецептора, и димерная молекула IgA вместе с частью рецептора, известной как секреторный компонент (SC), может свободно диффундировать по просвету , при этом димерные IgA и SC вместе образуют так называемый секреторный IgA ( сига) [14] В кишечнике IgA может связываться со слоем слизи, покрывающим эпителиальные клетки. Таким образом формируется барьер, способный нейтрализовать угрозы до того, как они достигнут эпителиальных клеток. [ нужна ссылка ]
Уровни секреторного IgA колеблются в течение суток, причем самые высокие уровни обнаруживаются в тонком кишечнике и кале в районе ZT6, в середине светового периода. [15] Регуляция секреции IgA связана с микробиотой, и известно, что IgA контролирует определенных членов колеблющихся микробов посредством прямых взаимодействий. [15] Однако основная причина ритмичной секреции IgA до конца не ясна и может различаться в разных частях тела.
Продукция sIgA против специфических антигенов зависит от отбора проб М-клеток и лежащих в их основе дендритных клеток , активации Т-клеток и переключения класса В-клеток в GALT, мезентериальных лимфатических узлах и изолированных лимфоидных фолликулах в тонком кишечнике. [16]
sIgA в первую очередь действует путем блокирования эпителиальных рецепторов (например, путем связывания их лигандов с патогенами), стерически препятствуя прикреплению к эпителиальным клеткам и путем иммунного исключения. [16] Иммунная эксклюзия — это процесс агглютинации поливалентных антигенов или патогенов путем сшивания их антителами, улавливания их в слое слизи и/или их перистальтического удаления . Олигосахаридные цепи компонента IgA могут связываться со слоем слизи, который находится поверх эпителиальных клеток. [16] Поскольку sIgA является плохим опсонином и активатором комплемента, простого связывания патогена не обязательно достаточно для его сдерживания — возможно, придется связываться со специфическими эпитопами, чтобы стерически затруднить доступ к эпителию. [16]
Клиренс IgA опосредован, по крайней мере частично, рецепторами асиалогликопротеинов , которые распознают галактозоконцевыми IgA с N- гликаны концами . [8]
Патология
[ редактировать ]Генетический
[ редактировать ]Снижение или отсутствие IgA из-за наследственной неспособности вырабатывать IgA называется селективным дефицитом IgA и может привести к клинически значимому иммунодефициту . [17]
Антитела против IgA, иногда присутствующие у людей с низким уровнем IgA или его отсутствием, могут привести к серьезным анафилактическим реакциям при переливании продуктов крови, случайно содержащих IgA. Однако у большинства лиц с подозрением на анафилактические реакции IgA наблюдались острые генерализованные реакции, вызванные другими причинами, а не переливанием анти-IgA. [18]
микробный
[ редактировать ]Neisseria Виды , включая Neisseria gonorrhoeae (вызывающую гонорею ), [19] Стрептококк пневмонии [20] и Haemophilus influenzae типа B. [21] все они выделяют протеазу, которая разрушает IgA . Кроме того, Blastocystis было показано, что виды имеют несколько подтипов, которые генерируют ферменты цистеин и аспарагиновую протеазу , которые разрушают человеческий IgA. [22]
Аутоиммунные и иммуноопосредованные
[ редактировать ]IgA-нефропатия вызвана отложениями IgA в почках. В патогенезе участвует продукция гипогликозилированного IgA1, который накапливается и в дальнейшем приводит к образованию иммунных комплексов и продукции IgA-специфических IgG, что в дальнейшем приводит к воспалению тканей. [23]
Целиакия включает патологию IgA из-за присутствия антиэндомизиальных антител IgA. [24] [25] Дополнительное тестирование было проведено с использованием аутоантител IgA к трансглутаминазе, которые были идентифицированы как специфические и чувствительные для выявления целиакии. [26] [27]
Пурпура Геноха-Шенлейна (HSP) — системный васкулит, вызванный отложениями IgA и компонента комплемента 3 (C3) в мелких кровеносных сосудах. HSP обычно возникает у маленьких детей и поражает кожу и соединительные ткани, мошонку, суставы, желудочно-кишечный тракт и почки. Обычно оно следует за инфекцией верхних дыхательных путей и проходит в течение пары недель, когда печень очищает агрегаты IgA. [28]
Линейный IgA-буллезный дерматоз и IgA-пузырчатка являются двумя примерами IgA-опосредованных иммунобуллезных заболеваний. IgA-опосредованные иммунобуллезные заболевания часто трудно лечить даже с помощью обычно эффективных лекарств, таких как ритуксимаб. [29]
Вызванный наркотиками
[ редактировать ]У некоторых пациентов ванкомицин может вызывать линейный IgA буллезный дерматоз. [30]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Боннер А., Альмогрен А., Фуртадо П.Б., Керр М.А., Перкинс С.Дж. (январь 2009 г.). «Расположение секреторного компонента на Fc-крае димерного IgA1 позволяет понять роль секреторного IgA1 в иммунитете слизистой оболочки» . Иммунология слизистой оболочки . 2 (1): 74–84. дои : 10.1038/ми.2008.68 . ПМИД 19079336 .
- ^ Боннер А., Альмогрен А., Фуртадо П.Б., Керр М.А., Перкинс С.Дж. (февраль 2009 г.). «Неплоская структура секреторного IgA2 и почти плоская структура раствора секреторного IgA1 рационализируют их различные иммунные реакции слизистой оболочки» . Журнал биологической химии . 284 (8): 5077–87. дои : 10.1074/jbc.M807529200 . ПМЦ 2643523 . ПМИД 19109255 .
- ^ Фэгэрашан С .; Хондзё Т. (январь 2003 г.). «Синтез кишечного IgA: регуляция передовых защитных сил организма». Обзоры природы. Иммунология . 3 (1): 63–72. дои : 10.1038/nri982 . ПМИД 12511876 . S2CID 2586305 .
- ^ Брандцаег П., Пабст Р. (ноябрь 2004 г.). «Пойдем на слизистую: общение на скользкой земле». Тенденции в иммунологии . 25 (11): 570–7. дои : 10.1016/j.it.2004.09.005 . ПМИД 15489184 .
- ^ Макферсон А.Дж., Slack E (ноябрь 2007 г.). «Функциональные взаимодействия комменсальных бактерий с секреторными IgA кишечника». Современное мнение в гастроэнтерологии . 23 (6): 673–8. дои : 10.1097/MOG.0b013e3282f0d012 . ПМИД 17906446 . S2CID 8445606 .
- ^ Жункейра LC, Карнейру Дж (2003). Базовая гистология . МакГроу-Хилл. ISBN 978-0-8385-0590-8 . [ нужна страница ]
- ^ Холмгрен Дж., Черкински С. (апрель 2005 г.). «Мукозальный иммунитет и вакцины» . Природная медицина . 11 (4 приложения): S45–53. дои : 10.1038/nm1213 . ПМИД 15812489 .
- ^ Перейти обратно: а б Маверакис Э., Ким К., Шимода М., Гершвин М.Е., Патель Ф., Уилкен Р., Райчаудхури С., Рухаак Л.Р., Лебрилла CB (февраль 2015 г.). «Гликаны в иммунной системе и теория аутоиммунитета с измененными гликанами: критический обзор» . Журнал аутоиммунитета . 57 : 1–13. дои : 10.1016/j.jaut.2014.12.002 . ПМЦ 4340844 . ПМИД 25578468 .
- ^ Перейти обратно: а б Делакруа Д.Л., Дайв С., Рамбо Дж.К., Верман Дж.П. (октябрь 1982 г.). «Подклассы IgA в различных секретах и сыворотке» . Иммунология . 47 (2): 383–5. ПМЦ 1555453 . ПМИД 7118169 .
- ^ Перейти обратно: а б Симелл Б., Килпи Т., Кайхти Х. (март 2006 г.). «Распределение подклассов естественных антител IgA слюны против пневмококкового капсульного полисахарида типа 14 и пневмококкового поверхностного адгезина А (PsaA) у детей» . Клиническая и экспериментальная иммунология . 143 (3): 543–9. дои : 10.1111/j.1365-2249.2006.03009.x . ПМК 1809616 . ПМИД 16487254 .
- ^ Макферсон А.Дж., Маккой К.Д., Йохансен Ф.Е., Брандцаег П. (январь 2008 г.). «Иммунная география индукции и функции IgA» . Иммунология слизистой оболочки . 1 (1): 11–22. дои : 10.1038/ми.2007.6 . ПМИД 19079156 .
- ^ Хунг А.Ф., Чен Дж.Б., Чанг Т.В. (август 2008 г.). «Аллели и изоформы мембраносвязанного IgA1 человека». Молекулярная иммунология . 45 (13): 3624–30. дои : 10.1016/j.molimm.2008.04.023 . ПМИД 18538846 . S2CID 26094982 .
- ^ Перейти обратно: а б с Сноек В., Питерс И.Р., Кокс Э. (2006). «Система IgA: сравнение структуры и функций у разных видов» (PDF) . Ветеринарное исследование . 37 (3): 455–67. дои : 10.1051/vetres:2006010 . ПМИД 16611558 .
- ^ Кетцель К.С., Робинсон Дж.К., Чинталачаруву К.Р., Верман Дж.П., Ламм М.Е. (октябрь 1991 г.). «Полимерный рецептор иммуноглобулина (секреторный компонент) опосредует транспорт иммунных комплексов через эпителиальные клетки: местная защитная функция для IgA» . Труды Национальной академии наук Соединенных Штатов Америки . 88 (19): 8796–800. Бибкод : 1991PNAS...88.8796K . дои : 10.1073/pnas.88.19.8796 . ПМК 52597 . ПМИД 1924341 .
- ^ Перейти обратно: а б Ратинер, Карина; Фахлер-Шарп, Тахель; Элинав, Эран (16 января 2023 г.). «Колебания микробиоты тонкого кишечника, эффекты хозяина и регуляция - рассмотрение трех ключевых эффекторных молекул» . Биология . 12 (1): 142. doi : 10.3390/biology12010142 . ПМЦ 9855434 . ПМИД 36671834 .
- ^ Перейти обратно: а б с д Мантис, Нью-Джерси, Рол Н., Кортези Б. (ноябрь 2011 г.). «Сложная роль секреторного IgA в иммунитете и гомеостазе слизистой оболочки кишечника» . Иммунология слизистой оболочки . 4 (6): 603–11. дои : 10.1038/ми.2011.41 . ПМЦ 3774538 . ПМИД 21975936 .
- ^ Йел Л. (январь 2010 г.). «Селективная недостаточность IgA» . Журнал клинической иммунологии . 30 (1): 10–6. дои : 10.1007/s10875-009-9357-x . ПМЦ 2821513 . ПМИД 20101521 .
- ^ Сэндлер С.Г., Мэллори Д., Маламут Д., Экрикч Р. (январь 1995 г.). «Анафилактические трансфузионные реакции IgA». Обзоры трансфузионной медицины . 9 (1): 1–8. дои : 10.1016/S0887-7963(05)80026-4 . ПМИД 7719037 .
- ^ Холтер Р., Полнер Дж., Мейер Т.Ф. (июль 1984 г.). «IgA-протеаза Neisseria gonorrhoeae: выделение и характеристика гена и его внеклеточного продукта» . Журнал ЭМБО . 3 (7): 1595–601. дои : 10.1002/j.1460-2075.1984.tb02016.x . ПМК 557564 . ПМИД 6430698 .
- ^ Проктор М., Мэннинг П.Дж. (сентябрь 1990 г.). «Продукция протеазы иммуноглобулина А Streptococcus pneumoniae из животных» . Инфекция и иммунитет . 58 (9): 2733–7. дои : 10.1128/IAI.58.9.2733-2737.1990 . ПМК 313560 . ПМИД 2117567 .
- ^ Сент-Жеме Дж.В., де ла Морена М.Л., Фальков С. (октябрь 1994 г.). «Белок, подобный протеазе IgA Haemophilus influenzae, способствует тесному взаимодействию с эпителиальными клетками человека». Молекулярная микробиология . 14 (2): 217–33. дои : 10.1111/j.1365-2958.1994.tb01283.x . ПМИД 7830568 . S2CID 30615746 .
- ^ Робертс Т., Старк Д., Харкнесс Дж., Эллис Дж. (2014). «Обновленная информация о патогенном потенциале и вариантах лечения Blastocystis sp» . Кишечные патогены . 6:17 . дои : 10.1186/1757-4749-6-17 . ПМК 4039988 . ПМИД 24883113 .
- ^ Лай, Кар Ненг; Тан, Сидней CW; Шена, Франческо Паоло; Новак, Джон; Томино, Ясухико; Фого, Агнес Б.; Глассок, Ричард Дж. (2016). «IgA-нефропатия» . Обзоры природы. Учебники по болезням . 2 : 16001. дои : 10.1038/nrdp.2016.1 . ПМИД 27189177 . S2CID 3989355 .
- ^ Принц Х.Э., Норман Г.Л., Биндер В.Л. (март 2000 г.). «Дефицит иммуноглобулина А (IgA) и альтернативные антитела, связанные с целиакией, в сыворотке крови, отправленной в справочную лабораторию для тестирования эндомизиального IgA» . Клинико-диагностическая лаборатория иммунологии . 7 (2): 192–6. дои : 10.1128/cdli.7.2.192-196.2000 . ПМЦ 95847 . ПМИД 10702491 .
- ^ Каннингем-Рандлс C (сентябрь 2001 г.). «Физиология IgA и дефицита IgA». Журнал клинической иммунологии . 21 (5): 303–9. дои : 10.1023/А:1012241117984 . ПМИД 11720003 . S2CID 13285781 .
- ^ Маламут Г., Кординг С., Серф-Бенсуссан Н. (26 июня 2019 г.). «Последние достижения в области целиакии и рефрактерной целиакии» . F1000Рес . 8 : 969. дои : 10.12688/f1000research.18701.1 . ПМК 6600866 . ПМИД 31297187 .
- ^ Каннингем-Рандлс C (февраль 2000 г.). «Сравнение анализов антиэндомизийных и антитрансглутаминазных антител для диагностики целиакии у детей». Журнал Израильской медицинской ассоциации . 2 (2): 122–5. ПМИД 10804933 .
- ^ Рай А., Наст С., Адлер С. (декабрь 1999 г.). «Пурпурный нефрит Геноха-Шенлейна» . Журнал Американского общества нефрологов . 10 (12): 2637–44. дои : 10.1681/ASN.V10122637 . ПМИД 10589705 .
- ^ Хе Ю, Шимода М, Оно Ю, Вильялобос И.Б., Митра А, Кониа Т, Грандо С.А., Зоне Джей Джей, Маверакис Э (июнь 2015 г.). «Сохранение аутореактивных IgA-секретирующих B-клеток, несмотря на прием нескольких иммунодепрессантов, включая ритуксимаб» . JAMA Дерматология . 151 (6): 646–50. дои : 10.1001/jamadermatol.2015.59 . ПМИД 25901938 .
- ^ Го-младший, Абу Салех ОМ (октябрь 2020 г.). «Ванкомицин-индуцированный линейный IgA буллезный дерматоз». Медицинский журнал Новой Англии . 383 (16): 1577. doi : 10.1056/NEJMicm2003334 . ПМИД 33053287 . S2CID 222420540 .
Внешние ссылки
[ редактировать ]- Иммуноглобулин + А в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- Херич, Р. (2017). «Известна ли полностью роль IgA в местном иммунитете?» . Пищевая и сельскохозяйственная иммунология . 28 (2): 223–237. дои : 10.1080/09540105.2016.1258547 .