Пирамидальный алкен
Пирамидальные алкены — алкены , в которых два углерода, атома образующие двойную связь , не копланарны своим четырем заместителям . Эта деформация является результатом геометрических ограничений. Пирамидальные алкены представляют интерес только потому, что из них можно многое узнать о природе химической связи . [ 1 ]
Энергетика
[ редактировать ]Поворот на двугранный угол 90° между двумя группами атомов углерода требует меньше энергии, чем сила пи-связи , и связь все еще сохраняется. Углероды двойной связи становятся пирамидальными , что позволяет сохранить некоторое выравнивание р-орбиталей и, следовательно, пи-связь. Две другие прикрепленные группы остаются под большим двугранным углом. Это противоречит распространенному в учебниках утверждению о том, что два атома углерода сохраняют свою плоскую природу при скручивании, и в этом случае p-орбитали будут поворачиваться достаточно далеко друг от друга, чтобы не иметь возможности поддерживать пи-связь. В алкене, закрученном на 90°, p-орбитали смещены всего на 42°, а энергия деформации составляет всего около 40 ккал/моль. Напротив, полностью разорванная пи-связь имеет энергетическую стоимость около 65 ккал/моль. [ 2 ]
Примеры
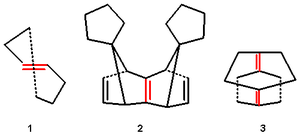
[ редактировать ]В циклогептене ( 1.1 ) цис- изомер представляет собой обычную ненапряженную молекулу, но гептановое кольцо слишком мало для размещения алкеновой группы в транс -конфигурации, что приводит к деформации и скручиванию двойной связи. Смещение р-орбитали сводится к минимуму за счет степени пирамидализации . В родственных анти-Бредтовских молекулах . доминирует не пиримидализация, а скручивание.
Алкены с пирамидальной структурой также существуют, в которых преобладает симметричный изгиб заместителей без смещения p-орбиталей.
Угол пирамидализации φ ( b ) определяется как угол между плоскостью, определяемой одним из атомов углерода с двойной связью и двумя его заместителями, и продолжением двойной связи, и рассчитывается как:
угол изгиба бабочки или угол складывания ψ ( c ) определяется как угол между двумя плоскостями и может быть получен путем усреднения двух углов скручивания R 1 C=CR 3 и R 2 C=CR 4 .
В алкенах 1.2 и 1.3 эти углы определены методом рентгеновской кристаллографии как 32,4°/22,7° и 27,3°/35,6° соответственно. Несмотря на стабильность, эти алкены очень реакционноспособны по сравнению с обычными алкенами. Они склонны к димеризации с образованием циклобутановых колец или реагируют с кислородом с образованием эпоксидов .
синтезируется фотохимическим циклоприсоединением бромантрацена с Соединение тетрадегидродиантрацен, также с углом пирамидализации 35° , последующим отщеплением бромистого водорода .
Это соединение очень реакционноспособно в реакциях Дильса-Альдера из -за пространственного взаимодействия между двумя алкеновыми группами. Эта повышенная реакционная способность, в свою очередь, позволила синтезировать первый в истории аромат Мебиуса .
В одном исследовании [ 3 ] напряженный алкен 4.4 был синтезирован с самыми высокими углами пирамидализации - 33,5° и 34,3°. собой двойной аддукт Дильса-Альдера дииодциклофана Это соединение представляет 4.1 и антрацена 4.3 по реакции в присутствии трет-бутоксида калия в кипящем дибутиловом эфире через диариновое промежуточное соединение 4.2 . Это стабильное соединение, но оно будет медленно реагировать с кислородом с образованием эпоксида , если его оставить в виде раствора в хлороформе .
В одном исследовании [ 4 ] выделение пирамидального алкена невозможно даже путем матричной изоляции при чрезвычайно низких температурах, если он не стабилизирован координацией металла :
Реакция дииодида 5.1 на рисунке 5 с амальгамой натрия в присутствии этиленбис(трифенилфосфин)платины(0) не дает промежуточного алкена 5.2, но дает стабилизированную платиной 5.3 . Сигма-связь в этом соединении разрушается при реакции с этанолом .
Ссылки
[ редактировать ]- ^ Васкес, Сантьяго; Кэмпс, Пелайо (2005). «Химия пирамидальных алкенов». Тетраэдр . 61 (22): 5147–5208. дои : 10.1016/j.tet.2005.03.055 .
- ^ Бэрроуз, Сьюзен Э.; Эберлейн, Томас Х. (2005). «Понимание вращения вокруг двойной связи C=C». Дж. Хим. Образование . 82 (9): 1329. Бибкод : 2005JChEd..82.1329B . дои : 10.1021/ed082p1329 .
- ^ Долбье, WR младший; Чжай, Ю.-А.; Баттист, Массачусетс; Аббуд, штат Калифорния; Гивирига, И. (2005). «Высокопирамидальный клеточный алкен, образующийся в результате двойного циклоприсоединения Дильса-Альдера син -4,5,13,14-бис(дегидро)октафторпарациклофана к антрацену». Дж. Орг. хим. 70 (25): 10336–10341. дои : 10.1021/jo051488v .
- ^ Феофаний, Фаница А.; Тасиопулос, Анастасиос Дж.; Николаидес, Афанасий; Чжоу, Синь; Джонсон, Уильям Т.Г.; Борден, Уэстон Тэтчер (2006). «Доказательства образования комплекса (Ph 3 P) 2 Pt 3,7-диметилтрицикло[3.3.0.0 3,7 ]окт-1(5)-ен — наиболее высокопирамидальный алкен в гомологическом ряду. Выделение и рентгеновская структура продукта присоединения этанола к комплексу». Org. Lett. 8 (14): 3001–3004. doi : 10.1021/ol060994j .