Метан
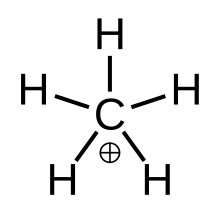 «Настоящий» метан, метастабильное переходное состояние. [ГЛ 5 ] + | |
 Флюксиальный метан, [СН 3 (Н 2 )] + | |
| Имена | |
|---|---|
| Название ИЮПАК Метан | |
| Другие имена карбоний (разочарован из-за множества определений) [1] | |
| Идентификаторы | |
3D model ( JSmol ) |
|
ПабХим CID | |
| Характеристики | |
| СН + 5 | |
| Молярная масса | 17.051 g·mol −1 |
| Сопряженная база | Метан |
| Структура | |
| тригонально-бипирамидальный | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
В химии метан — сложный положительный ион с формулой [ Ч 5 ] + (метастабильная переходная форма, углерода атом ковалентно связан с пятью атомами водорода ) или [СН 3 (Н 2 )] + (флюксная форма, а именно молекула с одним атомом углерода, ковалентно связанным с тремя атомами водорода и одной молекулой диводорода), несущая электрический заряд +1 . Это суперкислота и один из ониевых ионов , действительно, самый простой ион карбония .
Он очень нестабилен и очень реактивен даже при наличии полного октета, что придает ему сверхкислотные свойства.
Метан можно производить в лаборатории в виде разреженного газа или в виде разбавленной формы в суперкислотах. Впервые он был подготовлен в 1950 году и опубликован в 1952 году Виктором Талроузом и его помощницей Анной Константиновной Любимовой. [2] [3] Он встречается как промежуточный вид в химических реакциях.
Ион метана назван в честь метана ( CH 4 ), по аналогии с получением иона аммония ( NH + 4 ) из аммиака ( NH3 ) .
Структура
[ редактировать ]Флюксиальный метан можно представить как CH + 3 Ион карбения с молекулой водорода, взаимодействующей с пустой орбиталью по связи 3-центр-2-электрон . Связывающая электронная пара в Молекула H 2 разделена между двумя атомами водорода и одним атомом углерода, образующими связь 3-центр-2-электрона. [4]
Два атома водорода в Молекула H 2 может непрерывно обмениваться положениями с тремя атомами водорода в Ион CH + 3 (изменение конформации, называемое псевдовращением , в частности механизм Берри ). Поэтому ион метана считается флюссионной молекулой . Энергетический барьер обмена достаточно низок и происходит даже при очень низких температурах. [5] [6]
Инфракрасная спектроскопия использовалась для получения информации о различных конформациях иона метана. [7] [8] [9] ИК-спектр простого метана имеет две полосы CH симметричного и асимметричного простирания около 3000 см-1. −1 и две полосы около 1400 см. −1 от симметричных и асимметричных изгибных колебаний. В спектре CH + 5 присутствуют три асимметричных валентных колебания в районе 2800–3000 см. −1 , покачивающая вибрация на высоте 1300 см −1 , а изгибные колебания на высоте 1100 1300 см. −1 .
Подготовка
[ редактировать ]Метан можно получить из метана действием очень сильных кислот, например фторсурьмы ( пентафторид сурьмы). SbF 5 во фтористом водороде HF). [10]
около 270 Па и температуре окружающей среды ион метана При давлении CH + 4 будет реагировать с нейтральным метаном с образованием метана и метильного радикала : [11]
- СН + 4 + СН 4 → СН + 5 + СН 3 •
Ион метана также может быть получен в газовой фазе в результате реакции метана и ЧАС + ион (т.е. протон). [ нужна ссылка ]
- СН 4 + Н + (г) → СН + 5
Стабильность и реакции
[ редактировать ]Катионы, полученные реакцией метана с SbF 5 + HF , включая метан, стабилизируются за счет взаимодействия с молекулами HF.
При низких давлениях (около 1 мм рт. ст.) и температуре окружающей среды метан не реагирует с нейтральным метаном. [11]
Дальнейшее чтение
[ редактировать ]- Д. У. Бу; З.Ф. Лю; AG костюмы; Дж. С. Це; Ю. Т. Ли (1995). «Динамика ионов карбония, сольватированных молекулярным водородом: CH5+(H2)n (n = 1, 2, 3)». Наука . 269 (5220): 57–9. Бибкод : 1995Sci...269...57B . дои : 10.1126/science.269.5220.57 . ПМИД 17787703 . S2CID 2100896 .
- Крамер, генеральный директор (1999). «Стабильность CH5+ и масс-спектрометрия» . Наука . 286 (5442): 1051а–1051. дои : 10.1126/science.286.5442.1051a . ISSN 0036-8075 .
- Маркс, Д. (1999). «МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ: CH5+: Улыбается Чеширский кот». Наука . 284 (5411): 59–61. Бибкод : 1999Наука...284...59. . дои : 10.1126/science.284.5411.59 . ISSN 0036-8075 . S2CID 94058015 . </ref> У этого необычного вида
- Сяо-Ган Ван; Такер Кэррингтон-младший (2016). «Рассчитанные уровни энергии вращения и изгиба CH 5 + и сравнение с экспериментом». Journal of Chemical Physics . 144 (20): 204304. Bibcode : 2016JChPh.144t4304W . doi : 10.1063/1.4948549 . PMID 27250303 .
- Х. Шмидт; Пер Йенсен; С. Шлеммер (2017). «Вращательно-колебательное движение чрезвычайно гибких молекул – Молекулярный суперротор» . Письма по химической физике . 672 : 34–46. Бибкод : 2017CPL...672...34S . дои : 10.1016/j.cplett.2017.01.045 .
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Химия, Международный союз теоретической и прикладной химии (2009). «ион карбония» . Сборник химической терминологии ИЮПАК . ИЮПАК. дои : 10.1351/goldbook.C00839 . ISBN 978-0-9678550-9-7 . Проверено 27 ноября 2018 г.
- ^ V. L. Talrose and A. K. Lyubimova, Dokl. Akad. Nauk SSSR 86, 909-912 (1952) (In Russian: Тальрозе, В. Л., and А. К. Любимова. "Вторичные процессы в ионном источнике масс-спектрометра." ДАН СССР 86 (1952): 909-912)
- ^ Николаев, Евгений (1998). «Виктор Талроуз: оценка» . Журнал масс-спектрометрии . 33 (6): 499–501. Бибкод : 1998JMSp...33..499N . doi : 10.1002/(SICI)1096-9888(199806)33:6<499::AID-JMS684>3.0.CO;2-C . ISSN 1076-5174 .
- ^ Расул, Голам; Пракаш, Г.К. Сурья; Ола, Джордж А. (2011). «Сравнительное исследование гиперкоординированных ионов карбония и их аналогов бора: задача для спектроскопистов». Письма по химической физике . 517 (1–3): 1–8. Бибкод : 2011CPL...517....1R . дои : 10.1016/j.cplett.2011.10.020 .
- ^ Шрайнер, Питер Р.; Ким, Сын Джун; Шефер, Генри Ф.; Раге Шлейер, Поль (1993). " Ч +
5 : Бесконечная история или последнее слово?». Journal of Chemical Physics . 99 (5): 3716–3720. doi : 10.1063/1.466147 . - ^ Мюллер, Хендрик; Куцельнигг, Вернер; Нога, Йозеф; Клоппер, Вим (1997). «CH5 +: история продолжается. Явно коррелированное исследование связанных кластеров». Журнал химической физики . 106 (5): 1863. Бибкод : 1997ЖЧФ.106.1863М . дои : 10.1063/1.473340 .
- ^ Уайт, Эдмунд Т.; Тан, Цзянь; Ока, Такеши (1999). " Ч. +
5 : Наблюдаемый инфракрасный спектр». Science . 284 (5411): 135–7. Bibcode : 1999Sci...284..135W . doi : 10.1126/science.284.5411.135 . PMID 10102811 . - ^ Оскар Асвани, Падма Кумар П; Честно, Бритта; Хегеманн, Илька; Шлеммер, Стефан; Маркс, Доминик (2005). «Понимание инфракрасного спектра голого CH +
5 " . Science . 309 (5738): 1219–1222. : 2005Sci ...309.1219A . doi : 10.1126/science.1113729 . PMID 15994376. . S2CID 28745636 Бибкод - ^ Хуан, Синьчуань; Маккой, Энн Б.; Боуман, Джоэл М .; Джонсон, Линдси М.; Сэвидж, Чандра; Донг, Фэн; Несбитт, Дэвид Дж. (2006). «Квантовая деконструкция инфракрасного спектра CH +
5 " . Science . 311 (5757): 60–63. : 2006Sci ...311...60H . doi : 10.1126/science.1121166 . PMID 16400143. . S2CID 26158108 Бибкод - ^ Соммер, Дж.; Йост, Р. (2000). «Карбений и ионы карбония в активации малых алканов, катализируемой жидкостью и твердой суперкислотой» (PDF) . Чистая и прикладная химия . 72 (12): 2309–2318. дои : 10.1351/pac200072122309 . S2CID 46627813 .
- ^ Jump up to: а б Филд, Флорида; Мансон, MSB (1965). «Реакции газообразных ионов. XIV. Масс-спектрометрические исследования метана при давлениях до 2 Торр». Журнал Американского химического общества . 87 (15): 3289–3294. дои : 10.1021/ja01093a001 .