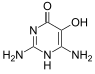
Дивицина
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК 2,6-Диамино-4,5-дигидроксипиримидин | |||
| Другие имена 2,6-диамино-4,5-пиримидиндиол; 2,6-диамин-5-гидрокси-4(3H ) -пиримидинон; 2,4-диамино-5,6-дигидроксипиримидин | |||
| Идентификаторы | |||
3D model ( JSmol ) |
| ||
| ХимическийПаук | |||
ПабХим CID | |||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA ) | |||
| Характеристики | |||
| С 4 Н 6 Н 4 О 2 | |||
| Молярная масса | 142.118 g·mol −1 | ||
| Появление | Коричневатые иглы | ||
| Растворимость в 10% КОН. | Растворимый [ нечеткий ] | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
Дивицин (2,6-диамино-4,5-дигидроксипиримидин) — окислитель и основание с алкалоидными свойствами, обнаруженное в бобах фава и Lathyrus sativus . Это агликон вицина . Распространенным производным является диацетатная форма (2,6-диамино-1,6-дигидро-4,5-пиримидиндион). [1]
Возникновение
[ редактировать ]Дивицин содержится в фасоли и бобовых Lathyrus sativus , также известных как хесари, которые являются дешевым и надежным источником пищи, обычно выращиваемым в Азии и Восточной Африке. [ нужна ссылка ]
Синтез
[ редактировать ]В растениях восстановленный дивицин образуется в результате гидролиза неактивного β-глюкозида вицина . [2]
Упрощенный трехэтапный процесс искусственного синтеза божественных веществ:
- Бензильная группа 2-амино-5-бензилокси-4-гидроксипиримидина удаляется кислотным гидролизом с образованием 2-амино-4,5-дигидроксипиримидина.
- Затем это промежуточное соединение обрабатывают азотистой кислотой с получением малорастворимого оранжевого продукта 2-амино-6-нитрозопиримидин-4,5-диола.
- Затем его восстанавливают дитионитом натрия с получением дивицина. [3]
Реакции
[ редактировать ]Изучены некоторые химические характеристики дивицина. Известно, что он энергично восстанавливает щелочные растворы 2,6-дихлорфенолиндофенола, фосфомолибдата или фосфовльфрамата и дает интенсивную синюю окраску при реакции с аммиачным раствором хлорида железа, что используется для идентификации и доказательства наличия енольной гидроксильной группы. .
Дивицин очень нестабилен в присутствии кислорода, а окисление происходит наиболее быстро при щелочных уровнях pH. Период полураспада дивицина при комнатной температуре и нейтральном pH составляет около получаса. Оба соединения почти сразу разрушаются при кипячении, а распад в обычных условиях может быть ускорен присутствием ионов тяжелых металлов, особенно Cu. 2+ . [4]
Токсичность
[ редактировать ]Дивицин считается гемотоксичным компонентом бобов и играет роль в развитии фавизма — заболевания, которое включает гемолитическую реакцию на потребление бобов из-за дефицита глюкозо-6-фосфатдегидрогеназы (G6PD или G6PDH). Этот дефицит, Х-сцепленное рецессивное наследственное заболевание, является наиболее распространенным дефицитом фермента во всем мире. Это особенно распространено среди лиц африканского, азиатского, средиземноморского и ближневосточного происхождения. Симптомы фавизма включают гемолиз , длительную желтуху , ядерную желтуху и даже острую почечную недостаточность . в крайних случаях [5]
Дивицин реагирует с кислородом в эритроцитах, в результате чего образуются активные формы кислорода, такие как перекись водорода и супероксид-анион . Эти молекулы являются сильными окислителями НАДФН и глутатиона . [6] Лица с дефицитом G6PD не могут регенерировать НАДФН достаточно быстро, чтобы предотвратить истощение запасов глутатиона. Это истощение приводит к тому, что клетки теряют защиту от окислительного стресса, вызванного агликонами. Окислительный стресс приводит к повреждению агрегатов гемоглобина и дисульфидных связей ( тельц Гейнца ), что приводит к гемолитической анемии, называемой фавизмом. [7]
Дивицин также присутствует в Lathyrus sativus и, по крайней мере частично, ответственен за его ядовитое действие – бобовое растение, обычно выращиваемое в подверженных засухе и голоду регионах Азии и Восточной Африки в качестве «страховой культуры» для потребления человеком и корма скота, когда другие культуры не могут расти, несмотря на их известную опасность для здоровья. [ нужна ссылка ]
Воздействие на животных
[ редактировать ]Исследования in vitro на крысах показали, что гемотоксическая доза дивицина 1,5 мМ при добавлении к суспензии эритроцитов приводила к быстрому снижению клеточного глутатиона, образованию эхиноцитов и повреждению мембранного скелета. Это привело к снижению гематокрита . [8]
Ссылки
[ редактировать ]- ^ Бендич, К. (1953). «Пересмотр структурной формулы вицина и его пиримидинового аглюкона, дивицина». Биохим. Биофиз. Акта . 12 (1–2): 462–77. дои : 10.1016/0006-3002(53)90166-8 . ПМИД 13115456 .
- ^ Бейкер, М.; Бося, А. (1984). «Механизм действия дивицина в бесклеточной системе и в эритроцитах с дефицитом глюкозо-6-фосфатдегидрогеназы». Токсикол. Патол . 12 (4): 331–336. дои : 10.1177/019262338401200405 . ПМИД 6099911 . S2CID 26038580 .
- ^ Честерфилд, Дж.; и др. (1964). «194. Пиримидины. Часть XIII. Электрофильное замещение в положении 6 и синтез дивицина (2,4-диамино-5,6-дигидроксипиримидина)». Дж. Хим. Соц. : 1001–1005. дои : 10.1039/jr9640001001 .
- ^ Магер, Дж.; Разин А.; Гершко, А. (1969). Линер, И. (ред.). Токсичные компоненты растительных продуктов питания . Нью-Йорк: Академическая пресса. стр. 293–312.
- ^ Фрэнк, Дж. (2005). «Диагностика и лечение дефицита G6PD». Являюсь. Фам. Врач . 72 (7): 1277–1282. ПМИД 16225031 .
- ^ Луццато, Лучио; Арезе, Паоло (04 января 2018 г.). Лонго, Дэн Л. (ред.). «Фавизм и дефицит глюкозо-6-фосфатдегидрогеназы». Медицинский журнал Новой Англии . 378 (1): 60–71. дои : 10.1056/NEJMra1708111 . ISSN 0028-4793 . ПМИД 29298156 .
- ^ Пулккинен, Марджо; Чжоу, Сяо; Лампи, Анна-Майя; Пииронен, Виено (декабрь 2016 г.). «Определение и стабильность дивицина и изоурамила, полученных путем ферментативного гидролиза вицина и конвицина бобов». Пищевая химия . 212 : 10–19. doi : 10.1016/j.foodchem.2016.05.077 . ПМИД 27374500 .
- ^ Макмиллан, округ Колумбия (1 августа 2001 г.). «Фавизм: влияние дивицина на сульфгидрильный статус эритроцитов крысы, активность гексозомонофосфатного шунта, морфологию и мембранные скелетные белки» . Токсикологические науки . 62 (2): 353–359. дои : 10.1093/toxsci/62.2.353 . ПМИД 11452148 .