Противоион

В химии противоион », произносится (иногда пишется как « противоион как таковой) — это ион , который сопровождает ионную разновидность , чтобы поддерживать электрическую нейтральность. В поваренной соли (NaCl, также известной как хлорид натрия) ион натрия (положительно заряженный) является противоионом иона хлорида (отрицательно заряженного) и наоборот.
Противоион чаще называют анионом или катионом , в зависимости от того, заряжен он отрицательно или положительно. Таким образом, противоионом аниону будет катион, и наоборот.
В биохимии противоионы обычно имеют расплывчатое определение. В зависимости от заряда белки связаны с множеством более мелких анионов и катионов. В растительных клетках анион малат часто накапливается в вакуоли , снижая водный потенциал и стимулируя расширение клеток. Чтобы сохранить нейтралитет, К + ионы часто накапливаются в виде противоиона. ионов Проникновение через гидрофобные клеточные стенки опосредовано ионно-транспортными каналами . Нуклеиновые кислоты анионные, соответствующие катионы часто представляют собой протонированные полиамины .
Межфазная химия
[ редактировать ]Противоионы — это подвижные ионы в ионообменных полимерах и коллоидах . [1] Ионообменные смолы представляют собой полимеры с суммарным отрицательным или положительным зарядом. Катионообменные смолы состоят из анионного полимера с противокатионами, обычно Na. + (натрий). Смола имеет более высокое сродство к сильно заряженным противокатионам, например Ca. 2+ (кальций) в случае умягчения воды . Соответственно, анионообменные смолы обычно поставляются в форме хлорида Cl. − , который представляет собой высокомобильный противоанион.
Противоионы используются в катализе фазового переноса . В типичном применении липофильный противокатион, такой как бензалконий, солюбилизирует реагенты в органических растворителях.
Химический раствор
[ редактировать ]Растворимость солей в органических растворителях зависит как от катиона, так и от аниона. Растворимость катионов в органических растворителях может быть повышена, если анион является липофильным. Аналогичным образом растворимость анионов в органических растворителях повышается за счет липофильных катионов. Наиболее распространенными липофильными катионами являются катионы четвертичного аммония , называемые «четвертичными солями».
- Липофильные контранионы
- Тетракис(пентафторфенил)борат лития представляет собой литиевую соль высоколипофильного тетраарилборатного аниона, часто называемого слабокоординирующим анионом . [2]
- Тетрафенилборат менее липофильен, чем перфторированное производное, но широко используется в качестве осаждающего агента.
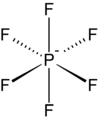
- Гексафторфосфат — обычный слабокоординирующий анион .
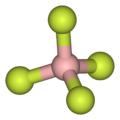
- Как показано на примере небольшого тетрафторбората противоаниона ( BF −
4 ), липофильные катионы имеют тенденцию быть симметричными и однозарядными.
- Липофильные противокатионы
- Хлорид бис(трифенилфосфин)иминия представляет собой хлоридную соль объемистого липофильного катиона фосфония [Ph 3 PNPph 3 ] + .
- Хлорид тетрафенилфосфония (C 6 H 5 ) 4 PCl, сокращенно Ph 4 PCl или PPh 4 Cl — хлорид симметричного катиона фосфония, который часто используется в металлоорганической химии . Соль арсония также хорошо известна.
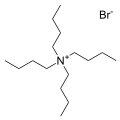
- Бромидная соль тетрабутиламмония , один из наиболее распространенных противокатионов. Известно множество аналогичных «четвертичных солей».
- Катионы щелочных металлов, связанные краун-эфирами , являются обычными липофильными противокатионами, как показано на примере [Li(12-краун-4) 2 ] + .
Многие катионные металлоорганические комплексы выделяются с инертными некоординирующими противоионами. Тетрафторборат ферроцения является одним из таких примеров.
Электрохимия
[ редактировать ]Для достижения высокой ионной проводимости электрохимические измерения проводятся в присутствии избытка электролита. В воде электролитом часто является простая соль, например хлорид калия . Для измерений в неводных растворах используют соли, состоящие как из липофильных катионов, так и из анионов, например гексафторфосфат тетрабутиламмония . Даже в таких случаях на потенциалы влияет образование ионных пар , эффект, который усиливается в растворителях с низкой диэлектрической проницаемостью . [3]
Стабильность противоиона
[ редактировать ]Во многих случаях противоион просто обеспечивает заряд и липофильность, что позволяет манипулировать его ионом-партнером. Ожидается, что противоион будет химически инертен. Для контранионов инертность выражается в низкой основности по Льюису . Противоионы в идеале прочные и нереакционноспособные. Для четвертичных противокатионов аммония и фосфония инертность связана с их устойчивостью к деградации сильными основаниями и сильными нуклеофилами.
Ссылки
[ редактировать ]- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Интернет-исправленная версия: (2006–) « Противоионы ». два : 10.1351/goldbook.C01371
- ^ И. Кроссинг и И. Раабе (2004). «Некоординирующие анионы - факт или вымысел? Обзор вероятных кандидатов». Angewandte Chemie, международное издание . 43 (16): 2066–2090. дои : 10.1002/anie.200300620 . ПМИД 15083452 .
- ^ Гейгер, В.Е., Барьер, Ф., «Металлоорганическая электрохимия на основе электролитов, содержащих слабокоординирующие фторарилборатные анионы», Acc. хим. Рез. 2010, 43, 1030. дои : 10.1021/ar1000023
![Тетракис(пентафторфенил)борат лития представляет собой литиевую соль высоколипофильного тетраарилборатного аниона, часто называемого слабокоординирующим анионом.[2]](http://upload.wikimedia.org/wikipedia/commons/thumb/9/90/Lithium-tetrakis%28pentafluorophenyl%29borate-2D-skeletal.png/152px-Lithium-tetrakis%28pentafluorophenyl%29borate-2D-skeletal.png)

![Хлорид бис(трифенилфосфин)иминия представляет собой хлоридную соль объемистого липофильного фосфониевого катиона [Ph3PNPph3]+.](http://upload.wikimedia.org/wikipedia/commons/thumb/9/99/PPNCl.png/180px-PPNCl.png)

![Катионы щелочных металлов, связанные краун-эфирами, являются обычными липофильными противокатионами, как показано на примере [Li(12-краун-4)2]+.](http://upload.wikimedia.org/wikipedia/commons/thumb/d/da/Bis%2812-crown-4%29lithium-cation-from-xtal-3D-balls-B.png/118px-Bis%2812-crown-4%29lithium-cation-from-xtal-3D-balls-B.png)