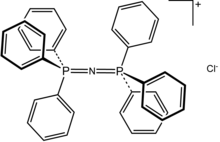
Бис(трифенилфосфин)иминия хлорид
| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Гексафенил-1λ 5 -дифосфат-1-ен-3-ий хлорид | |
| Другие имена
ПНП хлорид
ППН хлорид Бис(трифенилфосфин)иминия хлорид Бис(трифенилфосфоранилиден)иминия хлорид Хлорид бис(трифенилфосфоранилиден)аммония Гексафенилдифосфазения хлорид Селектофор | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.040.139 |
| Номер ЕС |
|
ПабХим CID
|
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| [((C 6 H 5 ) 3 P) 2 N]Cl | |
| Молярная масса | 574.03 g/mol |
| Появление | бесцветное твердое вещество |
| Температура плавления | От 260 до 262 ° C (от 500 до 504 ° F; от 533 до 535 К) |
| умеренный | |
| Опасности | |
| СГС Маркировка : | |

| |
| Предупреждение | |
| Х315 , Х319 , Х332 , Х335 | |
| P261 , P264 , P271 , P280 , P302+P352 , P304+P312 , P304+P340 , P305+P351+P338 , P312 , P321 , P332+P313 , P337+P313 , P362 , P403+P233 , П405 , П501 | |
| Родственные соединения | |
Родственные соединения
|
Тетрафениларсония хлорид Тетрабутиламмоний хлорид |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Хлорид бис(трифенилфосфин)иминия представляет собой химическое соединение с формулой [((C 6 H 5 ) 3 P) 2 N]Cl , часто сокращенно [(Ph 3 P) 2 N]Cl , где Ph – фенил C 6 H 5 , или даже сокращенно [PPN]Cl или [PNP]Cl, или PPNCl, или PNPCl, где PPN или PNP означает (Ф 3 П) 2 Н . Эта бесцветная соль является источником [(Ф 3 П) 2 Н] + катион (сокращенно ППН + или ПНП + ), который используется в качестве нереакционноспособного и слабокоординирующего катиона для выделения реакционноспособных анионов. [(Ф 3 П) 2 Н] + представляет собой фосфазен .
Синтез и структура
[ редактировать ][(Ph 3 P) 2 N]Cl получают в две стадии из трифенилфосфина. Ф 3 П : [ 1 ]
- Ф 3 П + Cl 2 → Ф 3 PCl 2
Это дихлорид трифенилфосфина. Ph 3 PCl 2 относится к пентахлориду фосфора. ПКл 5 . Обработка этого вида гидроксиламином в присутствии Ph 3 P приводит к замене двух одинарных связей P–Cl в Ph 3 PCl 2 по одной двойной связи P=N:
- 2 Ph 3 PCl 2 + NH 2 OH·HCl + Ph 3 P → [(Ph 3 P) 2 N]Cl + 4HCl + Ph 3 PO
оксид трифенилфосфина Ph 3 PO является побочным продуктом.
Хлорид бис(трифенилфосфин)иминия описывается как [(Ф 3 П) 2 Н] + кл. − . Строение катиона бис(трифенилфосфин)иминия [(Ф 3 П) 2 Н] + является [Ф 3 P=N=PPh 3 ] + . Угол P=N=P в катионе гибкий и составляет от ~130 до 180° в зависимости от соли. Изогнутая и линейная формы связей P=N=P наблюдались в одной и той же элементарной ячейке. [ 2 ] Такая же неглубокая потенциальная яма для изгиба наблюдается в изоэлектронной форме бис (трифенилфосфоранилиден) метана , Ph 3 P=C=PPH 3 , а также более отдаленная молекула субоксида углерода , О=С=С=С=О . Для хлоридной соли, не содержащей растворителя [(Ph 3 P) 2 N]Cl валентный угол P=N=P был определен как 133°. [ 3 ] Две связи P=N эквивалентны, их длина составляет 1,597(2) Å.

Использовать в качестве реагента
[ редактировать ]В лаборатории, [(Ph 3 P) 2 N]Cl является основным предшественником [(Ф 3 П) 2 Н] + соли. Используя реакции солевого обмена, нитрит , азид и другие небольшие неорганические анионы. можно получить [(Ф 3 П) 2 Н] + катионы. Полученные соли [(Ф 3 П) 2 Н] + НЕТ - 2 , [(Ф 3 П) 2 Н] + N - 3 и др. растворимы в полярных органических растворителях.
[(Ф 3 П) 2 Н] + образует кристаллические соли с рядом анионов, которые иначе трудно кристаллизовать. Его эффективность частично объясняется его жесткостью, отражающей наличие шести фенильных колец. Часто [(Ф 3 П) 2 Н] + образует соли, которые более стабильны на воздухе, чем соли с меньшими катионами, например, содержащие четвертичного аммония. катион [№ 4 ] + , или катионы щелочных металлов . Этот эффект объясняется стерическим экранированием, обеспечиваемым этим объемным катионом. Иллюстративный [(Ф 3 П) 2 Н] + соли реакционноспособных анионов включают [(Ф 3 П) 2 Н] + [HFe(CO) 4 ] − , [(Ф 3 П) 2 Н] + [Со(СО) 4 ] − , ([(Ф 3 П) 2 Н] + ) 2 [М 2 (СО) 10 ] 2+ (M = Cr, Mo, W) и [(Ф 3 П) 2 Н] + [Fe(CO) 3 (NO)] − . [ 1 ] Роль ионного спаривания в химических реакциях часто проясняется путем изучения родственной соли, полученной из [(Ф 3 П) 2 Н] + .
Родственные катионы
[ редактировать ]Катион фосфазения, родственный [(Ф 3 П) 2 Н] + является [((СН 3 ) 2 Н) 3 Р) 2 Н] + . [ 4 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б Рафф, Дж. К.; Шлинц, WJ (1974). «Соли μ-нитридобиса (трифенилфосфора) (l +) («PPN») с карбонильными анионами металлов». Неорганические синтезы . Том. 15. С. 84–90. дои : 10.1002/9780470132463.ch19 . ISBN 9780470132463 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Харди Дж.Е., Цинк Дж.И., Каска В.К., Болдуин Дж.К. (декабрь 1978 г.). «Структура и триболюминесценция полиморфов гексафенилкарбодифосфорана». Журнал Американского химического общества . 100 (25): 8001–8002. дои : 10.1021/ja00493a035 .
- ^ Кнапп С., Узун Р. (ноябрь 2010 г.). «Безсольватный бис-(трифенилфосфин)иминийхлорид» . Acta Crystallographica Раздел E. 66 (Часть 12): o3185. дои : 10.1107/S1600536810046325 . ПМК 3011587 . ПМИД 21589480 .
- ^ Швезингер, Рейнхард (2001). «1,1,1,3,3,3-Гексакис(диметиламино)-1λ5,3λ5-дифосфазения фторид». Электронная энциклопедия реагентов для органического синтеза EROS . стр. 1–2. дои : 10.1002/047084289X.rh014m . ISBN 0471936235 .