Трис (диметиламино) Метан

| |

| |

| |
| Имена | |
|---|---|
| Предпочтительное имя IUPAC
N , N , N ′ , N ' , N ′ ′ , N ′ ′ -Hexamethylmethanetriamine | |
| Другие имена
N , n , n , n , n , n -гексаметилметанетриамин
[Бис (диметиламино) метил] диметиламин | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Echa Infocard | 100.024.804 |
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 7 H 19 N 3 | |
| Молярная масса | 145.250 g·mol −1 |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Трис (диметиламино) Метан (TDAM) является самым простым репрезентативным метана Tris (диалкиламино) общей формулы (R 2 N) 3 C, в которых три из четырех атомов водорода метана заменяются диметиламино группами (-n (CH 3 ) 2 ). [ 1 ] Трис (диметиламино) метан можно рассматривать как амин и ортоамид .
Трис (диметиламино) Метан является сильным основанием и может использоваться в качестве агенталирования , в качестве реагента аминометиленации и в качестве источника для основного бис (диметиламино) карбена формулы (R 2 N) 2 C:. [ 2 ]
Подготовка
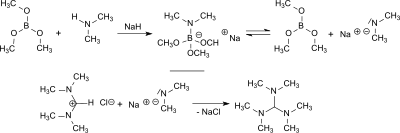
[ редактировать ]Трис (диметиламино) Метан образуется в реакции N, N, N ', N'-тетраметилформамидиния хлорид (TMF-CL) [ 1 ] [ 3 ] [ 4 ] или бис (диметиламино) ацетонитрил [ 5 ] с литием диметиламида или диметиламида натрия с выходом от 55 до 84%. [ 2 ]
Из диметиламина и триметоксиранового диметиламида натрия образуется in situ в присутствии гидрида натрия , который реагирует с N , N , N ' , N ' -Tetramethylformamidinium Chloride с выходом 84% с Tris (диметиламино) и с бис (диметиламино) ацетонитрил в 77%. [ 6 ]
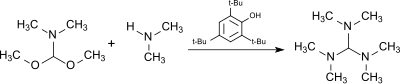
Реакция диметилформамидного (DMF) диметилацетального, HC (OCH 3 ) 2 N (CH 3 ) 2 , (из комплекса DMF -диметилсульфата и метоксида натрия [ 7 ] ) с диметиламином в присутствии кислого катализатора 2,4,6-третт - бутилфенол (который в значительной степени стабилен для алкилирующего агента ) продуцирует метан трис (диметиламино). [ 8 ]
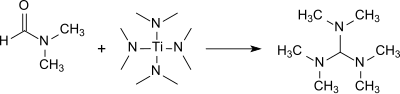
Трис (диметиламино) Метан образуется с хорошим выходом (83%) в реакции DMF с тетракисом (диметиламино) титаном (IV) . [ 9 ]
N , n , n ′ , n ' , n ″, n ″ -hexamethylguanidinium хлорид (легко доступный диметиламином и N , N , N ' , N ' -тетраметилхлорформамидином хлоридом, полученным из тетраметилореа и phosgene [ 10 ] ) образует трис (диметиламино) метан в 53% урожайности при воздействии BIS натрия с восстановительным агентом (2-метокситокси) алюминиевого гидрида (Red-Al). [ 11 ]
Гидрид натрия и триметил борат уменьшают N , N , N ' , N ' , N ″, N ″ -Hexamethylguanidinium Chloride с выходом 80% до метана Tris (диметиламино). [ 6 ]
Характеристики
[ редактировать ]Трис (диметиламино) Метан представляет собой прозрачную, бесцветную или бледно -желтую жидкость с сильным аммиачным запахом. Соединение свободно смешивается со многими неполярными апритомими и без воды растворителями. Однако, когда нагретый трис (диметиламино) метатан реагирует с протекащими растворителями (такими как вода или спирты), а также со слабыми х-ацидическими веществами, такими как ацетон или ацетонитрил . [ 2 ]
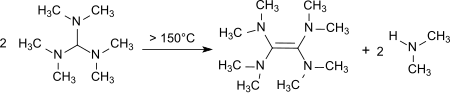
При нагревании до 150–190 ° C происходит разложение с образованием тетракиса (диметиламино) Этена , [ 12 ] Сильный донор электронов . [ 13 ]
Приложения
[ редактировать ]Трис (диметиламино) метан диссоциирует на катионы N , N , N ' , N' - Tetramethylformamidinium и диметиламидные анионы, которые абстрактные протоны из CH- и NH-ацидических соединений. Таким образом, образованные анионы добавляют к катионам формамидиния, которые, в свою очередь, устраняют диметиламин и реагируют с образованием диметиламинометилентных соединений (= CH - N (CH 3 ) 2 ) или амидинами путем аминометиленаации. [ 1 ]
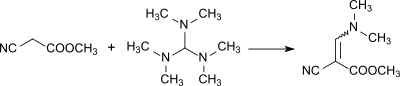
Реакция с образованием метил α-циано-β-диметиламиноакрилат:
Реакция с образованием n , n -диметил -н ' - p -нитрофенилформамидина:
Аминометиленация обеспечивает интермедиаты для синтеза гетероциклов, таких как пиримидины , пиразолы , 1,4-дигидропиридины и индолы .
N , N , N ′ , N ' -Tetramethyl Selenourea доступен путем расширенного нагрева метана Tris (диметиламино) с селеном в ксилоле , бис (диметиламино) карбене предлагается в качестве промежуточного звена. [ 14 ]
Связанный реагент
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный в Bredereck, H.; Effenberger, F.; Брендл Т. (1966). «Синтез и реакции трисдиметиламинометана» [синтез и реакция трис (диметиламино) метана]. Прикладная химия (на немецком языке). 78 (2): 147–148. Bibcode : 19666angch..78..147b . Doi : 10.1002/прикреплен .
- ^ Jump up to: а беременный в Kantlehner, W. (2001). «Трис (диметиламино) метатан». Энциклопедия реагентов для органического синтеза . doi : 10.1002/047084289x.rt403 . ISBN 0-471-93623-5 .
- ^ DE 1217391 , Bredereck, H.; Effenberger, F. & Brendle, T., «Процедура производства трис-диметиламинометана (процесс производства Tris (диметиламино) метана)», выпущенный 1966-12-08, назначенный Bredereck H.
- ^ Bredereck, H.; Effenberger, F.; Брендл, Т.; Muffler, H. (1968). «Ортоамид. В. Синтез трис-диалкаламино-метан» [ортоамиды. V. Синтез трис (диметиламино) метана]. Химические отчеты (на немецком языке). 101 (5): 1885–1888. Doi : 10.1002/cber.19681010541 .
- ^ Kantlehner, W.; Maier, T.; Speh, P. (1979). «Трис (диалкиламино) метан и тетраалкилформамидиние-тиоцианат aus bis (диалкиламино) ацетонитриллен» [Tris (диалкиламино) метан и тетраалкилформамидиниевые тиоцианаты из бис (диалкиламино) ацетонитрила]. Синтез (на немецком языке). 1979 (5): 342–343. doi : 10.1055/s-1979-28671 . S2CID 97378246 .
- ^ Jump up to: а беременный Kantlehner, W.; Stieglitz, R.; Hauber, M.; Haug, E.; Регулирование, C. (2000). «Ортоамид. Lii. Вклад в синтез команды ортокарбоновой кислоты» [ортоамиды. Lii. Статьи о синтезе ортоамидов карбоновой кислоты]. Журнал практической химии (на немецком языке). 342 (3): 256–268. Doi : 10.1002/(SICI) 1521-3897 (20003) 342: 3 <256 :: AID-PRAC256> 3.0.co ;
- ^ Bredereck, H.; Effenberger, F.; Симхен, Г. (1961). «Реактивные кислоты-диметилсульфатные комплексы» [реактивные кислотные амид-диметилсульфатные комплексы]. Прикладная химия (на немецком языке). 73 (14): 493. Bibcode : 1961angch..73..493b . Doi : 10.1002/прикреплен .
- ^ DE 2214497 , Leimgruber, W. & Wick, AE, «Процедура производства аминозамещенных механдеров (процесс производства аминозамещенного производного метана)», выпущенный 1972-05, назначенный F. Hoffmann-La Roche & Co.
- ^ Weingarten, H.; Уайт, Вашингтон (1966). «Новая реакция аминации производных карбоновых кислот с тетракисом (диметиламино) титана». Журнал Американского химического общества . 88 (4): 850. doi : 10.1021/ja00956a049 .
- ^ Kantlehner, W.; Haug, E.; Mergen, WW; Speh, P.; Maier, T.; Capassakalidis, JJ; Bräuner, HJ; Hagen, H. (1983). «Производственный процесс для N , N , N ' , N ' , N ″, N ″ HexaAlcylguanidinium хлориды» [процесс производства для N , N , N ′ , N ' , N HexaAlcylguanidinum хлориды ″ ]. Синтез (на немецком языке). 1983 (11): 904–905. Doi : 10.1055/s-1983-30558 . S2CID 93420838 .
- ^ Kantlehner, W.; Speh, P.; Bräuner, HJ (1983). «Простой синтез для трис (диалкиламино) метана» [простой синтез для метантов трис (диалкиламино). Синтез (на немецком языке). 1983 (11): 905–906. Doi : 10.1055/s-1983-30559 . S2CID 101466032 .
- ^ Bredereck, H.; Effenberger, F.; Bredereck, HJ (1966). «Новый синтез тетра (диметиламино) этилен» [новый синтез тетра (диметиламино) этилена] (PDF) . Прикладная химия (на немецком языке). 78 (21): 984. Bibcode : 19666angch..78..984b . Doi : 10.1002/Прилагается .
- ^ Wiberg, N.; Бухлер, JW (1962). «Тетракис (диметиламино) этилен: сильный электронононатор» [Тетракис (диметиламино) этилен: сильный донор электронов]. Прикладная химия (на немецком языке). 74 (14): 490–491. Bibcode : 1962angch..74..490W . Doi : 10.1002/Прилагается .
- ^ Kantlehner, W.; Hauber, M.; Феттель М. (1996). «Ортоамид. Il. Реализация производных ортоамидов с серной и селенами, синтеза 1,3 -азола и 1,3 селеназелеривата» [ортоамиды. Xlix. Реакции производного ортоамида с серой и селенами, синтезы 1,3-тиазола и 1,3 производных селеназола]. Журнал практической химии (на немецком языке). 338 (1): 403–413. Doi : 10.1002/prac.19963380180 .