Клатратное соединение
Клатрат , – это химическое вещество состоящее из решетки , которая улавливает или удерживает молекулы. Слово клатрат происходит от латинского clathratus ( clatratus ), что означает «с решетками, с решеткой ». [ 1 ] Большинство клатратных соединений являются полимерными и полностью окутывают молекулу гостя, но в современном использовании клатраты также включают комплексы хозяин-гость и соединения включения . [ 2 ] Согласно ИЮПАК , клатраты представляют собой соединения включения, «в которых молекула-гость находится в клетке, образованной молекулой-хозяином или решеткой молекул-хозяина». [ 3 ] Этот термин относится ко многим молекулярным хозяевам, включая каликсарены и циклодекстрины и даже к некоторым неорганическим полимерам, таким как цеолиты .
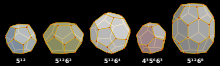
Клатраты можно разделить на две категории: клатратные гидраты и неорганические клатраты. Каждый клатрат состоит из фреймворка и гостей, находящихся в фреймворке. Наиболее распространенные кристаллические структуры клатрата могут состоять из полостей, таких как додекаэдрические , тетракаидекаэдрические и гексакаидекаэдрические полости.
Молярная доля воды большинства клатратных гидратов составляет 85%. Клатратные гидраты происходят из органических каркасов с водородными связями . Эти каркасы изготавливаются из молекул, которые «самоассоциируются» за счет множественных взаимодействий водородных связей. Маленькие молекулы или газы (например, метан, углекислый газ, водород) могут быть заключены в гидраты в качестве гостя. Идеальное соотношение «гость/хозяин» для клатратных гидратов составляет от 0,8 до 0,9. Взаимодействие гостя с хозяином ограничивается силами Ван-дер-Ваальса . Определенные исключения существуют у семиклатратов , где гости включаются в структуру хозяина посредством водородных связей со структурой хозяина. Гидраты образуются часто при частичном заполнении гостей и разрушаются при отсутствии гостей, занимающих водные клетки. Как и лед, клатратные гидраты стабильны при низких температурах и высоком давлении и обладают сходными свойствами, такими как электрическое сопротивление. Клатратные гидраты встречаются в природе и могут быть обнаружены в вечной мерзлоте и океанических отложениях. Гидраты также можно синтезировать путем затравочной кристаллизации или использования аморфных предшественников для зародышеобразования. [ 4 ]
В отличие от гидратов, неорганические клатраты имеют ковалентно связанный каркас из неорганических атомов с гостями, обычно состоящими из щелочных или щелочноземельных металлов . Из-за более прочной ковалентной связи клетки часто меньше, чем гидраты. Атомы гостя взаимодействуют с хозяином посредством ионных или ковалентных связей. Следовательно, частичное замещение атомов-гостей следует правилам Цинтля, так что заряд всего соединения сохраняется. Большинство неорганических клатратов имеют полное заполнение своих каркасных клеток атомом-гостем, чтобы находиться в стабильной фазе. Неорганические клатраты можно синтезировать прямой реакцией с использованием шаровой мельницы при высоких температурах или высоких давлениях. Кристаллизация из расплава по другому распространенному пути синтеза. Благодаря большому разнообразию состава видов-хозяев и гостей неорганические клатраты значительно более разнообразны по химическому составу и обладают широким спектром свойств. В частности, неорганические клатраты могут быть как изолятором, так и сверхпроводником (Ba 8 Si 46 ). Общим свойством неорганических клатратов, привлекавшим исследователей, является низкая теплопроводность . Низкая теплопроводность объясняется способностью атома-гостья «греметь» внутри каркаса-хозяина. Свобода движения атомов-гостей рассеивает фононы , переносящие тепло. [ 4 ]

Примеры
[ редактировать ]
Клатраты были исследованы для многих применений, включая хранение газа, добычу газа, разделение газа, опреснение , термоэлектрику , фотогальванику и батареи.
- Клатратные соединения формулы A 8 B 16 X 30 , где A – щелочноземельный металл , B – элемент III группы , а X – элемент IV группы, исследованы для термоэлектрических устройств. Термоэлектрические материалы следуют стратегии проектирования, называемой концепцией электронного кристалла фононного стекла . [ 6 ] [ 7 ] желательны низкая теплопроводность и высокая электропроводность Для создания эффекта Зеебека . Когда каркас гостя и хозяина настроены соответствующим образом, клатраты могут проявлять низкую теплопроводность, т. е. поведение фононного стекла , в то время как электропроводность через каркас хозяина не нарушается, что позволяет клатратам проявлять электронный кристалл .
- Клатраты метана имеют каркас с водородными связями, образованный водой и молекулами-гостями метана. Большие количества метана, замороженного в этой форме естественным путем, существуют как в вечной мерзлоте, так и под морским дном океана. [ 8 ] Другие сети с водородными связями происходят из гидрохинона , мочевины и тиомочевины . Хорошо изученной молекулой-хозяином является соединение Дианина .

- Клатраты Гофмана представляют собой координационные полимеры с формулой Ni(CN) 4 ·Ni(NH 3 ) 2 (арен). Эти материалы кристаллизуются с небольшими ароматическими компонентами (бензолом, некоторыми ксилолами), и эта селективность использовалась в коммерческих целях для разделения этих углеводородов. [ 2 ] Металлоорганические каркасы (МОФ) образуют клатраты.

История
[ редактировать ]Клатратные гидраты были открыты в 1810 году Хамфри Дэви . [ 9 ] Клатраты изучались П. Пфайфером в 1927, а в 1930 Э. Гертель определил «молекулярные соединения» как вещества, разлагающиеся на отдельные компоненты по закону действия масс в растворенном или газообразном состоянии. В 1934 году Хаммершмидт обнаружил, что клатратные гидраты образуют засоры в газопроводах, что привело к увеличению количества исследований по предотвращению образования гидратов. [ 10 ] В 1945 году Х. М. Пауэлл проанализировал кристаллическую структуру этих соединений и назвал их клатратами . Производство газа с помощью гидратов метана с тех пор было реализовано и испытано для производства энергии в Японии и Китае. [ 4 ]
Похожие материалы
[ редактировать ]Соединения включения часто представляют собой молекулы, тогда как клатраты обычно представляют собой полимеры. [ нужна ссылка ] . Интеркаляционные соединения не являются трехмерными, в отличие от клатратных соединений. Фотолитически чувствительные клеточные соединения были исследованы в качестве контейнеров для высвобождения лекарственного средства или реагента . [ 11 ]
Цеолиты — это еще один тип кристаллических структур, образующих каркас с полостями, в которых могут обитать виды-гости. В отличие от клатратов, цеолиты представляют собой тетраэдры, соединяющие четыре атома кислорода, окружающие катион. [ нужна ссылка ] Гости также не обязаны заполнять открытые полости. Структуры цеолита определяются разнообразными строительными единицами каркаса, в отличие от полых структур в клатратах. Подобные приложения были исследованы.
Кремнеземный клатрасил представляет собой соединения, структурно подобные клатратным гидратам с каркасом SiO 2 , и могут быть обнаружены в различных морских отложениях. [ 12 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Латинский словарь. Архивировано 14 апреля 2012 г. в Wayback Machine.
- ^ Перейти обратно: а б Этвуд, Дж. Л. (2012) «Соединения включения» в Энциклопедии промышленной химии Ульмана . Wiley-VCH, Вайнхайм. дои : 10.1002/14356007.a14_119
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Исправленная онлайн-версия: (2006–) « Клатраты ». два : 10.1351/goldbook.C01097
- ^ Перейти обратно: а б с д и Кришна, Лакшми; Кох, Кэролайн А. (февраль 2015 г.). «Неорганические и метановые клатраты: универсальность соединений «гость-хозяин» для сбора энергии» . MRS Энергетика и устойчивое развитие . 2 (1): 8. дои : 10.1557/mre.2015.9 . ISSN 2329-2229 .
- ^ Бирчалл, Т.; Фрэмптон, CS; Шробильген, Г.Дж.; Валсдоттир, Дж. (1989). «Б-гидрохинон клатрат ксенона». Acta Crystallographica Раздел C. Связь с кристаллической структурой . 45 (6): 944–946. Бибкод : 1989AcCrC..45..944B . дои : 10.1107/S0108270188014556 .
- ^ Нолас, Г.С.; Кон, Дж.Л.; Слэк, Джорджия; Шуйман, С.Б. (13 июля 1998 г.). «Полупроводниковые клатраты Ge: многообещающие кандидаты для термоэлектрических применений» . Письма по прикладной физике . 73 (2): 178–180. Бибкод : 1998АпФЛ..73..178Н . дои : 10.1063/1.121747 . ISSN 0003-6951 .
- ^ Бикман М., Морелли Д.Т., Нолас Г.С. (2015). «Лучшие термоэлектрики за счет стеклоподобных кристаллов». Природные материалы . 14 (12): 1182–1185. Бибкод : 2015NatMa..14.1182B . дои : 10.1038/nmat4461 . ISSN 1476-4660 . ПМИД 26585077 .
- ^ Пирс, Фред (27 июня 2009 г.). «Лед в огне: следующее ископаемое топливо» . Новый учёный . № 2714. С. 30–33. Архивировано из оригинала 13 апреля 2016 года . Проверено 5 июля 2009 г.
- ^ Томас, Эллен (ноябрь 2004 г.). «Клатраты: малоизвестные компоненты глобального углеродного цикла» . Уэслианский университет . Проверено 13 декабря 2007 г.
- ^ Хаммершмидт, Э.Г. (1 августа 1934 г.). «Образование газовых гидратов в магистральных газопроводах» . Промышленная и инженерная химия . 26 (8): 851–855. дои : 10.1021/ie50296a010 . ISSN 0019-7866 .
- ^ Эллис-Дэвис, Грэм CR (2007). «Соединения в клетках: технология фотовысвобождения для контроля клеточной химии и физиологии» . Природные методы . 4 (8): 619–628. дои : 10.1038/nmeth1072 . ПМК 4207253 . ПМИД 17664946 .
- ^ ; Икеда, Нишикубо, Кацуми; Хонма, Чибуне; Фурукава, Ёсихиро; Кудо, Ясухиро (сентябрь 2011 г.). Момма, Коичи газовые гидраты» . Nature Communications . 2 (1): 196. Бибкод : 2011NatCo...2..196M . doi : 10.1038/ncomms1196 . ISSN 2041-1723 . PMID 21326228 .