Тетрахлорокупрат(II) калия
| |
| Имена | |
|---|---|
| Название ИЮПАК
Тетрахлорокупрат(II) калия
| |
| Другие имена
Тетрахлоркупрат калия, тетрахлорид калия-меди(II), хлорид двухкалия-медь, мичерлихит (минерал дигидрат)
| |
| Идентификаторы | |
| |
ПабХим CID
|
|
| Характеристики | |
| К 2 CuCl 4 (безводный) K 2 CuCl 4 ·2H 2 O (дигидрат) | |
| Молярная масса | 319,585 г/моль (дигидрат) |
| Появление | зеленовато-синие кристаллы (дигидрат) |
| Плотность | 2,416 г/см 3 при 25 °C (дигидрат) [1] |
| Структура | |
| (дигидрат:) Тетрагональный.Точечная группа: 4/м 2/м 2/м (вероятно). Кристаллы короткопризматические вдоль [001] или пирамидальные {011}, мелкие; в сталактитовых наростах [2] | |
| Опасности | |
| точка возгорания | Невоспламеняющийся |
| Родственные соединения | |
Другие катионы
|
Тетрахлоридокупрат цезия(II) тетрахлорокупрат(II) аммония тетрахлорокупрат(II) рубидия тетрахлорокупрат(II) железа(II) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
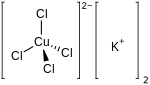
Тетрахлорокупрат(II) калия представляет собой соль формулы химической K.
2 CuCl
4 , также записываемый как ( K +
) 2 ·[ CuCl
4 ] 2− .
Соединение часто встречается в виде дигидрата K.
2 CuCl
4 · 2ч
2 O — блестящее зеленовато-голубое кристаллическое вещество. [1] Эта форма также встречается в природе как редкий минерал мичерлихит . [1] [2]
Соединение также называют тетрахлоркупратом калия (II) , тетрахлоркупратом дикалия , тетрахлоридом меди (II) калия , хлоридом меди (II) и другими подобными названиями.
дигидрат
[ редактировать ]
2 CuCl
4 · 2ч
2 О (на сетке 1 мм)
Синтез и естественное возникновение
[ редактировать ]Дигидрат редко встречается в природе вблизи жерл вулканов , например, на горе Везувий , как минерал мичерлихит; назван в честь Эйльхардта Мичерлиха (1794–1863), немецкого кристаллографа и химика, который впервые синтезировал это соединение. [2] Он был идентифицирован как пигмент в некоторых древних артефактах. [3]
Дигидрат можно получить медленным упариванием раствора хлорида калия ( KCl ) и хлорида меди(II) ( CuCl).
2 ) в молярном соотношении 2:1. [1] [4]

2 CuCl
4 · 2ч
2 О (мичерлихит).
Кристаллическая структура
[ редактировать ]Кристаллическая структура дигидрата была частично определена в 1927 году Хендриксом и Дикинсоном . [1] [4] и уточнен в 1934 году Хробаком. [5] Структура тетрагональная P4 2 /мнм (136), Z=2, изоструктурна тетрахоридокупрату(II) аммония ( NH
4 ) 2 CuCl
4 · 2ч
2 O и тетрахоридокупрат(II) рубидия Rb
2 CuCl
4 · 2ч
2О . [1] [4] [5] [6] [7] Каждый атом меди непосредственно окружен двумя атомами кислорода и четырьмя атомами хлора, образуя гидратированный анион тетрахлордокупрата(II) . Два атома хлора находятся примерно на 0,75 ангстрем дальше, чем два других. Каждый атом калия окружен четырьмя атомами кислорода, четырьмя атомами меди и восемью атомами хлора. [4]
Безводный
[ редактировать ]Синтез
[ редактировать ]О безводном соединении сообщили в 1952 г. К.М. Фонтана и другие. [8] В следующие два десятилетия другие сообщили о температуре его формирования. [9] и его структура. [6] [7]
Однако в середине 1970-х годов его существование было поставлено под сомнение. [10] [11] Фазовая диаграмма безводной системы KCl / CuCl
2 изображен трихлоридокупрат калия KCuCl.
3 как конгруэнтно плавящееся соединение, но не K
2 CuCl
4 . [12] Дигидрат разлагается при нагревании выше 93 °C до KCl , KCuCl.
3 и вода. [13] [14]
Сомнения развеялись, когда в 1975 году Т. Дж. Нолан и другие добились успешного обезвоживания. [15] [16]
См. также
[ редактировать ]- Трихлорокупрат(II) калия , KCuCl
3
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж Ховард Э. Суонсон, Ховард Ф. Макмерди, Марлен К. Моррис, Элоиза Х. Эванс и Борис Парецкин (1971) Гидрат хлорида меди и калия (мичерлихит) , в [Стандартные рентгеновские дифракционные порошковые картины] Национальное бюро стандартов, монография 25, раздел 9; страница 34.
- ^ Jump up to: а б с Джон В. Энтони, Ричард А. Бидо, Кеннет В. Блад и Монте К. Николс (1997) Мичерличит , в Справочнике по минералогии , Минералогическое общество Америки. том III.
- ^ Ридерер (1982)
- ^ Jump up to: а б с д Стерлинг Б. Хендрикс и Роско Г. Дикинсон (1927). Кристаллические структуры дигидратов хлоридов меди аммония, калия и рубидия. Журнал Американского химического общества, том 49, выпуск 9, страницы 2149–2162. два : 10.1021/ja01408a005
- ^ Jump up to: а б Хробак (1934)
- ^ Jump up to: а б Э. Жоли (1971). ЧР акад. наук, сер. С, том 271, стр. 1302.
- ^ Jump up to: а б I. V. Vasil'kova and G. M. Barvinok (1966). Chemical Abstracts, volume 65, page 9831.
- ^ CM Fontana, E. Gorin, GA Kidder и CS Meredith (1952). Индийский англ. Хим., том 44, стр. 363
- ^ С. А. Щукарев, И. В. Василькова и Г. М. Барвинок (1965). Вестн. Ленинград. ун-та, сер. Мат. Физический. хим., том 20, стр. 145.
- ^ HT Witteveen, DL Jongejan и W. Brandwijk (1974). Матер. Рез. Бюлл., том 9, стр. 345.
- ^ Д. В. Смит (1976), Хлорокупраты (II) . Обзоры координационной химии, том 21, выпуски 2–3, страницы 93–158. два : 10.1016/S0010-8545(00)80445-2
- ^ М. П. Воробей и О. В. Скиба (1970). Расс. Дж. Неорг. Хим., том 15, стр. 725.
- ^ Р. Перре (1966). Бык. Соц. Хим. Фр., том 1966, стр. 3190.
- ^ Х. Суга, М. Сорай, Т. Якамана и С. Секи (1965). Бык. хим. Соц. Япония, том 38, стр. 1007.
- ^ Н. Фогель и Ти Джей Нолан (1975). амер. хим. Соц. Symp., раздел Inorg., стр. 121.
- ^ Томас Дж. Нолан, Гарольд Харалсон, Джеймс Л. МакАдамс и Норман Фогель (1977) Дегидратация дигидрата тетрахлоркупрата (II) калия. Журнал Химического общества, Dalton Transactions, том 1977, выпуск 17, страницы 1608–1612. два : 10.1039/DT9770001608