Йодид меди(I)
 | |
| Имена | |
|---|---|
| Название ИЮПАК Йодид меди(I) | |
| Другие имена Йодид меди, маршит | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.028.795 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Который | |
| Молярная масса | 190.45 g/mol |
| Появление | Белый твердый |
| Запах | без запаха |
| Плотность | 5,67 г/см 3 [1] |
| Температура плавления | 606 ° C (1123 ° F; 879 К) |
| Точка кипения | 1290 ° C (2350 ° F; 1560 К) (разлагается) |
| 0,000042 г/100 мл | |
Произведение растворимости ( K sp ) | 1,27 х 10 −12 [2] |
| Растворимость | растворим в аммиака и йодида растворах нерастворим в разбавленных кислотах |
| Давление пара | 10 мм рт.ст. (656 °С) |
| -63.0·10 −6 см 3 /моль | |
Показатель преломления ( n D ) | 2.346 |
| Структура | |
| цинковая обманка | |
| Тетраэдрические анионы и катионы | |
| Опасности | |
| СГС Маркировка : | |
   | |
| Опасность | |
| Х302 , Х315 , Х319 , Х335 , Х410 | |
| П261 , П273 , П305+П351+П338 , П501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Невоспламеняющийся |
| NIOSH (пределы воздействия на здоровье в США): | |
МЕХ (Допускается) | СВВ 1 мг/м 3 (туз С) [3] |
РЕЛ (рекомендуется) | СВВ 1 мг/м 3 (туз С) [3] |
IDLH (Непосредственная опасность) | СВВ 100 мг/м 3 (туз С) [3] |
| Паспорт безопасности (SDS) | Сигма Олдрич |
| Родственные соединения | |
Другие анионы | |
Другие катионы | йодид серебра |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Йодид меди(I) — неорганическое соединение формулы CuI. Он также известен как йодид меди . Он полезен во множестве применений, начиная от органического синтеза и заканчивая засевом облаков .
Йодид меди(I) имеет белый цвет, но образцы часто кажутся коричневыми или даже, если они встречаются в природе как редкий минерал маршит , красновато-коричневыми, но такой цвет обусловлен наличием примесей. Образцы йодидсодержащих соединений обычно обесцвечиваются из-за легкого аэробного окисления йодид-аниона до молекулярного йода. [4] [5] [6]
Структура
[ редактировать ]меди(I) Йодид , как и большинство бинарных (содержащих только два элемента) галогенидов металлов, представляет собой неорганический полимер . Он имеет богатую фазовую диаграмму , что означает, что он существует в нескольких кристаллических формах. Он принимает структуру цинковой обманки при температуре ниже 390 ° C (γ-CuI), структуру вюрцита при температуре от 390 до 440 ° C (β-CuI) и структуру каменной соли при температуре выше 440 ° C (α-CuI). Ионы тетраэдрически координированы в структуре цинковой обманки или вюрцита с расстоянием Cu-I 2,338 Å. Бромид меди(I) и хлорид меди(I) также переходят из структуры цинковой обманки в структуру вюрцита при 405 и 435 °С соответственно. Следовательно, чем больше длина связи медь-галогенид, тем ниже должна быть температура, чтобы изменить структуру от структуры цинковой обманки к структуре вюрцита. Межатомные расстояния в бромиде меди(I) и хлориде меди(I) составляют 2,173 и 2,051 Å соответственно. [7] В соответствии со своей ковалентностью CuI является полупроводником p-типа. [8]
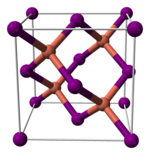 | 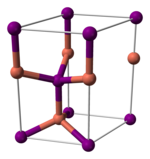 |  |
| γ-CuI | β-CuI | α-CuI |
Подготовка
[ редактировать ]Йодид меди(I) можно получить нагреванием йода и меди в концентрированной иодоводородной кислоте . [9]
Однако в лаборатории йодид меди (I) получают простым смешиванием водного раствора йодида калия и растворимой соли меди (II), такой как сульфат меди (II) . [4]
- С 2+ + 2И − → CuI + 0,5 I 2
Реакции
[ редактировать ]Йодид меди(I) реагирует с парами ртути с образованием тетраиодомеркурата меди:
- 4 CuI + Hg → Cu 2 HgI 4 + 2 Cu
Эту реакцию можно использовать для обнаружения ртути , поскольку изменение цвета от белого (CuI) до коричневого (Cu 2 HgI 4 ) является резким.
Йодид меди(I) используется в синтезе кластеров Cu(I), таких как Cu 6 I − 7 . [10]
Йодид меди(I) растворяется в ацетонитриле с образованием разнообразных комплексов. При кристаллизации молекулярный [11] или полимерный [12] [13] соединения можно выделить. раствора соответствующего комплексообразователя в ацетоне или хлороформе Растворение наблюдается и при использовании . Например, тиомочевину можно использовать и ее производные. Твердые вещества, которые кристаллизуются из этих растворов, состоят из гибридных неорганических цепочек . [14]
Использование
[ редактировать ]В сочетании с 1,2- или 1,3-диаминовыми лигандами CuI катализирует превращение арил- , гетероарил- и винилбромидов в соответствующие иодиды. NaI является типичным источником йодида, а диоксан — типичным растворителем (см. ароматическую реакцию Финкельштейна ). [15]
CuI используется в качестве сокатализатора с палладиевым катализатором в реакции Соногашира . [16]
CuI используется при засеве облаков . [17] изменение количества или типа осадков в облаках или их структуры путем рассеивания в атмосфере веществ, которые повышают способность воды образовывать капли или кристаллы. CuI создает сферу, вокруг которой конденсируется влага в облаке, вызывая увеличение количества осадков и уменьшение плотности облаков.
Структурные свойства CuI позволяют CuI стабилизировать тепло в нейлоне при производстве коммерческих и бытовых ковров, аксессуаров для автомобильных двигателей и на других рынках, где долговечность и вес являются важными факторами. [ нужна ссылка ]
CuI используется в качестве источника пищевого йода в поваренной соли и кормах для животных. [17]
Ссылки
[ редактировать ]- ^ Лиде, Дэвид Р., изд. (2006). Справочник CRC по химии и физике (87-е изд.). Бока-Ратон, Флорида: CRC Press . ISBN 0-8493-0487-3 .
- ^ Джон Рамбл (18 июня 2018 г.). Справочник CRC по химии и физике (99-е изд.). ЦРК Пресс. стр. 4–47. ISBN 978-1138561632 .
- ^ Jump up to: а б с Карманный справочник NIOSH по химическим опасностям. «#0150» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Jump up to: а б Джордж Б. Кауфман, Лоуренс В. Фанг (1983). Йодид меди(I) . Неорганические синтезы. Том. 22. с. 101. дои : 10.1002/9780470132531.ch20 .
- ^ «Верификация» .
- ^ «Список минералов» . 21 марта 2011 г.
- ^ Уэллс А. Ф. (1984). Структурная неорганическая химия (5-е изд.). Оксфорд: Издательство Оксфордского университета. стр. 410 и 444.
- ^ Бидикуди, Мария; Кимакис, Эммануэль (2019). «Новые подходы и перспективы масштабируемости материалов, транспортирующих дырки на основе меди, для плоских перовскитных солнечных элементов» . Журнал химии материалов C. 7 (44): 13680–13708. дои : 10.1039/c9tc04009a .
- ^ Холлеман А.Ф., Виберг Э. (2001). Неорганическая химия . Сан-Диего: Академическая пресса. ISBN 0-12-352651-5 .
- ^ Ю М, Чен Л, Цзян Ф, Чжоу К, Лю С, Сунь С, Ли Х, Ян Ю, Хун М (2017). «Катион-индуцированная стратегия создания кластера Cu6I7– в форме песочных часов и его настраиваемой по цвету люминесценции». Химия материалов . 29 (19): 8093–8099. doi : 10.1021/acs.chemmater.7b01790 .
- ^ Барт Э.Р., Гольц С., Кнорр М., Строманн С. (ноябрь 2015 г.). «Кристаллическая структура ди-μ-йодид-бис-[бис(ацето-нитрил-κN)меди (I)]» . Acta Crystallographica Раздел E. 71 (Пт 11): м189-90. дои : 10.1107/S2056989015018149 . ПМЦ 4645014 . ПМИД 26594527 .
- ^ Хили ПК, Килдеа Дж.Д., Скелтон Б.В., Уайт А.Х. (1989). «Аддукты с основанием Льюиса соединений металла (I) группы 11. XL. Конформационная систематика [(N-основание) 1 (CuX) 1] ∞ ортогональных полимеров «лестницы» (N-основание = «одномерный ацетонитрил, Бензо-нитриловый лиганд)». Австралийский химический журнал . 42 (1): 79. дои : 10.1071/CH9890079 . ISSN 0004-9425 .
- ^ Архиреева Т.М., Булычев Б.М., Сизов А.И., Соколова Т.А., Бельский В.К., Соловейчик Г.Л. (1990). «Комплексы меди(I) со связью металл-металл (d10–d10). Кристаллическая и молекулярная структура аддуктов тригидрида танталоцена с иодидом меди(I) состава: (η5-C5H5)2TaH[(μ2-H)Cu(μ2) -I)2Cu(μ2-H)]2HTa(η5-C5H5)2, (η5-C5H4But)2TaH(μ2-H)2Cu(μ2-I)2Cu(μ2-H)2HTa(η5-C5H4But)2·CH3CN и {Cu(μ3-I)·P[N(CH3)2]3}4». Неорганика Химика Акта . 169 (1): 109–118. дои : 10.1016/S0020-1693(00)82043-5 .
- ^ Росяк Д., Окуневский А., Хойнацкий Дж. (декабрь 2018 г.). «Ленты йодида меди (I), координированные с производными тиомочевины». Acta Crystallographica Раздел C. 74 (Часть 12): 1650–1655. дои : 10.1107/S2053229618015620 . ПМИД 30516149 . S2CID 54615309 .
- ^ Клапарс А., Бухвальд С.Л. (декабрь 2002 г.). «Медь-катализируемый обмен галогенов в арилгалогенидах: ароматическая реакция Финкельштейна». Журнал Американского химического общества . 124 (50): 14844–5. дои : 10.1021/ja028865v . ПМИД 12475315 . S2CID 11338218 .
- ^ Соногашира, К. (2002), «Развитие катализируемой Pd-Cu кросс-сочетания концевых ацетиленов с sp 2 -галогениды углерода», J. Organomet. Chem. , 653 (1–2): 46–49, doi : 10.1016/s0022-328x(02)01158-0.
- ^ Jump up to: а б Чжан Дж., Ричардсон Х.В. (июнь 2000 г.). «Медные соединения». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. стр. 1–31. дои : 10.1002/14356007.a07_567 . ISBN 3527306730 .
Дальнейшее чтение
[ редактировать ]- Макинтайр Дж (1992). Словарь неорганических соединений . Том. 3. Лондон: Чепмен и Холл. п. 3103.
