Йодид палладия(II)
| |
| Идентификаторы | |
|---|---|
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.029.276 |
| Номер ЕС |
|
ПабХим CID
|
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| я 2 ПД | |
| Молярная масса | 360.229 g/mol |
| Появление | Черные кристаллы |
| Плотность | 6003 г/см 3 |
| Температура плавления | 350 °C (разлагается) |
| Нерастворим в воде | |
| Опасности | |
| СГС Маркировка : [1] | |

| |
| Предупреждение | |
| Х315 , Х319 , Х335 | |
| Родственные соединения | |
Другие анионы
|
Фторид палладия(II) Хлорид палладия(II) Палладий(II) бромид |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Йодид палладия(II) — неорганическое соединение палладия и йода . Он коммерчески доступен, хотя и менее распространен, чем хлорид палладия (II) , который обычно используется в химии палладия. три полиморфа . Известны [2]
Подготовка
[ редактировать ]Йодид палладия(II) можно получить обработкой разбавленного раствора палладия в азотной кислоте йодидом натрия при 80 °C. [2]
Высокотемпературный полиморф иодида α-палладия(II) может быть получен реакцией элементов при температуре выше 600 °C. γ-модификация получается в виде почти аморфного порошка добавлением йодистых солей к водному раствору H 2 PdCl 4 . При нагревании в разбавленном растворе йодистого водорода эта полиморфная модификация переходит в β-фазу примерно при 140 °C. [3]
Реакции и использование
[ редактировать ]Йодид палладия(II) нерастворим в воде. Реагирует с йодидом с образованием PdI 4. 2− анион :
- ПДИ 2 + 2И − → ПДИ 2− 4
Он находит применение в качестве катализатора . [4]
Исторически количество палладия в растворе можно определить гравиметрически путем осаждения в виде йодида палладия (II). [5]
Кристаллография
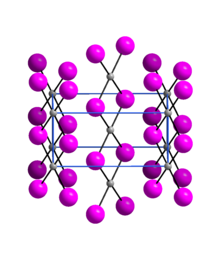
[ редактировать ]Йодид палладия(II) представляет собой практически рентгеноаморфный черный порошок. α-модификация имеет орторомбическую кристаллическую структуру с пространственной группой Pnmn (пр. группа № 58, позиция 5). [6]
Ссылки
[ редактировать ]- ^ «Инвентаризация C&L» . echa.europa.eu . Проверено 13 декабря 2021 г.
- ^ Jump up to: а б Справочник по препаративной неорганической химии. 3 (3-е, исправленное изд.). Штутгарт: Энке. 1981. ISBN 978-3-432-87823-2 .
- ^ Брендель, Кристин; Тиле, Герхард (2001). «Двойные и тройные соединения платиновых металлов палладия и родия с теллуром и галогенами. Получение и структурная характеристика» .
{{cite journal}}: Для цитирования журнала требуется|journal=( помощь ) - ^ Габриэле, Бартоло; Салерно, Джузеппе (2006), «Иодид палладия (II)» , Энциклопедия реагентов для органического синтеза , Американское онкологическое общество, doi : 10.1002/047084289x.rn00658 , ISBN 978-0-470-84289-8 , получено 26 марта 2021 г.
- ^ Бимиш, FE; Дейл, Дж. (1938). «Определение палладия с помощью йодида калия». Аналитическое издание по промышленной и технической химии . 10 (12): 697. дои : 10.1021/ac50128a015 .
- ^ Анс, Жан д'; Лакс, Эллен (1998). Мягкая обложка для химиков и физиков (на немецком языке). Спрингер. ISBN 978-3-540-60035-0 .