Йодид галлия(III)
| |

| |
| Имена | |
|---|---|
| Другие имена
галлиевые триоды
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.033.269 |
| Номер ЕС |
|
ПабХим CID
|
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| Гал 3 | |
| Молярная масса | 450.436 g/mol |
| Появление | светло-желтый порошок |
| Плотность | 4,5 г/см 3 [1] |
| Температура плавления | 212 ° С (414 ° F; 485 К) [1] |
| Точка кипения | 340 ° С (644 ° F; 613 К) [1] |
| разлагается | |
| −149.0·10 −6 см 3 /моль | |
| Термохимия [2] | |
Теплоемкость ( С )
|
100 Дж/(моль К) |
Стандартный моляр
энтропия ( S ⦵ 298 ) |
205,0 Дж/(моль К) |
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
−238,9 кДж/моль |
| Опасности | |
| СГС Маркировка : | |
  
| |
| Опасность | |
| Х314 , Х317 , Х334 , Х335 , Х361 | |
| П280 , П305+П351+П338 , П310 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
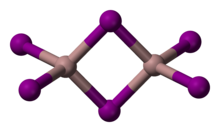
III) — неорганическое соединение формулы Йодид галлия ( Ga I 3 . Желтое гигроскопичное твердое вещество, наиболее распространенный йодид галлия. [3] В методе химического паропереноса выращивания кристаллов арсенида галлия в качестве транспортного агента используется йод. В твердом состоянии он существует в виде димера Ga 2 I 6 . [4] При испарении он образует молекулы GaI 3 симметрии D 3h , где расстояние Ga-I составляет 2,458 Ангстрем . [5]
Трииодид галлия можно восстановить металлическим галлием с получением йодида галлия (I) зеленого цвета . Природа этого вида неясна, но он полезен для получения галлия (I) и соединений галлия (II). [6] [7]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с Хейнс, с. 4,63
- ^ Хейнс, с. 5.20
- ^ Донж, Э. (1963). «Иодид галлия (III)». В Брауэр, Г. (ред.). Справочник по препаративной неорганической химии, 2-е изд . Том. 1. Нью-Йорк, Нью-Йорк: Академик Пресс. п. 846.
- ^ Брюниг, К.; Локмелис, С.; Мильке, Э.; Бинньюис, М. (2006). «Химический транспорт твердых растворов. 27. Образование смешанной фазы и химический транспорт в системе Zn Se /Ga As ». Журнал неорганической и общей химии . 632 (6): 1067–1072. дои : 10.1002/zaac.200600008 .
- ^ Хейнс, с. 9.23
- ^ Бейкер, Роберт Дж.; Джонс, Кэмерон (2005). " "ГаИ": Универсальный реагент для химика-синтетика". Далтон Транс (8): 1341–1348. дои : 10.1039/b501310k . hdl : 2262/69572 . ПМИД 15824768 .
- ^ Грин, Шон П.; Джонс, Кэмерон; Сташ, Андреас; Роуз, Ричард П. (2007). « GaI: новый реагент для хемо- и диастереоселективных реакций образования связей C – C». Нью Дж. Хим . 31 : 127–134. дои : 10.1039/b613669a .
Цитируемые источники
[ редактировать ]- Хейнс, Уильям М., изд. (2016). Справочник CRC по химии и физике (97-е изд.). ЦРК Пресс . ISBN 9781498754293 .
