Йодид хрома(III)
 | |
| Имена | |
|---|---|
| Название ИЮПАК Йодид хрома(III) | |
| Другие имена Трииодид хрома, йодид хрома | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.033.614 |
| Номер ЕС |
|
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| CrIКрИ3 | |
| Молярная масса | 432.7095 g·mol −1 |
| Появление | черный сплошной |
| Плотность | 5,32 г/см 3 [1] |
| Температура плавления | > 600 ° C (1112 ° F; 873 К) |
| Растворимый | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Йодид хрома(III) , также известный как трийодид хрома, представляет собой неорганическое соединение с формулой Кр я 3 . Это черное твердое вещество, которое используется для получения других йодидов хрома. [2]
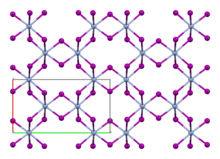
Подобно изоморфному хлориду хрома (III) ( CrCl 3 ), иодид хрома(III) обладает плотнейшей кубической упаковкой в двухслойной кристаллической решетке. В этой структуре хром демонстрирует октаэдрическую координационную геометрию . [3]
Приготовление и свойства
[ редактировать ]Трийодид хрома получают прямой реакцией металлического хрома с избытком йода . Реакцию проводят при 500 °С:
- 2 Кр + 3 И 2 → 2 КрI 3
Для получения образцов высокой чистоты продукт термически разлагают при 700 °C с сублимацией йодида хрома(II) . Затем дииодид повторно иодируют. [2]
Трииодид хрома стабилен при контакте с кислородом и влагой , но при температуре, приближающейся к 200°С, вступает в реакцию с кислородом и выделяет йод. Нравиться CrCl 3 трииодид медленно растворяется в воде из-за кинетической инертности Cr(III). Добавление небольших количеств йодида хрома ускоряет процесс растворения . [2]
Трииодид хрома также можно получить в виде нанопластинок. [ нужны разъяснения ] из алкоксида Cr(OC(CH 3 )(C(CH 3 ) 3 ) 2 ) 3 . [4] [ как? ]
Трийодид хрома был одним из первых материалов, который оказался магнитным двумерным материалом , имеющим большой потенциал для спинтроники . устройств [5]
Ссылки
[ редактировать ]- ^ Перри, Дейл Л. (2011). Справочник неорганических соединений, второе издание . Бока-Ратон, Флорида: CRC Press. п. 123. ИСБН 978-1-43981462-8 . Проверено 10 января 2014 г.
- ^ Jump up to: а б с Грегори, Северо-Запад; Хэнди, LL (1957). «Хрома (III) Йодид». Неорганические синтезы . Том. 5. С. 128–130. дои : 10.1002/9780470132364.ch34 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Грегори, Северо-Запад; Хэнди, LL (1952). «Структурные свойства йодида хрома (III) и некоторых смешанных галогенидов хрома (III)». Дж. Ам. хим. Соц . 74 (4): 891–893. дои : 10.1021/ja01124a009 .
- ^ Де Сиена, Майкл С.; Крейц, Сидни Э.; Риган, Энни; Малиновский, Пол; Цзян, Цянни; Клюхерц, Кайл Т.; Чжу, Гоминь; Линь, Чжун; Де Йорео, Джеймс Дж.; Сюй, Сяодун; Чу, Цзюн-Хо (11 марта 2020 г.). «Двумерные нанопластинки Ван дер Ваальса с устойчивым ферромагнетизмом» . Нано-буквы . 20 (3): 2100–2106. arXiv : 2001.04594 . Бибкод : 2020NanoL..20.2100D . дои : 10.1021/acs.nanolett.0c00102 . ISSN 1530-6984 . ПМИД 32031382 . S2CID 210473134 .
- ^ Хуанг, Б.; и др. (2017). «Слоисто-зависимый ферромагнетизм в кристалле Ван-дер-Ваальса вплоть до предела монослоя». Природа . 546 (7657): 270–273. arXiv : 1703.05892 . Бибкод : 2017Natur.546..270H . дои : 10.1038/nature22391 . ПМИД 28593970 . S2CID 4456526 .