(Бензол)трикарбонил хрома
| |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК (бензол)трикарбонилхром | |||
| Другие имена бензолтрикарбонилхром, трикарбонил (бензол)хрома, бенхротрен, пи-бензолтрикарбонилхром | |||
| Идентификаторы | |||
3D model ( JSmol ) | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.031.939 | ||
| Номер ЕС |
| ||
ПабХим CID | |||
| Характеристики | |||
| Cr(C 6 H 6 )(CO) 3 | |||
| Молярная масса | 214.14 g/mol | ||
| Появление | твердые желтые кристаллы | ||
| Температура плавления | От 163 до 166 ° C (от 325 до 331 ° F; от 436 до 439 К) | ||
| нерастворимый | |||
| Растворимость | ТГФ , эфир , бензол | ||
| Структура | |||
| четырехгранный, «табурет для фортепиано» | |||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности | Вреден при вдыхании, контакте с кожей или проглатывании. | ||
| СГС Маркировка : | |||
 | |||
| Предупреждение | |||
| Х302 , Х312 , Х332 | |||
| P261 , P264 , P270 , P271 , P280 , P301+P312 , P302+P352 , P304+P312 , P304+P340 , P312 , P322 , P330 , P363 , P501 | |||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |||
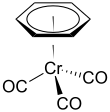
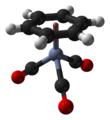
Трикарбонил (бензол)хрома представляет собой металлоорганическое соединение формулы Cr(C 6 H 6 )(CO) 3 . Это желтое кристаллическое твердое соединение растворимо в обычных неполярных органических растворителях. Молекула принимает геометрию, известную как « табурет фортепиано » из-за плоского расположения арильной группы и присутствия трех лигандов CO в качестве «ножек» на оси связи хрома. [1]
Подготовка
[ редактировать ]О (Бензол)трикарбонилхроме впервые сообщили в 1957 году Фишер и Офеле, которые получили это соединение карбонилированием бис ( бензол)хрома . [2] Они получили в основном карбонил хрома (Cr(CO) 6 ) и следы Cr(C 6 H 6 )(CO) 3 . Синтез был оптимизирован за счет реакции Cr(CO) 6 и Cr(C 6 H 6 ) 2 . реакция Cr(CO) 6 и бензола В коммерческих целях используется :
- Cr(CO) 6 + C 6 H 6 → Cr(C 6 H 6 )(CO) 3 + 3 CO
Приложения
[ редактировать ]Комплексы типа (Арен)Cr(CO) 3 хорошо изучены в качестве реагентов в органическом синтезе. [3] Ароматическое кольцо (бензол)трикарбонилхрома значительно более электрофильно , чем сам бензол, что позволяет ему вступать в реакции нуклеофильного присоединения . [4]
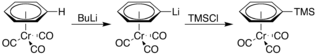
Он также более кислый и подвергается литиированию при обработке н -бутиллитием . Полученное литийорганическое соединение затем можно использовать в качестве нуклеофила в различных реакциях, например, с триметилсилилхлоридом :
(Бензол)трикарбонилхром является полезным гидрирования 1,3 катализатором - диенов . Продукт алкен образуется в результате 1,4-присоединения водорода . Комплекс не гидрирует изолированные двойные связи .
Ссылки
[ редактировать ]- ^ Гилберт Т.М. Бауэр CB, Роджерс Р.Д. (1996). «Структуры (η 6 -диметилацеталь бензола)- и (η 6 -бензолдиэтилацеталь)трикарбонил хрома: структурные доказательства почти электронейтральности диалкилацетального заместителя». Журнал химической кристаллографии . 26 (5): 355. doi : 10.1007/BF01677100 . S2CID 91957129 .
- ^ Фишер, Эрнст Отто; Офеле, Карл. (1957). «Об ароматических комплексах металлов XIII бензол-хром-трикарбонил», Chemical Reports, 90, 2532-5. два : 10.1002/cber.19570901117 .
- ^ Э. Питер Кундиг (2004). «Синтез переходного металла η 6 -Ареновые комплексы». Темы органометной химии . Темы металлоорганической химии. 7 : 3–20. doi : 10.1007/b94489 . ISBN 978-3-540-01604-5 .
- ^ Херндон, Джеймс В.; Лоран, Стефан Э. (2008). «(η 6 -Бензол)трикарбонилхром», в Энциклопедии реагентов для органического синтеза, John Wiley & Sons, Чичестер, 2008 г. дои : 10.1002/047084289X.rb025.pub2 . Дата публикации статьи в Интернете: 15 марта 2009 г.