Триметилгаллий
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК триметилгаллан, триметанидогаллий | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.014.452 |
ПабХим CID | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| Га( СН3 ) 3 | |
| Молярная масса | 114.827 g/mol |
| Появление | бесцветная жидкость |
| Температура плавления | −15 ° C (5 ° F; 258 К) |
| Точка кипения | 55,7 ° C (132,3 ° F; 328,8 К) |
| Реагирует с водой | |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности | Пирофорен (может самовозгораться на воздухе), реагирует с водой с выделением метана. |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
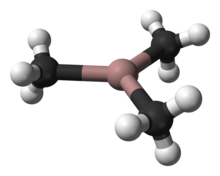
Триметилгаллий , часто сокращенно TMG или TMGa , представляет собой галлийорганическое соединение формулы Ga(CH 3 ) 3 . Это бесцветная пирофорная жидкость. [1] В отличие от триметилалюминия , ТМГ имеет мономерную структуру. [2] При детальном рассмотрении мономерные звенья явно связаны множественными слабыми взаимодействиями Ga-C, что напоминает ситуацию с триметилиндием . [3]
Подготовка
[ редактировать ]Обычно исследуются две формы ТМГ: аддукты оснований Льюиса или сам ТМГ. Все они получаются реакцией трихлорида галлия с различными метилирующими агентами. Когда метилирование проводится йодидом метилмагния в диэтиловом эфире , продукт представляет собой малолетучий аддукт диэтилового эфира. Как отметили первооткрыватели TMG Краус и Тундер в 1933 году, эфирный лиганд не теряется легко, хотя его можно заменить жидким аммиаком. [4] При проведении алкилирования метиллитием в присутствии третичного фосфина получается стабильный на воздухе фосфиновый аддукт:
- GaCl 3 + 3 MeLi + PR 3 → R 3 P−GaMe 3 + 3 LiCl
Нагревание твердого аддукта фосфина в вакууме высвобождает не содержащий оснований ТМГ: [1]
- Р 3 P−GaMe 3 → R 3 P + GaMe 3
Описаны и другие нелетучие основания. [5] Другие метилирующие агенты для синтеза ТМГ включают диметилцинк и триметилалюминий .
Приложения
[ редактировать ]ТМГ является предпочтительным металлоорганическим источником галлия для металлоорганической эпитаксии из паровой фазы (MOVPE) галлийсодержащих соединений полупроводников , таких как GaAs , GaN , GaP , GaSb , InGaAs , InGaN , AlGaInP , InGaP , AlInGaNP и Ga 2 O 3 . [6] Этот материал используется в производстве светодиодного освещения и полупроводников в качестве предшественника металлорганического химического осаждения из паровой фазы.
Ссылки
[ редактировать ]- ^ Перейти обратно: а б Брэдли, округ Колумбия; Чудзинская, ХК; Хардинг, И.С. (1997). «Триметилиндий и триметилгаллий». Неорганические синтезы . Том. 31. С. 67–74. дои : 10.1002/9780470132623.ch8 . ISBN 978-0-470-13262-3 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Митцель, Норберт В.; Люстиг, Кристиан; Бергер, Рафаэль Дж. Ф.; Рунеберг, Нино (2002). «Явления люминесценции и твердотельные структуры триметил- и триэтилгаллия». Angewandte Chemie, международное издание . 41 (14): 2519–2522. doi : 10.1002/1521-3773(20020715)41:14<2519::AID-ANIE2519>3.0.CO;2-2 . ПМИД 12203520 .
- ^ Краус, Калифорния; Тундер, Ф.Е. (1933). «Триметилгаллий, эфир триметилгаллия и аммин триметилгаллия» . ПНАС . 19 (3): 292–8. Бибкод : 1933ПНАС...19..292К . дои : 10.1073/pnas.19.3.292 . ПМК 1085965 . ПМИД 16577510 .
- ^ Фостер, Дуглас Ф.; Коул-Гамильтон, Дэвид Дж. (1997). «Алкилы элементов 12 и 13 групп электронного качества». Неорганические синтезы . Том. 31. с. 29-66. дои : 10.1002/9780470132623.ch7 . ISBN 978-0-471-15288-0 .
- ^ Шенай-Хатхате, ДВ; Гойетт, Р.Дж.; Дикарло, Р.Л. младший; Дриппс, Г. (2004). «Вопросы окружающей среды, здоровья и безопасности для источников, используемых при выращивании сложных полупроводников методом MOVPE». Журнал роста кристаллов . 272 (1–4): 816–21. Бибкод : 2004JCrGr.272..816S . дои : 10.1016/j.jcrysgro.2004.09.007 .