Диалкилбиарилфосфиновые лиганды
Диалкилбиарилфосфиновые лиганды представляют собой фосфиновые лиганды , которые используются в гомогенном катализе . Они оказались полезными в Бухвальда-Хартвига, реакциях аминирования и этерификации а также в реакциях кросс-сочетания Негиши , кросс-сочетания Сузуки-Мияуры и родственных реакциях. [ 1 ] Помимо этих процессов на основе Pd, их использование также распространено на превращения, катализируемые никелем . [ 2 ] золото , [ 3 ] [ 4 ] [ 5 ] серебро , [ 6 ] медь , [ 7 ] родий , [ 8 ] [ 9 ] и рутений , [ 10 ] [ 11 ] среди других переходных металлов. [ 12 ]
История
[ редактировать ]Диалкилбиарилфосфиновые лиганды были впервые описаны Стивеном Л. Бухвальдом в 1998 году для применения в реакциях сочетания, катализируемых палладием, с образованием связей углерод-азот и углерод-углерод. [ 13 ] До их разработки использование фосфиновых лигандов первого или второго поколения для Pd-катализируемого кросс-сочетания с образованием связи CN (например, трис(о-толил)фосфина и BINAP соответственно) требовало жестких условий и масштабов трансформации. было жестко ограничено. обычно проводились с Реакции кросс-сочетания Сузуки-Мияуры и Негиши использованием Pd(PPh 3 ) 4 в качестве катализатора и в основном ограничивались арилбромидами и йодидами при повышенных температурах, в то время как широко доступные арилхлориды были нереакционноспособными. Диалкилбиарилфосфиновые лиганды иногда называют «лигандами Бухвальда». [ 14 ]
Общие характеристики
[ редактировать ]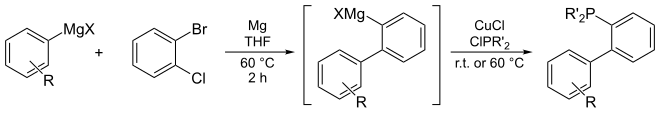
Диалкилбиарилфосфиновые лиганды представляют собой устойчивые на воздухе твердые вещества. Многие из них доступны коммерчески. Их часто можно синтезировать из недорогих исходных материалов. Протоколы с одним горшком проводились на весах >10 кг. [ 15 ] [ 16 ]

Их повышенная каталитическая активность по сравнению с другими лигандами в реакциях сочетания, катализируемых палладием, объясняется их богатым электронами, стерической массой и некоторыми особыми структурными особенностями. В частности, циклогексильную, трет в качестве объемных электронодонорных заместителей для этой цели используют -бутильную и адамантильную группы фосфора. Нижнее кольцо бифенильной системы, орто- по отношению к фосфиногруппе, также является ключевой структурной особенностью. Многочисленные кристаллографические исследования показали, что он ведет себя как гемилабильный лиганд и, как полагают, играет роль в стабилизации высокореактивного, формально 12-электронного L-Pd. 0 промежуточное звено в каталитическом цикле. 2,6-Замещение в нижнем кольце сводит к минимуму разложение катализатора за счет Pd-опосредованной активации CH этих положений. Обширные эксперименты группы Бухвальда показали, что дальнейшие незначительные изменения в структуре этих лигандов могут резко изменить их каталитическую активность в реакциях кросс-сочетания с различными субстратами. Это привело к эволюции множества лигандов, предназначенных для конкретных трансформаций. [ 17 ] Предоставляя средства генерации постулируемого каталитически активного L – Pd 0 видов в мягких условиях (во многих случаях комнатная температура или ниже), разработка нескольких поколений циклопалладированных прекатализаторов, активируемых основаниями, еще больше расширила возможности применения лигандов и упростила их использование. [ 18 ] [ 19 ]
Общие диалкилбиарилфосфиновые лиганды
[ редактировать ]ДэйвФос
[ редактировать ]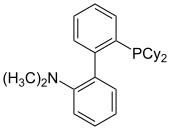
DavePhos, первый зарегистрированный диалкилбиарилфосфиновый лиганд, первоначально использовался в катализируемых Pd реакциях кросс-сочетания Сузуки-Мияуры, а также аминирования Бухвальда-Хартвига . [ 20 ] Комплексы этого лиганда также катализируют широкий спектр реакций, в том числе арилирование кетонов. [ 21 ] и сложные эфиры, [ 22 ] борилирование арилхлоридов, [ 23 ] и арилирование индолов. [ 24 ]
Было синтезировано множество модифицированных версий DavePhos. t- Было показано, что BuDavePhos является еще более реакционноспособным вариантом DavePhos в реакции сочетания Сузуки-Мияуры арилбромидов и хлоридов при комнатной температуре. [ 25 ] Также доступен бифенильный эквивалент (PhDavePhos).
ДжонФос
[ редактировать ]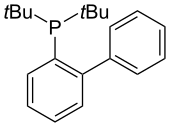
JohnPhos поддерживает катализируемые Pd реакции Сузуки-Мияуры с арилбромидами и хлоридами. [ 26 ] Он толерантен к затрудненным субстратам и работает при комнатной температуре с низкой загрузкой катализатора. Этот лиганд использовался во многих реакциях, включая аминирование ряда арилгалогенидов и трифлатов. [ 27 ] [ 28 ] а также арилирование тиофенов. [ 29 ]
МеФос
[ редактировать ]
Как и DavePhos и JohnPhos, MePhos способен осуществлять катализируемое Pd соединение Сузуки-Мияуры . [ 30 ] Он также может образовывать активный катализатор образования арилкетонов. [ 31 ] Варианты этого лиганда, включая t- BuMePhos, также коммерчески доступны.
Каталитическая система Pd 2 (dba) 3 /MePhos была применена в перекрестных муфтах Suzuki поздней стадии . Эта реакция проводилась в килограммовом масштабе, и никакой специальной обработки для удаления палладия не требовалось, поскольку избыток имидазола, присутствующий на конечной стадии амидного сочетания, координировался с Pd и образовывал удаляемый побочный продукт. [ 32 ]

XPhos
[ редактировать ]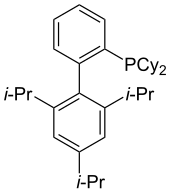
XPhos поддерживает катализаторы на основе Pd для аминирования и амидирования арилсульфонатов и арилгалогенидов. [ 33 ] XPhos также использовался в катализируемом Pd борилировании арил- и гетероарилхлоридов. [ 34 ]
Модифицированные версии XPhos, он более затруднен t- BuXPhos и Me4 t ButylXPhos, использовались при образовании диариловых эфиров. [ 35 ] Включение сульфонатной группы в положение 4 позволяет использовать этот лиганд для реакций Соногаширы в водных двухфазных растворителях. [ 36 ]
Сфос
[ редактировать ]
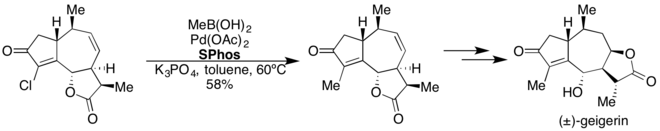
SPhos доказал свою эффективность в реакциях сочетания Сузуки-Мияуры, катализируемых палладием . [ 37 ] Этот лиганд позволяет осуществлять перекрестное соединение гетероарилов, богатых электронами и бедных электронами ариловых и винилбороновых кислот с различными арил- и гетероарилгалогенидами в мягких условиях реакции. SPhos также использовался в катализируемом Pd борилировании арил- и гетероарилхлоридов. [ 38 ]
3-Сульфонатные варианты sSPhos использовались в соединениях Сузуки-Мияура в водных средах. [ 39 ] SPhos использовался в 8-стадийном полном синтезе (±)-гейгерина. [ 40 ]
РуФос
[ редактировать ]
RuPhos оказался эффективным для катализируемого Pd сочетания Негиши цинкорганических соединений с арилгалогенидами. [ 41 ] Эти лиганды толерантны к затрудненным субстратам, а также к широкому спектру функциональных групп. Его комплексы также катализируют трифторметилирование арилхлоридов. [ 42 ] и аминирование арилгалогенидов. [ 43 ]
БреттФос
[ редактировать ]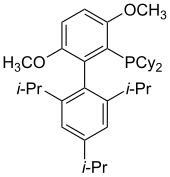
BrettPhos был протестирован на катализируемое Pd аминирование арилмезилатов и арилгалогенидов . [ 44 ] Комплексы Pd-BrettPhos катализируют реакцию сочетания слабых нуклеофилов с арилгалогенидами. Такие катализаторы селективны в отношении моноарилирования первичных аминов. Другие применения BrettPhos в катализе включают трифторметилирование арилхлоридов, [ 45 ] образование арилтрифторметилсульфидов, [ 46 ] и крестовины Suzuki-Miyaura. [ 47 ]
Комплексы Pd- t- BuBrettPhos катализируют превращение арилтрифлатов и арилбромидов в арилфториды. [ 48 ] а также синтез ароматических нитросоединений. [ 49 ] Громоздкий AdBrettPhos можно использовать при амидировании пятичленных гетероциклических галогенидов, содержащих множество гетероатомов (таких как галоимидазолы и галопиразолы). [ 50 ]
CPhos
[ редактировать ]
CPhos использовался в качестве лиганда в катализируемом Pd синтезе производных 3-циклопентилиндола. [ 51 ] дигидробензофураны, [ 52 ] и трансбициклические сульфамиды. [ 53 ] Он также использовался для синтеза палладациклических прекатализаторов для сочетания Негиши вторичных алкилцинковых реагентов с арилгалогенидами. [ 54 ] [ 55 ] [ 56 ]
АльФос
[ редактировать ]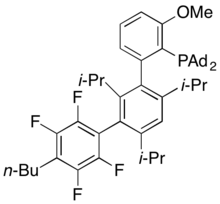
AlPhos позволяет осуществлять мягкое Pd-катализируемое фторирование арил- и гетероарилтрифлатов. [ 57 ] В 2015 году сообщалось, что этот лиганд использовался для реакций кросс-сочетания Бухвальда-Хартвига и для синтеза высокорегиоселективных арилфторидов посредством катализируемого палладием фторирования различных активированных арильных и гетероарилтрифлатов и бромидов. [ 58 ] [ 59 ] Его палладиевые комплексы также использовались для получения арилтиоэфиров путем перекрестного C–S-сочетания тиолов с ароматическими электрофилами. [ 60 ]
Комплекс окислительного присоединения
[ редактировать ]Многие реакции кросс-сочетания, катализируемые Pd, включают окислительное присоединение с образованием производных Pd (II), называемых комплексами окислительного присоединения (ОАК). Полученный L – Pd II (Ar)X OAC является электрофильным, так что он реагирует с нуклеофилом и образует связи C–C и C–гетероатом после восстановительного элиминирования . [ 61 ] Такой Pd II ОАЦ использовались в качестве прекатализаторов. [ 62 ] ОАЦ обладают стабильностью, что позволяет реакциям протекать в мягких условиях. Они были применены к биоконъюгации . [ 63 ] Например, RuPhos и SPhos использовались в качестве лигандов для Pd-опосредованного арилирования цистеина, а использование BrettPhos и t -BuBrettPhos имеет решающее значение для арилирования лизина. [ 64 ] [ 65 ] [ 66 ] [ 67 ]
См. также
[ редактировать ]- Реакция сцепления
- Металлоорганическая химия
- Лиганд
- Биоконъюгация: реакции биоконъюгации, опосредованные переходными металлами
Ссылки
[ редактировать ]- ^ Сарри, Дэвид С.; Бухвальд, Стивен Л. (11 августа 2008 г.). «Биарилфосфановые лиганды в палладий-катализируемом аминировании» . Angewandte Chemie, международное издание . 47 (34): 6338–6361. дои : 10.1002/anie.200800497 . ISSN 1521-3773 . ПМК 3517088 . ПМИД 18663711 .
- ^ Ньюман-Стоунбрейкер, Сэмюэл Х.; Ван, Джейсон Ю.; Джеффри, Филип Д.; Дойл, Эбигейл Г. (октябрь 2022 г.). «Взаимосвязь структура-реактивность фосфинов бухвальдского типа в катализируемых никелем кросс-сочетаниях» (PDF) . Журнал Американского химического общества . 144 (42): 19635–19648. дои : 10.1021/jacs.2c09840 . ПМИД 36250758 . S2CID 252917338 .
- ^ Феррер, Каталина; Эмис, Кателин Х.М.; Эчаваррен, Антонио М. (2 февраля 2007 г.). «Внутри- и межмолекулярные реакции индолов с алкинами, катализируемые золотом» . Химия - Европейский журнал . 13 (5): 1358–1373. дои : 10.1002/chem.200601324 . ПМИД 17206736 .
- ^ Феррер, Каталина; Эчаваррен, Антонио М. (6 февраля 2006 г.). «Катализируемая золотом внутримолекулярная реакция индолов с алкинами: легкое образование восьмичленных колец и неожиданное алленилирование» . Angewandte Chemie (на немецком языке). 118 (7): 1123–1127. дои : 10.1002/ange.200503484 . ISSN 0044-8249 .
- ^ Лопес, Саломе; Эрреро-Гомес, Елена; Перес-Галан, Патрисия; Ньето-Оберхубер, Кристина; Эчаваррен, Антонио М. (11 сентября 2006 г.). «Межмолекулярное циклопропанирование энинов алкенами, катализируемое золотом (I): захват двух разных карбенов золота» . Angewandte Chemie (на немецком языке). 118 (36): 6175–6178. дои : 10.1002/ange.200602448 . ISSN 0044-8249 .
- ^ Порсель, Сусана; Эчаваррен, Антонио М. (6 марта 2007 г.). «Внутримолекулярное карбостаннилирование алкинов, катализируемое соединениями серебра (I)» . Ангеванде Хеми . 119 (15): 2726–2730. дои : 10.1002/ange.200605041 .
- ^ Хайдер, Иоахим; Кунц, Клаус; Шольц, Ульрих (июнь 2004 г.). «Высокоселективное моноарилирование анилина, катализируемое медью» . Расширенный синтез и катализ . 346 (7): 717–722. дои : 10.1002/adsc.200404011 . ISSN 1615-4150 .
- ^ Дхонди, Паван К.; Чисхолм, Джон Д. (1 января 2006 г.). «Родий-катализируемое присоединение алкинов к активированным кетонам и альдегидам» . Органические письма . 8 (1): 67–69. дои : 10.1021/ol0525260 . ISSN 1523-7060 . ПМИД 16381569 .
- ^ Дхонди, Паван К.; Карберри, Патрик; Цой, Лидия Б.; Чисхолм, Джон Д. (1 декабря 2007 г.). «Присоединение алкинов к альдегидам и активированным кетонам, катализируемое родий-фосфиновыми комплексами» . Журнал органической химии . 72 (25): 9590–9596. дои : 10.1021/jo701643h . ISSN 0022-3263 . ПМИД 17999525 .
- ^ Мовассаги, Мохаммед; Хилл, Мэтью Д. (1 ноября 2006 г.). «Одностадийный синтез производных пиримидина» . Журнал Американского химического общества . 128 (44): 14254–14255. дои : 10.1021/ja066405m . ISSN 0002-7863 . ПМИД 17076488 .
- ^ Фаллер, Дж.В.; Д'Аллиесси, Дарлин Г. (1 июня 2003 г.). «Планарная хиральность в связанных комплексах η 6 :η 1 -(фосфинофенилен-P) рутения (II) и их потенциальное использование в качестве асимметричных катализаторов» . Металлоорганические соединения . 22 (13): 2749–2757. дои : 10.1021/om030080q . ISSN 0276-7333 .
- ^ Сарри, Дэвид С.; Бухвальд, Стивен Л. (2011). «Диалкилбиарилфосфины в Pd-катализируемом аминировании: руководство пользователя» . хим. Наука . 2 (1): 27–50. дои : 10.1039/C0SC00331J . ISSN 2041-6539 . ПМК 3306613 . ПМИД 22432049 .
- ^ Олд, Дэвид В.; Вулф, Джон П.; Бухвальд, Стивен Л. (сентябрь 1998 г.). «Высокоактивный катализатор реакций кросс-сочетания, катализируемых палладием: соединения Сузуки при комнатной температуре и аминирование неактивированных арилхлоридов». Журнал Американского химического общества . 120 (37): 9722–9723. дои : 10.1021/ja982250+ .
- ^ «Фосфиновые лиганды Бухвальда» . Сигма-Олдрич . Проверено 8 июня 2023 г.
- ^ Мартин, Рубен; Бухвальд, Стивен Л. (18 ноября 2008 г.). «Катализируемые палладием реакции кросс-сочетания Сузуки-Мияуры с использованием диалкилбиарилфосфиновых лигандов» . Отчеты о химических исследованиях . 41 (11): 1461–1473. дои : 10.1021/ar800036s . ISSN 0001-4842 . ПМЦ 2645945 . ПМИД 18620434 .
- ^ Кэй, Стивен; Фокс, Джозеф М.; Хикс, Фредерик А.; Бухвальд, Стивен Л. (31 декабря 2001 г.). «Использование каталитических количеств CuCl и другие улучшения на пути бензона к фосфиновым лигандам на основе дифенила». Расширенный синтез и катализ . 343 (8): 789–794. doi : 10.1002/1615-4169(20011231)343:8<789::AID-ADSC789>3.0.CO;2-A . ISSN 1615-4169 .
- ^ Мартин, Рубен; Бухвальд, Стивен Л. (18 ноября 2008 г.). «Катализируемые палладием реакции кросс-сочетания Сузуки-Мияуры с использованием диалкилбиарилфосфиновых лигандов» . Отчеты о химических исследованиях . 41 (11): 1461–1473. дои : 10.1021/ar800036s . ISSN 0001-4842 . ПМЦ 2645945 . ПМИД 18620434 .
- ^ Биско, Марк Р.; Форс, Бретт П.; Бухвальд, Стивен Л. (1 мая 2008 г.). «Новый класс легко активируемых палладиевых предкатализаторов для легких реакций кросс-сочетания C-N и низкотемпературного окислительного присоединения арилхлоридов» . Журнал Американского химического общества . 130 (21): 6686–6687. дои : 10.1021/ja801137k . ПМК 2587037 . ПМИД 18447360 .
- ^ Бруно, Северная Каролина; Бухвальд, СЛ (2014). Палладиевые прекатализаторы для реакций кросс-сочетания (PDF) . Стрем Химик.
- ^ Олд, Дэвид В.; Вулф, Джон П.; Бухвальд, Стивен Л. (сентябрь 1998 г.). «Высокоактивный катализатор реакций кросс-сочетания, катализируемых палладием: соединения Сузуки при комнатной температуре и аминирование неактивированных арилхлоридов». Журнал Американского химического общества . 120 (37): 9722–9723. дои : 10.1021/ja982250+ .
- ^ Фокс, Джозеф М.; Хуан, Сяохуа; Шеффи, Андре; Бухвальд, Стивен Л. (1 февраля 2000 г.). «Высокоактивные и селективные катализаторы образования α-арилкетонов». Журнал Американского химического общества . 122 (7): 1360–1370. дои : 10.1021/ja993912d . ISSN 0002-7863 .
- ^ Моради, Вахед А.; Бухвальд, Стивен Л. (2001). «Катализируемое палладием α-арилирование сложных эфиров». Журнал Американского химического общества . 123 (33): 7996–8002. дои : 10.1021/ja010797+ . ISSN 0002-7863 . ПМИД 11506555 .
- ^ Биллингсли, Кельвин Л.; Бардер, Тимоти Э.; Бухвальд, Стивен Л. (9 июля 2007 г.). «Катализируемое палладием борилирование арилхлоридов: область применения, применение и вычислительные исследования». Angewandte Chemie, международное издание . 46 (28): 5359–5363. дои : 10.1002/anie.200701551 . ISSN 1521-3773 . ПМИД 17562550 .
- ^ Олд, Дэвид В.; Харрис, Мишель С.; Бухвальд, Стивен Л. (1 мая 2000 г.). «Эффективное палладий-катализируемое N-арилирование индолов». Органические письма . 2 (10): 1403–1406. дои : 10.1021/ol005728z . ISSN 1523-7060 . ПМИД 10814458 .
- ^ Вулф, Джон П.; Певец, Роберт А.; Ян, Брайант Х.; Бухвальд, Стивен Л. (1 октября 1999 г.). «Высокоактивные палладиевые катализаторы для реакций сочетания Сузуки». Журнал Американского химического общества . 121 (41): 9550–9561. дои : 10.1021/ja992130h . ISSN 0002-7863 .
- ^ Вулф, Джон П.; Певец, Роберт А.; Ян, Брайант Х.; Бухвальд, Стивен Л. (1 октября 1999 г.). «Высокоактивные палладиевые катализаторы для реакций сочетания Сузуки». Журнал Американского химического общества . 121 (41): 9550–9561. дои : 10.1021/ja992130h . ISSN 0002-7863 .
- ^ Вулф, Джон П.; Томори, Хироши; Садиги, Джозеф П.; Инь, Цзинцзюнь; Бухвальд, Стивен Л. (1 февраля 2000 г.). «Простая и эффективная каталитическая система для катализируемого палладием аминирования арилхлоридов, бромидов и трифлатов» (PDF) . Журнал органической химии . 65 (4): 1158–1174. дои : 10.1021/jo991699y . ISSN 0022-3263 . ПМИД 10814067 .
- ^ Сарри, Дэвид С.; Бухвальд, Стивен Л. (11 августа 2008 г.). «Биарилфосфановые лиганды в палладий-катализируемом аминировании» . Angewandte Chemie, международное издание . 47 (34): 6338–6361. дои : 10.1002/anie.200800497 . ISSN 1521-3773 . ПМК 3517088 . ПМИД 18663711 .
- ^ Окадзава, Тору; Сато, Тецуя; Миура, Масахиро; Номура, Масакацу (1 мая 2002 г.). «Множественное арилирование тиофена, катализируемое палладием». Журнал Американского химического общества . 124 (19): 5286–5287. дои : 10.1021/ja0259279 . ISSN 0002-7863 . ПМИД 11996567 .
- ^ Вулф, Джон П.; Певец, Роберт А.; Ян, Брайант Х.; Бухвальд, Стивен Л. (1 октября 1999 г.). «Высокоактивные палладиевые катализаторы для реакций сочетания Сузуки». Журнал Американского химического общества . 121 (41): 9550–9561. дои : 10.1021/ja992130h . ISSN 0002-7863 .
- ^ Фокс, Джозеф М.; Хуан, Сяохуа; Шеффи, Андре; Бухвальд, Стивен Л. (1 февраля 2000 г.). «Высокоактивные и селективные катализаторы образования α-арилкетонов». Журнал Американского химического общества . 122 (7): 1360–1370. дои : 10.1021/ja993912d . ISSN 0002-7863 .
- ^ Тиль, Оливер; Ахматович, Михал; Милберн, Роберт (11 июня 2012 г.). «Исследование и разработка процесса гетероциклических ингибиторов киназы p38 MAP». Синлетт . 23 (11): 1564–1574. дои : 10.1055/s-0031-1290425 . S2CID 196773656 .
- ^ Хуан, Сяохуа; Андерсон, Кевин В.; Зим, Данило; Цзян, Лей; Клапарс, Артис; Бухвальд, Стивен Л. (1 июня 2003 г.). «Расширение процессов образования связей C-N, катализируемых палладием: первое амидирование арилсульфонатов, водное аминирование и комплементарность с реакциями, катализируемыми медью». Журнал Американского химического общества . 125 (22): 6653–6655. дои : 10.1021/ja035483w . ISSN 0002-7863 . ПМИД 12769573 .
- ^ Биллингсли, Кельвин Л.; Бардер, Тимоти Э.; Бухвальд, Стивен Л. (9 июля 2007 г.). «Катализируемое палладием борилирование арилхлоридов: область применения, применение и вычислительные исследования». Angewandte Chemie, международное издание . 46 (28): 5359–5363. дои : 10.1002/anie.200701551 . ISSN 1521-3773 . ПМИД 17562550 .
- ^ Бургос, Карлос Х.; Бардер, Тимоти Э.; Хуан, Сяохуа; Бухвальд, Стивен Л. (26 июня 2006 г.). «Значительно улучшенный метод Pd-катализируемого сочетания фенолов с арилгалогенидами: понимание эффектов лигандов». Angewandte Chemie, международное издание . 45 (26): 4321–4326. дои : 10.1002/anie.200601253 . ISSN 1521-3773 . ПМИД 16733839 .
- ^ Андерсон, Кевин В.; Бухвальд, Стивен Л. (26 сентября 2005 г.). «Общие катализаторы реакций сочетания Сузуки-Мияуры и Соногаширы с арилхлоридами и сочетания сложных комбинаций субстратов в воде». Angewandte Chemie, международное издание . 44 (38): 6173–6177. дои : 10.1002/anie.200502017 . ISSN 1521-3773 . ПМИД 16097019 .
- ^ Уокер, Шон Д.; Бардер, Тимоти Э.; Мартинелли, Джозеф Р.; Бухвальд, Стивен Л. (26 марта 2004 г.). «Рационально разработанный универсальный катализатор для процессов соединения Сузуки-Мияуры». Angewandte Chemie, международное издание . 43 (14): 1871–1876. дои : 10.1002/anie.200353615 . ISSN 1521-3773 . ПМИД 15054800 .
- ^ Биллингсли, Кельвин Л.; Бардер, Тимоти Э.; Бухвальд, Стивен Л. (9 июля 2007 г.). «Катализируемое палладием борилирование арилхлоридов: область применения, применение и вычислительные исследования». Angewandte Chemie, международное издание . 46 (28): 5359–5363. дои : 10.1002/anie.200701551 . ISSN 1521-3773 . ПМИД 17562550 .
- ^ Андерсон, Кевин В.; Бухвальд, Стивен Л. (26 сентября 2005 г.). «Общие катализаторы реакций сочетания Сузуки-Мияуры и Соногаширы с арилхлоридами и сочетания сложных комбинаций субстратов в воде». Angewandte Chemie, международное издание . 44 (38): 6173–6177. дои : 10.1002/anie.200502017 . ISSN 1521-3773 . ПМИД 16097019 .
- ^ Карре, Себастьян; Депре, Жан-Пьер (10 сентября 2007 г.). «Доступ к гуаянолидам: высокоэффективный стереоконтролируемый полный синтез (±)-гейгерина». Angewandte Chemie, международное издание . 46 (36): 6870–6873. дои : 10.1002/anie.200702031 . ISSN 1521-3773 . ПМИД 17676568 .
- ^ Милн, Жаклин Э.; Бухвальд, Стивен Л. (1 октября 2004 г.). «Чрезвычайно активный катализатор реакции кросс-сочетания Негиши». Журнал Американского химического общества . 126 (40): 13028–13032. дои : 10.1021/ja0474493 . ISSN 0002-7863 . ПМИД 15469301 .
- ^ Чо, Ын Джин; Сенекал, Тодд Д.; Кинзел, Том; Чжан, Юн; Уотсон, Дональд А.; Бухвальд, Стивен Л. (25 июня 2010 г.). «Катализируемое палладием трифторметилирование арилхлоридов» . Наука . 328 (5986): 1679–1681. Бибкод : 2010Sci...328.1679C . дои : 10.1126/science.1190524 . ISSN 0036-8075 . ПМК 3005208 . ПМИД 20576888 .
- ^ Чарльз, Марк Д.; Шульц, Филипп; Бухвальд, Стивен Л. (1 сентября 2005 г.). «Эффективное Pd-катализируемое аминирование гетероарилгалогенидов». Органические письма . 7 (18): 3965–3968. дои : 10.1021/ol0514754 . ISSN 1523-7060 . ПМИД 16119943 .
- ^ Форс, Бретт П.; Уотсон, Дональд А.; Биско, Марк Р.; Бухвальд, Стивен Л. (15 октября 2008 г.). «Высокоактивный катализатор реакций аминирования, катализируемых палладием: реакции кросс-сочетания с использованием арилмезилатов и высокоселективное моноарилирование первичных аминов с использованием арилхлоридов» . Журнал Американского химического общества . 130 (41): 13552–13554. дои : 10.1021/ja8055358 . ISSN 0002-7863 . ПМЦ 2748321 . ПМИД 18798626 .
- ^ Чо, Ын Джин; Сенекал, Тодд Д.; Кинзел, Том; Чжан, Юн; Уотсон, Дональд А.; Бухвальд, Стивен Л. (25 июня 2010 г.). «Катализируемое палладием трифторметилирование арилхлоридов» . Наука . 328 (5986): 1679–1681. Бибкод : 2010Sci...328.1679C . дои : 10.1126/science.1190524 . ISSN 0036-8075 . ПМК 3005208 . ПМИД 20576888 .
- ^ Теверовский, Георгий; Сарри, Дэвид С.; Бухвальд, Стивен Л. (1 августа 2011 г.). «Pd-катализируемый синтез соединений Ar-SCF3 в мягких условиях» . Angewandte Chemie, международное издание . 50 (32): 7312–7314. дои : 10.1002/anie.201102543 . ISSN 1521-3773 . ПМЦ 3395331 . ПМИД 21692157 .
- ^ Бхайана, Бриджеш; Форс, Бретт П.; Бухвальд, Стивен Л. (3 сентября 2009 г.). «Универсальная каталитическая система для реакций кросс-сочетания Сузуки-Мияуры C (sp2)-тозилатов и мезилатов» . Органические письма . 11 (17): 3954–3957. дои : 10.1021/ol9015892 . ISSN 1523-7060 . ПМЦ 2759755 . ПМИД 19663467 .
- ^ Уотсон, Дональд А.; Су, Минцзюань; Теверовский, Георгий; Чжан, Юн; Гарсиа-Фортанет, Хорхе; Кинзел, Том; Бухвальд, Стивен Л. (25 сентября 2009 г.). «Образование ArF из LPdAr(F): каталитическое превращение арилтрифлатов в арилфториды» . Наука . 325 (5948): 1661–1664. Бибкод : 2009Sci...325.1661W . дои : 10.1126/science.1178239 . ISSN 0036-8075 . ПМК 3038120 . ПМИД 19679769 .
- ^ Форс, Бретт П.; Бухвальд, Стивен Л. (16 сентября 2009 г.). «Pd-катализируемое превращение арилхлоридов, трифлатов и нонафлатов в нитроароматические соединения» . Журнал Американского химического общества . 131 (36): 12898–12899. дои : 10.1021/ja905768k . ISSN 0002-7863 . ПМЦ 2773681 . ПМИД 19737014 .
- ^ Су, Минцзюань; Бухвальд, Стивен Л. (7 мая 2012 г.). «Объемный биарилфосфиновый лиганд позволяет катализируемое палладием амидирование пятичленных гетероциклов в качестве электрофилов» . Angewandte Chemie, международное издание . 51 (19): 4710–4713. дои : 10.1002/anie.201201244 . ISSN 1521-3773 . ПМЦ 3407381 . ПМИД 22473747 .
- ^ Кирш, Джанель К.; Манске, Дженна Л.; Вулф, Джон П. (2 ноября 2018 г.). «Реакции карбогетероарилирования алкенов, катализируемые Pd, для синтеза производных 3-циклопентилиндола» . Журнал органической химии . 83 (21): 13568–13573. дои : 10.1021/acs.joc.8b02165 . ISSN 0022-3263 . ПМЦ 6375689 . ПМИД 30351050 .
- ^ Хатт, Джонатон Т.; Вулф, Джон П. (20 сентября 2016 г.). «Синтез 2,3-дигидробензофуранов путем катализируемого палладием карбоалкоксилирования 2-аллилфенолов» . Границы органической химии . 3 (10): 1314–1318. дои : 10.1039/C6QO00215C . ISSN 2052-4129 . ПМК 5382964 . ПМИД 28392926 .
- ^ Бабий, Николас Р.; Маккенна, Грейс М.; Форнвальд, Райан М.; Вулф, Джон П. (20 июня 2014 г.). «Стереоконтролируемый синтез бициклических сульфамидов посредством Pd-катализируемых реакций карбоаминирования алкенов. Контроль 1,3-асимметричной индукции путем манипулирования механистическими путями» . Органические письма . 16 (12): 3412–3415. дои : 10.1021/ol5015976 . ISSN 1523-7060 . ПМК 4076003 . ПМИД 24916343 .
- ^ Хан, Чонг; Бухвальд, Стивен Л. (10 июня 2009 г.). «Сочетание Негиши вторичных галогенидов алкилцинка с арилбромидами и хлоридами» . Журнал Американского химического общества . 131 (22): 7532–7533. дои : 10.1021/ja902046m . ISSN 0002-7863 . ПМЦ 2746668 . ПМИД 19441851 .
- ^ Ян, Ян; Нидерманн, Катрин; Хан, Чонг; Бухвальд, Стивен Л. (05 сентября 2014 г.). «Высокоселективное палладий-катализируемое перекрестное сочетание вторичных алкилцинковых реагентов с гетероарилгалогенидами» . Органические письма . 16 (17): 4638–4641. дои : 10.1021/ol502230p . ISSN 1523-7060 . ПМЦ 4156254 . ПМИД 25153332 .
- ^ Чжан, Ху; Бухвальд, Стивен Л. (23 августа 2017 г.). «Катализируемое палладием сочетание Негиши α-CF 3 оксиранилцинката: доступ к хиральным CF 3 -замещенным бензиловым третичным спиртам» . Журнал Американского химического общества . 139 (33): 11590–11594. дои : 10.1021/jacs.7b06630 . ISSN 0002-7863 . ПМИД 28753004 .
- ^ «AlPhos и [(AlPhosPd)2•COD] для Pd-катализируемого фторирования» . Сигма-Олдрич . Проверено 17 августа 2018 г.
- ^ Сатер, Аарон К.; Ли, Хон Гын; Де Ла Роза, Валентина Ю.; Ян, Ян; Мюллер, Питер; Бухвальд, Стивен Л. (21 октября 2015 г.). «Фторированный лиганд обеспечивает региоселективное Pd-катализируемое фторирование арилтрифлатов и бромидов при комнатной температуре» . Журнал Американского химического общества . 137 (41): 13433–13438. дои : 10.1021/jacs.5b09308 . ISSN 0002-7863 . ПМЦ 4721526 . ПМИД 26413908 .
- ^ Сатер, Аарон К.; Ли, Хон Гын; Де Ла Роза, Валентина Ю.; Ян, Ян; Мюллер, Питер; Бухвальд, Стивен Л. (21 октября 2015 г.). «Фторированный лиганд обеспечивает региоселективное Pd-катализируемое фторирование арилтрифлатов и бромидов при комнатной температуре» . Журнал Американского химического общества . 137 (41): 13433–13438. дои : 10.1021/jacs.5b09308 . ISSN 0002-7863 . ПМЦ 4721526 . ПМИД 26413908 .
- ^ Шонесси, Кевин Х. (март 2020 г.). «Разработка палладиевых прекатализаторов, которые эффективно генерируют активные частицы LPd (0)» . Израильский химический журнал . 60 (3–4): 180–194. дои : 10.1002/ijch.201900067 . ISSN 0021-2148 . S2CID 202882630 .
- ^ Йоханссон Зеечерн, Карин СиСи; Китчинг, Мэтью О.; Колакот, Томас Дж.; Снекус, Виктор (21 мая 2012 г.). «Кросс-сочетание, катализируемое палладием: исторический контекстуальный взгляд на Нобелевскую премию 2010 года» . Angewandte Chemie, международное издание . 51 (21): 5062–5085. дои : 10.1002/anie.201107017 . ПМИД 22573393 .
- ^ Инголья, Брайан Т.; Бухвальд, Стивен Л. (2 июня 2017 г.). «Комплексы окислительного присоединения как предкатализаторы реакций кросс-сочетания, требующих чрезвычайно объемных биарилфосфиновых лигандов» . Органические письма . 19 (11): 2853–2856. doi : 10.1021/acs.orglett.7b01082 . ISSN 1523-7060 . ПМК 5580394 . ПМИД 28498667 .
- ^ Юлинг, Мика Р.; Кинг, Райан П.; Крска, Шейн В.; Чернак, Тим; Бухвальд, Стивен Л. (25 января 2019 г.). «Фармацевтическая диверсификация за счет комплексов окислительного присоединения палладия» . Наука . 363 (6425): 405–408. doi : 10.1126/science.aac6153 . ISSN 0036-8075 . ПМИД 30679373 . S2CID 59248487 .
- ^ Виноградова Екатерина Владимировна; Чжан, Чи; Спокойный, Александр М.; Пентелюта, Брэдли Л.; Бухвальд, Стивен Л. (октябрь 2015 г.). «Металлоорганические палладиевые реагенты для биоконъюгации цистеина» . Природа . 526 (7575): 687–691. дои : 10.1038/nature15739 . ISSN 0028-0836 . ПМЦ 4809359 . ПМИД 26511579 .
- ^ Рохас, Энтони Дж.; Пентелюта, Брэдли Л.; Бухвальд, Стивен Л. (18 августа 2017 г.). «Водорастворимые палладиевые реагенты для S-арилирования цистеина в водных условиях» . Органические письма . 19 (16): 4263–4266. doi : 10.1021/acs.orglett.7b01911 . ISSN 1523-7060 . ПМЦ 5818991 . ПМИД 28777001 .
- ^ Джбара, Мухаммед; Родригес, Джейкоб; Дханджи, Химал Х.; Лоас, Андрей; Бухвальд, Стивен Л.; Пентелюта, Брэдли Л. (17 мая 2021 г.). «Биоконъюгация олигонуклеотидов с бифункциональными палладиевыми реагентами» . Angewandte Chemie, международное издание . 60 (21): 12109–12115. дои : 10.1002/anie.202103180 . ISSN 1433-7851 . ПМК 8143041 . ПМИД 33730425 .
- ^ Ли, Хон Гын; Лотретт, Гийом; Пентелюта, Брэдли Л.; Бухвальд, Стивен Л. (13 марта 2017 г.). «Палладий-опосредованное арилирование лизина в незащищенных пептидах» . Angewandte Chemie, международное издание . 56 (12): 3177–3181. дои : 10.1002/anie.201611202 . hdl : 1721.1/115190 . ПМК 5741856 . ПМИД 28206688 .
