Сузуки реакция
| Сузуки реакция | |
|---|---|
| Назван в честь | Акира Сузуки |
| Тип реакции | Реакция связи |
| Идентификаторы | |
| Органическая химическая портал | Suzuki-Coupling |
| RSC Ontology Id | RXNO: 0000140 |
Реакция Suzuki или Suzuki-связь представляют собой органическую реакцию , которая использует палладия катализатор комплекса для перекрестной колпаки бориновой кислоты на органохалид . [ 1 ] [ 2 ] [ 3 ] Впервые он был опубликован в 1979 году Акирой Сузуки , и он разделил Нобелевскую премию 2010 года по химии с Ричардом Ф. Хеком и Эй-Ичи Негиши за их вклад в открытие и развитие катализа благородных металлов в органическом синтезе . [ 4 ] Эта реакция иногда телескопируется со связанным борилированием Мияуры ; Комбинация - это реакция Сузуки -Мияура . Он широко используется для синтеза полиофинов и , стихов замещенных бифенилов .
Общая схема реакции Suzuki показана ниже, где одноуглеродная отдельная связь образуется путем соединения галогенида (R 1 -X) с видом органоборона (r 2 -By 2 ) Использование палладийского катализатора и основания . Виды Organoboron , что позволяет быстро обычно синтезируются гидроборированием или карбоборией генерировать молекулярную сложность.

Было опубликовано несколько обзоров с описанием достижений и разработки реакции Сузуки. [ 5 ] [ 6 ] [ 7 ]
Механизм реакции
[ редактировать ]Механизм реакции Сузуки лучше всего рассматривать с точки зрения катализатора палладия. Каталитический цикл инициируется образованием активного PD 0 каталитические виды, а . Это участвует в окислительном добавлении палладия к галогенидскому реагенту 1 образуя органопалладий промежуточный B. , Реакция ( метатезис ) с основанием дает промежуточный C , который посредством трансмитации [ 8 ] С комплексом борной D (продуцируемый реакцией реагента 2 с основанием 2) образует переходные органопалладия виды e . Стадия восстановительного устранения приводит к образованию желаемого продукта 3 и восстанавливает оригинальный палладийский катализатор A, который завершает каталитический цикл .

Соединение Suzuki происходит в присутствии основания, и в течение долгого времени роль основания не была до конца изучена. Считалось, что основание образует пробную борату (R 3 B-или), в случае реакции пробного килборина (BR 3 ) и алкоксида ( − ИЛИ); Этот вид можно считать более нуклеофильным , а затем более реактивным в отношении комплекса палладия, присутствующего на стадии трансмиссии. [ 9 ] [ 10 ] [ 11 ] DUC и коллеги исследовали роль основания в механизме реакции для связи Suzuki, и они обнаружили, что у основания есть три роли: образование комплекса Palladium [arpd (OR) L 2 ], образование пробного бората и ускорение Редактивное устранение стадирует реакцией алкоксида с комплексом палладия. [ 9 ]
Окислительное дополнение
[ редактировать ]В большинстве случаев окислительное добавление является стадией определения скорости каталитического цикла. [ 12 ] На этом этапе катализатор палладий окисляется от палладия (0) до палладия (II). Каталитически активные виды палладия A связаны с арилгалогенидным субстратом 1, получить органопалладийный комплекс B. чтобы Как видно на диаграмме ниже, этап окислительного добавления разбивает углеродную связь , где палладий теперь связан как с галогеном (x), так и R 1 группа.

Окислительное дополнение происходит с сохранением стереохимии с виниловыми галогенидами , одновременно давая инверсию стереохимии с аллиловыми и бензиличными галогниками. [ 13 ] Окислительное добавление первоначально образует цис -палладий, который быстро изомеризуется в транс-комплекс. [ 14 ]

Соединение Suzuki происходит с сохранением конфигурации на двойных связях как для реагента органоборона, так и для галогенида. [ 15 ] менее, конфигурация этой двойной связи, цис или транс определяется цис -транс Тем не -изомеризацией комплекса палладия на стадии окислительного добавления, где транс -палладийный комплекс является преобладающей формой. Когда органоборон прикреплен к двойной связи, и он связан с алкенильным галогеной, продукт представляет собой диен, как показано ниже.

Передача
[ редактировать ]Трансмитация - это органометаллическая реакция, в которой лиганды переносятся из одного вида в другой. В случае сочетания Suzuki лиганды переносятся из вида органоборона D в комплекс Palladium (II) C , где основание, которое добавлялось на предыдущем этапе, обменивается с заместителем R 2 на видах органоборона, чтобы получить новый палладий (Ii) комплекс e . Точный механизм передачи для связи Сузуки еще предстоит обнаружить. Соединения органоборона не подвергаются трансмитации в отсутствие основания, и поэтому широко распространено мнение, что роль основания заключается в активации соединения органоборона, а также облегчить образование R 1 -Пд LL - Т BU Intermediate ( c ) из продукта окислительного добавления r 1 -Пд LL -X ( b ). [ 12 ]

Редактивное устранение
[ редактировать ]Последним этапом является этап восстановительного устранения, на котором комплекс палладия (II) ( E ) устраняет продукт ( 3 ) и восстанавливает катализатор палладий (0) ( A ). Используя маркировку дейтерия , Ridgway et al. показали восстановительное устранение с сохранением стереохимии. [ 16 ]

Лиганд играет важную роль в реакции Сузуки. Как правило, фосфиновый лиганд используется в реакции Suzuki. Фосфиновый лиганд увеличивает плотность электронов в металлическом центре комплекса и, следовательно, помогает на стадии окислительного добавления. Кроме того, объемность замещения фосфинового лиганда помогает на этапе восстановительного устранения. Тем не менее, N -гетероциклические карбеновые лиганды недавно использовались в этой перекрестной связи из -за нестабильности фосфинового лиганда в условиях реакции Suzuki. [ 17 ] N -гетероциклические карбены более богаты электронами и громоздкой, чем фосфиновый лиганд. Следовательно, как стерические, так и электронные факторы n -гетероциклического карбенового лиганда помогают стабилизировать активный катализатор PD (0). [ 18 ]
Преимущества
[ редактировать ]Преимущества связывания Suzuki по сравнению с другими подобными реакциями включают доступность общих борных кислот, легкие условия реакции и ее менее токсичную природу. Бороновые кислоты менее токсичны и безопаснее для окружающей среды, чем организма и соединения организма . Легко удалить неорганические побочные продукты из реакционной смеси. Кроме того, эта реакция предпочтительнее, потому что она использует относительно дешевые и легко подготовленные реагенты. Возможность использовать воду в качестве растворителя [ 19 ] делает эту реакцию более экономичной, экологически чистым и практичным в использовании с различными водорастворимыми реагентами. Большое разнообразие реагентов может быть использовано для сочетания Suzuki, например, арил или виниловой бориновой кислоты и арил или виниловые галогениды. Работа также расширила масштаб реакции на включение алкил -бромидов. [ 20 ] В дополнение к тому, что множество различных галогенидов возможны для реакции сочетания Suzuki, реакция также работает с псевдохалидами , такими как трифляты (OTF), в качестве замены для галогенидов . Относительная реактивность для партнера по связке с галогенидом или псевдогалидом: r 2 -i> r 2 -otf> r 2 –br >> r 2 –cl. Бороновые сложные эфиры и органотрифторобораторные соли могут использоваться вместо борных кислот. Катализатор также может быть катализатором на основе наноматериалов на наноматериалах . [ 21 ] о новом органофосфинном лиганде ( SPHOS ), нагрузки на катализатор до 0,001 моль. Сообщалось [ 22 ] Эти достижения и общая гибкость процесса сделали общепринятую связь Suzuki для химического синтеза.
Приложения
[ редактировать ]Промышленные применения
[ редактировать ]Реакция связывания Suzuki является масштабируемой и экономически эффективной для использования в синтезе промежуточных соединений для фармацевтических препаратов или тонких химических веществ . [ 23 ] Реакция Suzuki когда -то была ограничена высоким уровнем катализатора и ограниченной доступностью борных кислот . Также были обнаружены замены для галогенидов, что увеличило количество партнеров по связям и для галогенидов или псевдогалида. Масштабированные реакции были проведены в синтезе ряда важных биологических соединений, таких как CI-1034, которые использовали партнеров по связке трифлат и бориновой кислоты , которые работали по масштабе 80 килограммов с выходом 95%. [ 24 ]
Другим примером является связь 3-пиридилборанового и 1-бром-3- (метилсульфонил) бензола, который образовал промежуточный соединение, которое использовалось в синтезе потенциального агента центральной нервной системы. Реакция связи с образованием промежуточного соединения продуцировала 278 килограммов с выходом 92,5%. [ 15 ] [ 23 ]
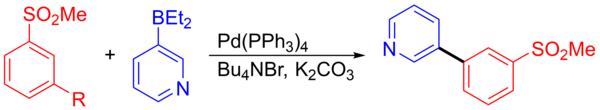
Значительные усилия были приложены в разработку гетерогенных катализаторов для реакции Suzuki CC, мотивированной повышением производительности в промышленном процессе (устранение отделения катализатора от субстрата), а недавно показано, что однородный катализатор одного атома PD опережает гетерогенный катализатор PD. Промышленность по умолчанию гомогенный PD (PPH 3 ) 4 Катализатор. [ 25 ]
Синтетические приложения
[ редактировать ]Соединение Suzuki часто используется в синтезах сложных соединений. [ 26 ] [ 27 ] Связание Suzuki использовалась на цитронеллальной производной для синтеза капарратриена , натурального продукта, который очень активен против лейкемии: [ 28 ]

Вариации
[ редактировать ]Металлический катализатор
[ редактировать ]Было разработано различное каталитическое использование металлов, отличных от палладия (особенно никеля). [ 29 ] Первая никелевая катализируемая реакция перекрестной связки была сообщена Percec и коллегами в 1995 году с использованием арил мезилатов и бориновых кислот. [ 30 ] более высокое количество никелевого катализатора Несмотря на то, что для реакции было необходимо , около 5 мол. %, Никель не такой дорогой или драгоценный металл, как палладий . Никель катализировала реакция связи Suzuki также позволила ряд соединений, которые не работали или работали хуже для палладийской катализированной системы, чем система, катализируемая никелем. [ 29 ] Использование никелевых катализаторов позволило для электрофилов, которые оказались сложными для первоначальной связи Suzuki с использованием палладия, включая субстраты, такие как фенолы, ариловые эфиры, сложные эфиры, фосфаты и фториды. [ 29 ]

Исследование никелевого катализируемого перекрестного связки продолжилось и увеличило масштаб реакции после того, как эти первые примеры были показаны, и исследовательский интерес вырос. Мияура и Инада сообщили в 2000 году, что более дешевый никелевый катализатор может быть использован для перекрестной связи с использованием трифенилфосфина (PPH 3 ) вместо более дорогих лигандов, которые ранее использовались. [ 31 ] Тем не менее, катализируемая никелевая перекрестная связь по-прежнему требовала высоких нагрузок катализатора (3-10%), требуется избыточный лиганд (1-5 эквивалентов) и оставался чувствительным к воздуху и влаге. [ 29 ] Достижения Han и коллег попытались решить эту проблему, разработав метод с использованием низкого количества никелевого катализатора (<1 моль%) и никаких дополнительных эквивалентов лиганда. [ 32 ]
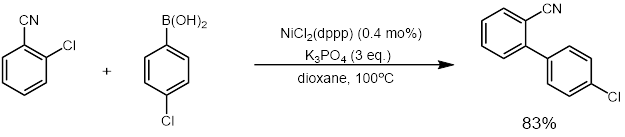
В 2011 году WU также сообщили, что в 2011 году можно было использовать высокоактивный никелевый катализатор для перекрестного связывания арилхлоридов, который требовал только 0,01-0,1 моль% никелевого катализатора. Они также показали, что катализатор может быть переработан до шести раз, практически без потерь в каталитической активности. [ 33 ] Катализатор был пригоден для переработки, потому что это был катализатор наночастиц фосфина (G 3 Denp-Ni), который был сделан из дендримеров .

Преимущества и недостатки применяются как к реакциям связывания Suzuki, катализируемых палладием, так и на никель. Помимо системы катализатора PD и NI, дешевые и нетоксичные металлоистения, такие как железо и медь [ 34 ] были использованы в реакции связи Сузуки. Исследовательская группа из Бедфорда [ 35 ] и исследовательская группа Накамура [ 36 ] широко работали над разработкой методологии реакции сочетания Suzuki, катализируемой железом. Рутениум является еще одним источником металлов, который использовался в реакции сочетания Сузуки. [ 37 ]
Амидная связь
[ редактировать ]Катализ никеля может построить СС связи из амидов. Несмотря на инертную природу амидов в качестве синлонов, следующая методология может быть использована для подготовки связей с CC. Процедура связи мягкая и толерантная для множества функциональных групп, в том числе: амины, кетоны, гетероциклы, группы с кислыми протонами. Этот метод также может быть использован для приготовления биологически активных молекул и объединения гетероциклов контролируемыми способами посредством проницательных последовательных перекрестных связей. Общий обзор схемы реакции приведен ниже. [ 38 ]

Синтез тубулинового соединения ( антипролиферативный агент) проводили с использованием триметокси бензамида и партнера по связке атоборона индолила пинакола в граммовой масштабе. [ 38 ]

Органобораны
[ редактировать ]Арилбононические кислоты сравнительно дешевле, чем другие органобораны, и широкий спектр ариловых кислот , коммерчески доступны. Следовательно, он широко использовался в реакции Suzuki в качестве партнера по организму. Соли арилтрифлуоробората - это еще один класс органоборанов, которые часто используются, потому что они менее подвержены протодеборонации по сравнению с арил бориновыми кислотами . Их легко синтезировать и могут быть легко очищены. [ 39 ] Соли арилтрифлуоробората могут образовываться из бориновых кислот при обработке фторидом водорода калия , которые затем можно использовать в реакции связывания Сузуки. [ 40 ]

Вариации растворителя
[ редактировать ]Реакция сцепления Suzuki отличается от других реакций связи тем, что ее можно работать в двухфазной органической воде, [ 41 ] только вода, [ 19 ] или нет растворителя. [ 42 ] Это увеличило объем реакций связи, поскольку различные водорастворимые основания, катализаторные системы и реагенты могут использоваться без беспокойства по поводу их растворимости в органическом растворителе. Использование воды в качестве системы растворителя также привлекательно из -за экономических и безопасности. Часто используются в системах растворителя для сцепления Suzuki, являются толуол , [ 43 ] Тхар , [ 44 ] диоксан , [ 44 ] и DMF . [ 45 ] Наиболее часто используемыми основаниями являются K 2 CO 3 , [ 41 ] Ко Т ку , [ 46 ] CS 2 CO 3 , [ 47 ] K 3 PO 4 , [ 48 ] Нао , [ 49 ] и сеть 3 . [ 50 ]
Смотрите также
[ редактировать ]- Чан-лам сцепление
- Черт возьми
- Хияма муфта
- Кумуппин
- Негиши сцепление
- Отлипание реакции
- Соногашира Связь
- Стилл Реакция
- Список органических реакций
Ссылки
[ редактировать ]- ^ Мияура, Норо; Ямада, Кинджи; Suzuki, Akira (1979). «Новая стереоспецифическая перекрестная связка с помощью катализируемой палладием реакции 1-алкенилборанов с 1-алкениловыми или 1-алкинильскими галогенидами» . Тетраэдр буквы . 20 (36): 3437–3440. doi : 10.1016/s0040-4039 (01) 95429-2 . HDL : 2115/44006 .
- ^ Мияура, Норо; Suzuki, Akira (1979). «Стереоселективный синтез арилированных (E) -алкен с реакцией ALK-1-проенилборанов с арилгалогендами в присутствии палладий-катализатора». Химический Коммуникация (19): 866–867. doi : 10.1039/c39790000866 .
- ^ Мияура, Норо ; Suzuki, Akira (1995). «Катализируемые палладием реакции перекрестного связки соединений органоборона». Химические обзоры . 95 (7): 2457–2483. Citeseerx 10.1.1.735.7660 . doi : 10.1021/cr00039a007 . S2CID 53050782 .
- ^ Nobelprize.org. «Нобелевская премия по химии 2010» . Нобелевский фонд . Получено 2013-10-25 .
- ^ Suzuki, Akira (1991). «Синтетические исследования посредством реакции перекрестной связки производных органоборона с органическими галогенидами» . Чистое приложение. Химический 63 (3): 419–422. doi : 10.1351/pac199163030419 .
- ^ Мияура, Норо; Suzuki, Akira (1979). «Катализируемые палладием реакции перекрестного связки соединений органоборона» . Химические обзоры . 95 (7): 2457–2483. Citeseerx 10.1.1.735.7660 . doi : 10.1021/cr00039a007 . S2CID 53050782 . (Обзор)
- ^ Suzuki, Akira (1999). «Недавние достижения в реакциях перекрестной связи производных органоборонов с органическими электрофилами, 1995–1998» . Журнал органометаллической химии . 576 (1–2): 147–168. doi : 10.1016/s0022-328x (98) 01055-9 .
- ^ Матос, К.; Содерквист, JA (1998). «Алкилборины в связи Сузуки -Мияура: стереохимические и механистические исследования». J. Org. Химический 63 (3): 461–470. doi : 10.1021/jo971681s . PMID 11672034 .
- ^ Подпрыгнуть до: а беременный Аматоре, Кристиан; Джутанд, Энни; Le Duc, Гаэтан (18 февраля 2011 г.). «Кинетические данные для трансмитации/восстановительного элиминации в реакциях Suzuki-Miyaura, катализируемых палладием: неожиданная тройная роль гидроксидных ионов, используемых в качестве основания». Химия: европейский журнал . 17 (8): 2492–2503. doi : 10.1002/chem.201001911 . PMID 21319240 .
- ^ Смит, Джордж Б.; Dezeny, George C.; Хьюз, Дэвид Л.; Король, Энтони О.; Верховен, Томас Р. (1 декабря 1994 г.). «Механистические исследования реакции перекрестного связывания Suzuki». Журнал органической химии . 59 (26): 8151–8156. doi : 10.1021/jo00105a036 .
- ^ Матос, Карл; Содерквист, Джон А. (1 февраля 1998 г.). «Алкилборины в связи Сузуки -Мияура: стереохимические и механистические исследования». Журнал органической химии . 63 (3): 461–470. doi : 10.1021/jo971681s . PMID 11672034 .
- ^ Подпрыгнуть до: а беременный Курти, Ласло (2005). Стратегическое применение названных реакций в органическом синтезе . Elsevier Academic Press. ISBN 978-0124297852 .
- ^ Стил, Джон К.; Лау, Крейслер Си (1977). «Механизмы окислительного добавления органических галогенидов к комплексам переходных металлов группы 8». Счета химических исследований . 10 (12): 434–442. doi : 10.1021/ar50120a002 .
- ^ Касадо, Артуро Л.; Espinet, Pablo (1998). «В конфигурации, возникающей в результате окислительного добавления RX в PD (PPH3) 4 и механизм цис-транзисомеризации комплексов \ pdrx (PPH3) 2] (r = aryl, x = halidide) †». Органометаллики . 17 (5): 954–959. doi : 10.1021/om9709502 .
- ^ Подпрыгнуть до: а беременный Усовершенствованная органическая химия . Спрингер. 2007. С. 739–747 .
- ^ Риджуэй, Брайан Х.; Woerpel, Ka (1998). «Трансмитация алкилборинов в палладий в реакции связи Сузуки продолжается с удержанием стереохимии». Журнал органической химии . 63 (3): 458–460. doi : 10.1021/jo970803d . PMID 11672033 .
- ^ «Наука синтеза: лучшие методы. Лучшие результаты - химия Thieme» . Science-of-Synthesis.theme.com . Получено 2021-04-14 .
- ^ Хопкинсон, Мэтью Н.; Рихтер, Кристиан; ПЕРЕДЕЛЕР, Майкл; Глориус, Фрэнк (июнь 2014 г.). «Обзор N-гетероциклических карбенов» . Природа . 510 (7506): 485–496. Bibcode : 2014natur.510..485h . doi : 10.1038/nature13384 . ISSN 1476-4687 . PMID 24965649 . S2CID 672379 .
- ^ Подпрыгнуть до: а беременный Casalnuovo, Albert L.; Калабрезе (1990). «Катализируемые палладием алкилирования в водной среде». J. Am. Химический Соц 112 (11): 4324–4330. doi : 10.1021/ja00167a032 .
- ^ Кирххофф, январь Х.; Нетертон, Мэтью Р.; Hills, Ivory D.; Фу, Грегори С. (2002). «Бороновые кислоты: новые партнеры по связям в сузуки-реакциях в комнатной температуре алкил бромидов. Кристаллографическая характеристика аддукта окислительного изменения, генерируемого в удивительно мягких условиях». Журнал Американского химического общества . 124 (46): 13662–3. doi : 10.1021/ja0283899 . PMID 12431081 .
- ^ Ohtaka, Atsushi (2013). «Нанометальные катализаторы, поддерживаемые полимером, нанометальные катализаторы в воде». Химическая запись . 13 (3): 274–285. doi : 10.1002/tcr.201300001 . PMID 23568378 .
- ^ Martin, R.; Бучвальд, SL (2008). «Катализируемые палладием Suzuki-Miyaura поперечные реакции с использованием диалкилбиарий фосфиновых лигандов» . Счета химических исследований . 41 (11): 1461–1473. doi : 10.1021/ar800036s . PMC 2645945 . PMID 18620434 .
- ^ Подпрыгнуть до: а беременный Рухи, А. Морин (6 сентября 2004 г.). «Прекрасные химические вещества». C & en .
- ^ Джекс, Томас Э.; Белмонт, Даниэль Т.; Бриггс, Кристофер А.; Хорн, Николь М.; Кантер, Джеральд Д.; Каррик, Грег Л.; Крик, Джеймс Дж.; МакКейб, Ричард Дж.; Мустакис; Нэннинге, Томас Н. (1 марта 2004 г.). «Разработка масштабируемого процесса для CI-1034, антагониста эндотелина». Органические процессы исследования и разработки . 8 (2): 201–212. doi : 10.1021/op034104g .
- ^ Чен, Зупенг; Воробева, Евгения; Митчелл, Шарон; Фако, Эдвин; Ортуньо, Мануэль А.; Лопес, Нурия ; Коллинз, Шон М.; Мидгли, Пол А.; Ричард, Сильвия; Виле, Джанвито; Перес-Рамирес, Хавьер (2018). «Гетереостый однополостный палладий-катализатор палладий-палладий, фальшивая гомогенные системы для муфты Suzuki» (PDF ) Природная нанотехнология 13 (8): 702–7 Bibda : 2018natna..13..702c Doi : 10.1038/s41565-018-0167-2 . HDL : 2072/3 PMID 29941887 S2CID 49415437
- ^ Балог, Аарон; Мэн, Донгфанг; Каменека, Тед; Бертанато, Питер; Су, Дай-Ши; Соренсен, Эрик Дж.; Данишефский, Сэмюэль Дж. (1996). «Полный синтез (-)-эпотилон А». Angewandte Chemie International Edition на английском языке . 35 (2324): 2801–2803. doi : 10.1002/anie.199628011 .
- ^ Лю, Джуния; Лотеста, Стивен Д.; Соренсен, Эрик Дж. (2011). «Краткий синтез молекулярной структуры плевромутилина» . Химическая связь . 47 (5): 1500–2. doi : 10.1039/c0cc04077k . PMC 3156455 . PMID 21079876 .
- ^ Vyvyan, Jr; Петерсон, Эмили А.; Стефан, Мари Л. (1999). «Высокий общий синтез (+/-)-капраратриена». Тетраэдр буквы . 40 (27): 4947–4949. doi : 10.1016/s0040-4039 (99) 00865-5 .
- ^ Подпрыгнуть до: а беременный в дюймовый Хан, Фу-Ше (1 января 2013 г.). «Катализируемые переходными металлами Suzuki-Miyaura реакции перекрестного связки: замечательный прогресс от палладий к никелевым катализаторам». Обзоры химического общества . 42 (12): 5270–98. doi : 10.1039/c3cs35521g . PMID 23460083 .
- ^ Персек, Вирджил; Bae, Jin-Young; Хилл, Дейл (1995). «Арил мезилаты в металлических катализируемых гомоко-образовательных реакциях и перекрестной связке. 2. Катализируемый никель-катализированным типом Suzuk Журнал органической химии . 60 (4): 1060–1065. doi : 10.1021/jo00109a044 .
- ^ Инада, Каору; Норио Мияура (2000). «Синтез биарилов посредством реакции перекрестной связки арилбороновых кислот с арилхлоридами, катализируемыми NICL2/трифенилфосфинными комплексами». Тетраэдр . 56 (44): 8657–8660. doi : 10.1016/s0040-4020 (00) 00814-0 .
- ^ Чжао, Ю-Лонг; Ли, ты; Ли, Шуи-Мин; Чжоу, И-Гуо; Солнце, фэн-Йи; Гао, Лиан-Хун; Хан, Фу-Ше (1 июня 2011 г.). «Высоко практичный и надежный никелевый катализатор для сузуки-мияуры с помощью арилгалогенидов». Расширенный синтез и катализ . 353 (9): 1543–1550. doi : 10.1002/adsc.201100101 .
- ^ Ву, Лей; Лин, Цзе; Wu, Zong-Quan (1 июня 2011 г.). «Высоко активный и переработанный катализатор: стабилизированные фосфиновыми дендримерами наночастицы никеля для реакции сцепления Suzuki». Расширенный синтез и катализ . 353 (9): 1452–1456. doi : 10.1002/adsc.201100134 .
- ^ Ян, CT; Чжан, Чжэнь-Ки; Лю, Ю-Чен; Лю, Лей (2011). «Катализируемая медь реакция перекрестной связки соединений органоборона с первичными алкилгалогенками и псевдохалидами». Ангев. Химический Инт. Редакция 50 (17): 3904–3907. doi : 10.1002/anie.201008007 . PMID 21455914 .
- ^ Бредфорд, РБ; Холл, Марк А.; Ходжес, Джордж Р.; Хуве, Майкл; Уилкинсон, Марк С. (2009). «Простые смешанные катализаторы Fe-ZN для сузуки-муфт тетраарилборбов с бензилгалогенками и 2-халопиридинами». Химический Общение (42): 6430–6432. doi : 10.1039/b915945b . PMID 19841799 . S2CID 40428708 .
- ^ Накан, м, м; Ха -ха, место, Токе; Камаль собрался вместе, Килдия; Зун, Тэм такой же; Сикейк, Очами; Mahalai, Mahai, Marush, (2012). "I-D, снятый в 2-х кодистах локков. Я прав. химин Его. Редакция 5125 ) 83: 84–8 Rel : 10.102/2, 70979 . PMIDD 2842424 .
- ^ Na, y; Парк, Soyoung; Хан, Су Бонг; Хан, Хун; Ко, Сангвон; Чанг, Сукбок (2004). «Катализируемая рутением олефинация и сузуки-реакции Suzuki: исследования природы каталитических видов». J. Am. Химический Соц 126 (1): 250–258. doi : 10.1021/ja038742q . PMID 14709090 .
- ^ Подпрыгнуть до: а беременный Weires, Nicholas A.; Бейкер, Эмма Л.; Гарг, Нил К. (2015). «Связанная с никель-катализированием Suzuki-Miyaura Supling of Amides». Природная химия . 8 (1): 75–79. Bibcode : 2016natch ... 8 ... 75W . doi : 10.1038/nchem.2388 . PMID 26673267 .
- ^ Моландер, Гари А.; Биолатто, Бетина (2003). «Катализируемые палладием Suzuki-Miyaura реакции перекрестного связывания калия арил- и гетероарилтрифлуороборатов». J. Org. Химический 68 (11): 4302–4314. doi : 10.1021/jo0342368 . PMID 12762730 .
- ^ Бейтс, Родерик (2012). Органический синтез с использованием переходных металлов . Уайли. ISBN 978-1119978930 .
- ^ Подпрыгнуть до: а беременный Долливер, Дебра; Бхаттарай, Биджай Т.; Пандей, Арджун; Lanier, Megan L.; Bordelon, Amber S.; Аадхикари, Сарджу; Динсер, Джордан А.; Цветы, Патрик Ф.; Уиллс, Вероника С.; Schneider, Caroline L.; Шоннесс, Кевин Х.; Мур, Джейн Н.; Рейдерс, Стивен М.; Сноуден, Тимоти С.; МакКим, Арти С.; Fronczek, Frank R. (2013). «Стареоспецифические реакции Suzuki, Sonogashira и Negishi йодид и метров» Negishi ». J. Org. Химический 78 (8): 3676–3 Doi : 10.1021/ jo4 23534335PMID
- ^ Asachenko, Andrey; Sorochkina, Kristina; Dzhevakov, Pavel; Topchiy, Maxim; Nechaev, Mikhail (2013). "Suzuki–Miyaura Cross-Coupling under Solvent-Free Conditions". Adv. Synth. Catal . 355 (18): 3553–3557. doi : 10.1002/adsc.201300741 .
- ^ Пан, Чандуо; Лю, Чжан; Wu, Huayue; Дин, Джинчан; Ченг, Цзян (2008). «Палладий катализируется без лиганда, не содержащая лиганд, реакция перекрестной связи Suzuki». Катализ связи . 9 (4): 321–323. doi : 10.1016/j.catcom.2007.06.022 .
- ^ Подпрыгнуть до: а беременный Литтке, Адам Ф.; FU (2000). «Универсальные катализаторы для перекрестной связывания арилбороновых кислот с арил и виниловыми галогенками и трифлируются в мягких условиях». J. Am. Химический Соц 122 (17): 4020–4028. doi : 10.1021/ja0002058 .
- ^ Ху, Мин-Ганг; Вэй, песня; Цзянь, AI-AI (2007). «Высокоэффективная реакция сочетания Suzuki PD/C-катализируемой Suzuki ofp- (un) замещают фенилгалогенид (p-замещенным фенил) боронной кислотой». Китайский журнал химии . 25 (8): 1183–1186. doi : 10.1002/cjoc.200790220 .
- ^ Сайто, б; FU (2007). «Алкил-алкил Сузуки поперечные связи неактивированных вторичных алкилгалогенидов при комнатной температуре» . J. Am. Химический Соц 129 (31): 9602–9603. doi : 10.1021/ja074008l . PMC 2569998 . PMID 17628067 .
- ^ Кингстон, СП; Веркад, Джон Г. (2007). «Синтез и характеристика R2PNP (ibunch2Ch2) 3n: новый громоздкий электрон, богатый электроном фосфина для эффективных реакций перекрестного связанного со стороны Suzuki-Miyaura» ». J. Org. Химический 72 (8): 2816–2822. doi : 10.1021/jo062452l . PMID 17378611 .
- ^ Baillie, C; Чжан, Ликсин; Сяо, Цзяньлян (2004). «Ферросенил -монофосфинные лиганды: синтез и применение в связке Suzuki -Miyaura арилхлоридов». J. Org. Химический 69 (22): 7779–7782. doi : 10.1021/jo048963u . PMID 15498017 .
- ^ Хан, J; Лю, y; Го, Р. (2009). «Формальный синтез высоко стабильных наночастиц золота и их неожиданная превосходная каталитическая активность для реакции перекрестного связанного связки Сузуки-мияура в воде». J. Am. Химический Соц 131 (6): 2060–2061. doi : 10.1021/ja808935n . PMID 19170490 .
- ^ Lipshutz, BH; Petersen, Tue B.; Абела, Александр Р. (2008). «Комната-температурная муфты Suzuki-Miyaura в воде, облегчаемая неионовыми амфифилами †». Орг Летал 10 (7): 1333–1336. doi : 10.1021/ol702714y . PMID 18335944 .