Связь возбуждения и сокращения сердца
Связь сердечного возбуждения-сокращения сердечная ЭК -связь ) описывает серию событий, от выработки потенциала действия) до сокращения мышц электрического импульса ( сердца . ( [1] Этот процесс имеет жизненно важное значение, поскольку он позволяет сердцу биться контролируемым образом, без необходимости сознательного участия. Соединение ЕС приводит к последовательному сокращению сердечных мышц , что позволяет кровь перекачивать сначала в легкие ( малое кровообращение ), а затем по всему телу ( системное кровообращение ) со скоростью от 60 до 100 ударов в минуту, когда тело находится в состоянии покоя. [2] Однако эта частота может быть изменена нервами , которые либо увеличивают частоту сердечных сокращений ( симпатические нервы ), либо уменьшают ее ( парасимпатические нервы ), поскольку потребность организма в кислороде меняется. В конечном счете, сокращение мышц вращается вокруг заряженного атома (иона) кальция (Ca 2+ ) , [3] который отвечает за преобразование электрической энергии потенциала действия в механическую энергию (сокращение) мышцы. Это достигается в области мышечной клетки, называемой поперечными канальцами, во время процесса, известного как высвобождение кальция, индуцированное кальцием . [4]
Инициация
[ редактировать ]В стенке правого предсердия расположена группа специализированных клеток, называемая синоатриальным узлом (САН) . Эти клетки, в отличие от большинства других , могут клеток сердца спонтанно вырабатывать потенциалы действия . [5] Эти потенциалы действия распространяются вдоль клеточной мембраны (сарколеммы) в виде импульсов, переходящих от одной клетки к другой через каналы в структурах, известных как щелевые контакты . [6]
Высвобождение кальция, индуцированное кальцием
[ редактировать ]Определенные участки сарколеммы проникают глубоко в клетку . Они известны как поперечные канальцы (Т-трубочки) ; которые также обнаружены в клетках скелетных мышц и позволяют потенциалу действия перемещаться в центр клетки. [7] Специальные белки, называемые кальциевыми каналами L-типа (также известные как дигидропиридиновые рецепторы (DHPR)) расположены на мембране Т-канальцев и активируются потенциалом действия. Активированные DHPR открываются, образуя канал , по которому поступает Ca 2+ пройти в клетку. Это увеличение Ca 2+ , затем связывается и активирует другой рецептор , называемый рианодиновым рецептором 2 типа (RyR2) , расположенный на мембране структуры, известной как саркоплазматический ретикулум (SR) . SR представляет собой Ca 2+ хранится внутри клетки и расположен очень близко к Т-трубочкам. Активация RyR2 заставляет его открываться, высвобождая еще больше Ca. 2+ В клетку этот выброс кальция называется кальциевой искрой . Это означает, что начальный поток Ca 2+ в клетку , вызывало большее высвобождение Ca 2+ внутри клетки , поэтому этот процесс называется кальций-индуцированным высвобождением кальция (CICR) . [8]
Сокращение мышц
[ редактировать ]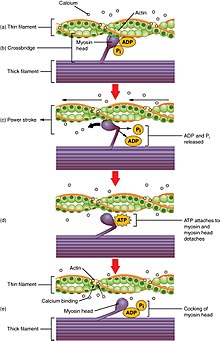
Увеличение Са 2+ , созданный CICR, теперь выполняет две функции. Во-первых, он связывается с внутриклеточной стороной DHPR, сигнализируя каналам о закрытии и предотвращая дальнейший приток Ca. 2+ в клетку. Во-вторых, Ка 2+ косвенно активирует белки , называемые миофиламентами , что приводит к сокращению мышц . Двумя основными миофиламентами сердечной (и скелетной ) мышцы являются актин и миозин . Калифорния 2+ связывается с белком тропонином , который связан с актиновой нитью. Это связывание вызывает изменение формы тропонина, в результате чего обнажаются участки актина , с которыми связывается головка миозиновой нити . Связывание головки миозина с актином известно как поперечный мостик. Молекула , затем используется в качестве , называемая аденозинтрифосфатом (АТФ) , которая вырабатывается внутриклеточной структурой, называемой митохондрией источника энергии, чтобы помочь переместить головку миозина, несущую актин. В результате актин скользит по миозиновой нити, укорачивая мышцу. Это называется силовым ударом. Затем миозин отделяется от актина и возвращается в исходное положение, связываясь с другой частью актина и производя еще один мощный удар, еще больше укорачивая мышцу . Этот процесс продолжается, причем головка миозина движется подобно движению весла в лодке, пока Ca 2+ уровень внутри клетки снижается (см. рисунок 1). [9]
Прекращение сокращения
[ редактировать ]Сокращение заканчивается, когда Ca 2+ удаляется из клетки. Когда это происходит, тропонин возвращается к своей первоначальной форме, блокируя места связывания актина и предотвращая образование поперечных мостиков. Это снижение Ca 2+ Внутри клетки осуществляется различными белками , известными под общим названием переносчики ионов . Основными задействованными насосами являются: саркоплазматический ретикулум Ca 2+ -АТФаза , перекачивающая Ca 2+ обратно в СР, сарколеммальный натрий-кальциевый обменник , который перекачивает один Са 2+ из клетки в обмен на 3 иона натрия, закачиваемые в клетку, сарколеммальный Са 2+ -АТФаза , которая использует АТФ для перекачки кальция. 2+ непосредственно из клетки и митохондриального Са 2+ Система Uniport , перекачивающая Ca 2+ в митохондрии. [10]
Частота сердечных сокращений
[ редактировать ]Симпатические нервы работают, высвобождая белок ( нейромедиатор ) под названием норадреналин , который связывается со специфическим рецептором ( бета-1-адренорецептором ), расположенным в сарколемме и мембране Т-канальцев сердечных клеток . Это активирует белок, называемый G-белком, и приводит к серии реакций (известных как путь циклического АМФ ), которые приводят к выработке молекулы под названием цАМФ ( циклический аденозинмонофосфат ). В SAN цАМФ связывается с ионным каналом, участвующим в инициации потенциала действия, ускоряя выработку потенциала действия ( см. В синоатриальном узле более подробно ). цАМФ также активирует белок , называемый протеинкиназой А ( PKA ). PKA влияет как на кальциевые каналы L-типа (также известные как дигидропиридиновые рецепторы (DHPR)) и RyR , увеличивая повышение уровня Ca. 2+ внутри сократительных клеток и, следовательно, увеличивает скорость мышечного сокращения . PKA также влияет на миофиламенты , а также на белок, называемый фосфоламбаном (PLB; более подробную информацию см. в саркоплазматическом ретикулуме ), ускоряя скорость высвобождения кальция. 2+ снижение клеток и, следовательно, ускорение мышечной релаксации . [2]
Парасимпатические нервы работают, высвобождая нейромедиатор, называемый ацетилхолином (АХ), который связывается со специфическим рецептором ( мускариновым рецептором М2 ) на сарколемме как клеток SAN, так и клеток желудочков. Это снова активирует G-белок . Однако этот G-белок действует путем ингибирования пути цАМФ, тем самым предотвращая увеличение частоты сердечных сокращений симпатической нервной системой. Кроме того, в SAN G-белок активирует специфический калиевый канал, который противодействует инициации потенциала действия ( см. SAN ), тем самым замедляя частоту сердечных сокращений. подробнее [2]
Ссылки
[ редактировать ]- ^ Сантана, Луис Ф.; Ченг, Эдвард П.; Ледерер, В. Джонатан (2010). «Как форма сердечного потенциала действия контролирует передачу сигналов кальция и сокращение сердца?» . Журнал молекулярной и клеточной кардиологии . 49 (6): 901–903. дои : 10.1016/j.yjmcc.2010.09.005 . ISSN 1095-8584 . ПМЦ 3623268 . ПМИД 20850450 .
- ^ Перейти обратно: а б с Гордан, Ричард; Гватми, Джудит К.; Се, Лай-Хуа (26 апреля 2015 г.). «Вегетативная и эндокринная регуляция сердечно-сосудистой функции» . Всемирный журнал кардиологии . 7 (4): 204–214. дои : 10.4330/wjc.v7.i4.204 . ISSN 1949-8462 . ПМК 4404375 . ПМИД 25914789 .
- ^ Маркс, Эндрю Р. (2003). «Кальций и сердце: вопрос жизни и смерти» . Журнал клинических исследований . 111 (5): 597–600. дои : 10.1172/JCI18067 . ISSN 0021-9738 . ПМК 151912 . ПМИД 12618512 .
- ^ Вонг, AY; Фабиато, А.; Бассингтуэйт, Дж. Б. (1992). «Модель механизма высвобождения кальция, индуцированного кальцием, в сердечных клетках» . Бюллетень математической биологии . 54 (1): 95–116. дои : 10.1007/BF02458622 . ISSN 0092-8240 . ПМЦ 4331357 . ПМИД 25665663 .
- ^ Монфреди, Оливер; Добжински, Галина; Мондал, Тапас; Бойетт, Марк Р.; Моррис, Гвилим М. (2010). «Анатомия и физиология синоатриального узла - Современный обзор: АНАТОМИЯ И ФИЗИОЛОГИЯ СИНОАТРИАЛЬНОГО УЗЛА». Стимуляция и клиническая электрофизиология . 33 (11): 1392–1406. дои : 10.1111/j.1540-8159.2010.02838.x . ПМИД 20946278 .
- ^ Куртенбах, Стефан; Куртенбах, Сара; Зойдл, Георг (2014). «Модуляция щелевого соединения и ее значение для функции сердца» . Границы в физиологии . 5 : 82. дои : 10.3389/fphys.2014.00082 . ISSN 1664-042X . ПМЦ 3936571 . ПМИД 24578694 .
- ^ Хун, ТинТин; Шоу, Робин М. (2017). «Микроанатомия и функция сердечных Т-трубочек» . Физиологические обзоры . 97 (1): 227–252. doi : 10.1152/physrev.00037.2015 . ISSN 0031-9333 . ПМК 6151489 . ПМИД 27881552 .
- ^ Хинч, Р.; Гринштейн, Дж.Л.; Тансканен, А.Дж.; Сюй, Л.; Уинслоу, Р.Л. (2004). «Упрощенная модель местного контроля высвобождения кальция, индуцированного кальцием, в миоцитах желудочков сердца» . Биофизический журнал . 87 (6): 3723–3736. Бибкод : 2004BpJ....87.3723H . дои : 10.1529/biophysj.104.049973 . ISSN 0006-3495 . ПМК 1304886 . PMID 15465866 .
- ^ Лодиш, Х.; Берк, А.; Зипурский, Л.С.; Мацудайра, П.; Балтимор, округ Колумбия; Дарнелл, Дж. (2000). «Мышцы: специализированный сократительный аппарат» . Архивировано из оригинала 27 апреля 2016 года.
- ^ Балке, CW; Иган, ТМ; Вир, В.Г. (1 февраля 1994 г.). «Процессы удаления кальция из цитоплазмы во время сопряжения возбуждения-сокращения в интактных клетках сердца крысы» . Журнал физиологии . 474 (3): 447–462. дои : 10.1113/jphysicalol.1994.sp020036 . ISSN 0022-3751 . ПМЦ 1160336 . ПМИД 8014906 .