Сольвотермический синтез
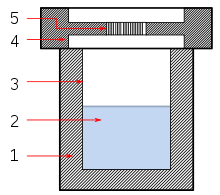
Сольвотермический синтез — метод получения химических соединений , при котором растворитель, содержащий реагенты, помещают под высокое давление и температуру в автоклав . Многие вещества лучше растворяются в одном и том же растворителе в таких условиях, чем в стандартных условиях , что позволяет проводить реакции, которые в противном случае не могли бы произойти, и приводя к новым соединениям или полиморфам . Сольвотермальный синтез очень похож на гидротермальный путь; оба обычно проводятся в автоклаве из нержавеющей стали. Единственное отличие состоит в том, что раствор предшественника обычно неводный . [1]
использовался сольвотермический синтез Для получения MOF . [2] [3] диоксид титана , [4] и графен , [5] углеродные сферы, [6] халькогениды [7] и другие материалы.
Растворители
[ редактировать ]Помимо воды (гидротермальный синтез), в сольвотермальном синтезе используется широкий спектр растворителей, включая аммиак , диоксид углерода , диметилформамид и различные спирты, такие как метанол , или гликоли, такие как гексан-1,6-диол . [1] [8] [9]
Муравьиная кислота как реакционная среда
[ редактировать ]Муравьиная кислота разлагается при высоких температурах на углекислый газ и водород или оксид углерода и воду. Это свойство позволяет использовать муравьиную кислоту в качестве восстановительной и богатой углекислым газом реакционной среды, в которой возможно образование различных оксидов и карбонатов . [8]
Аммиак как реакционная среда
[ редактировать ]Критическая температура и давление аммиака составляют 132,2 °С и 111 бар. В этих условиях можно получить ряд амидов , имидов и нитридов . Хотя его диэлектрическая проницаемость ниже, чем у воды, аммиак ведет себя как полярный растворитель, особенно при высоких давлениях. [8]
Ссылки
[ редактировать ]- ^ Jump up to: а б Демазо, Г. (2008). «Сольвотермические реакции: оригинальный путь синтеза новых материалов». Дж. Матер. Наука . 43 (7): 2104–2114. Бибкод : 2008JMatS..43.2104D . дои : 10.1007/s10853-007-2024-9 . S2CID 55825984 .
- ^ Яги, ОМ ; Калмуцкий, МЮ; Диркс, CS (2019). Введение в ретикулярную химию: металлоорганические каркасы и ковалентные органические каркасы . Вайнхайм: Wiley-VCH . ISBN 978-3-527-82110-5 .
- ^ Фарха, Омар К.; Хапп, Джозеф Т. (2010). «Рациональный дизайн, синтез, очистка и активация материалов металлоорганического каркаса». Отчеты о химических исследованиях . 43 (8): 1166–1175. дои : 10.1021/ar1000617 . ПМИД 20608672 .
- ^ Онг, Ви-Джун; Тан, Ллинг-Ллинг; Чай, Сян-Пяо; Йонг, Сик-Тинг; Мохамед, Абдул Рахман (2014). «Высокореактивные грани {001} композитов на основе TiO 2 : синтез, механизм образования и характеристика». Наномасштаб . 6 (4): 1946–2008. Бибкод : 2014Nanos...6.1946O . дои : 10.1039/c3nr04655a . ПМИД 24384624 .
- ^ Сян, Цюаньцзюнь; Ю, Цзяго; Яронец, Метек (2012). «Полупроводниковые фотокатализаторы на основе графена». хим. Соц. Преподобный . 41 (2): 782–796. дои : 10.1039/C1CS15172J . ПМИД 21853184 .
- ^ Ху, Банда; Ма, Дин; Ченг, Модзи; Лю, Лин; Бао, Синьхэ (2002). «Прямой синтез однородных полых углеродных сфер с помощью шаблона самосборки». Химические коммуникации (17): 1948–1949. дои : 10.1039/B205723A . ПМИД 12271688 .
- ^ Ли, Дж.; Чен, З.; Ван, Р.Дж.; Прозерпио, DM (1999). «Низкотемпературный путь к новым материалам: сольвотермический синтез халькогенидов металлов в этилендиамине». Обзоры координационной химии . 190–192: 707–735. дои : 10.1016/S0010-8545(99)00107-1 .
- ^ Jump up to: а б с Рабенау, Альбрехт (1985). «Роль гидротермального синтеза в препаративной химии» . Angewandte Chemie International Edition на английском языке . 24 (12): 1026–1040. дои : 10.1002/anie.198510261 . ISSN 0570-0833 .
- ^ Справочник Спрингера по выращиванию кристаллов . Говиндхан Дханарадж. Гейдельберг: Спрингер. 2010. ISBN 978-3-540-74761-1 . OCLC 671821738 .
{{cite book}}: CS1 maint: другие ( ссылка )