Биомиметический синтез
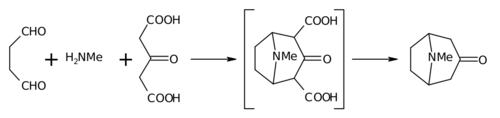
Биомиметический синтез — это область органического химического синтеза , имеющая конкретное биологическое происхождение. Этот термин охватывает как проверку «биогенетической гипотезы» ( предполагаемого хода биосинтеза в природе) посредством выполнения серии реакций, параллельных предполагаемому биосинтезу, так и программы исследований, в которых синтетическая реакция или реакции, направленные на желаемая синтетическая цель предназначена для имитации одной или нескольких известных ферментных трансформаций установленного пути биосинтеза . [1] [2] Самым ранним широко цитируемым примером биомиметического синтеза является осуществленный сэром Робертом Робинсоном органический синтез алкалоида тропинона, . [3]
Более свежий пример — проведенная Э. Дж. Кори с карбениевая циклизация искусственно созданного линейного полиена, образованием тетрациклической стероидной кольцевой системы. [4] который основан на исследованиях катионной циклизации линейных полиенов Альбертом Эшенмозером и Гилбертом Сторком , [5] [6] и обширные исследования У.С. Джонсона по определению требований для инициирования и прекращения циклизации, а также для стабилизации катионной карбениевой группы во время циклизации (как это происходит в природе с помощью ферментов во время биосинтеза стероидов, таких как холестерин ). [7] Что касается второго определения, синтетические органические или неорганические катализаторы, применяемые для осуществления химического превращения, осуществляемого в природе с помощью биокатализатора (например, чисто белкового катализатора , металла или другого кофактора, связанного с ферментом , или рибозима можно сказать, что ), являются осуществлять биомиметический синтез, где разработка и характеристика таких каталитических систем получила название биомиметической химии . [8] [9] [10]
Синтез прото -дафнифиллина
[ редактировать ]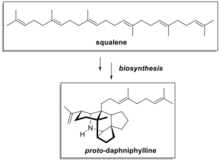

Прото -дафнифиллин является предшественником в биосинтезе семейства алкалоидов, обнаруженных в Daphniphyllum macropodum . Он представляет интерес из-за своей сложной молекулярной структуры , что делает его сложной мишенью для традиционных методов органического синтеза из-за конденсированной кольцевой структуры и спироуглеродного центра. Основываясь на предложенном пути биосинтеза прото -дафнифиллина из сквалена , Клейтон Хиткок и его коллеги разработали удивительно элегантный и короткий общий синтез прото -дафнифиллина из простых исходных материалов. [11] Это пример того, как биомиметический синтез может упростить общий синтез сложного природного продукта.
Ключевой этап синтетического пути Хиткока включает циклизацию ациклических диальдегидов A или B с образованием прото -дафнифиллина. Оба диальдегида (А или В) имеют углеродный скелет, аналогичный сквалену, и могут быть синтезированы из простых исходных материалов. Обработка А или В последовательностью простых реагентов, содержащих гидроксид калия , аммиак и уксусную кислоту , привела к образованию прото -дафнифиллина. На этом замечательном этапе образовались шесть σ-связей и пять колец. В исходном отчете было предложено, что промежуточный гидроксилдигидропиран C впервые образовался, когда исходный диальдегид (A) обрабатывался гидроксидом калия. Промежуточное соединение 2-аза-1,3-диен (D) было получено в результате реакции промежуточного соединения C с аммиаком. катализируемой кислотой, В результате реакции Дильса-Альдера, образовалось промежуточное соединение E, которое в дальнейшем превращалось в конечный продукт в условиях реакции.
Примеры биомиметических синтезов в Википедии
[ редактировать ]- карпанон , с помощью подхода Чепмена
- спиротрипростатин B , с помощью подхода Ganesan
- эндиандровая кислота , см. Биомиметический полный синтез , с использованием подхода Николау.
Дополнительные литературные примеры биомиметического синтеза
[ редактировать ]- Синтез Merck C-нор-D-гомостероидов типа накитерпиозина , например, структурный: расщепленные, сжатые и расширенные кольца (секо-, нор- и гомостероиды) , посредством миграции атома C-13. [12]
- Синтез Хиткока сквалена , посредством каскадов тетрациклизации или пентациклизации. алкалоидов типа дафнифиллина, производных [13] [14]
Ссылки
[ редактировать ]- ^ де ла Торре MC, Сьерра, Массачусетс (январь 2004 г.). «Комментарии к последним достижениям биомиметического органического синтеза». Энджью. хим. Межд. Эд. англ . 43 (2): 160–81. дои : 10.1002/anie.200200545 . ПМИД 14695603 .
- ^ ван Тамелен Э.Э. (1961). «Синтез натуральных продуктов биогенетического типа». Достижения в химии органических натуральных продуктов / Прогресс в химии органических натуральных продуктов / Progrès dans la Chimie des Substances Organiques Naturelles . Том 19. С. 242–290. дои : 10.1007/978-3-7091-7156-1_5 . ISBN 978-3-7091-7158-5 . ПМИД 13924635 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Робинсон Р. (1917). «LXIII. Синтез тропинона» . Журнал Химического общества, Сделки . 111 : 762–768. дои : 10.1039/CT9171100762 .
- ^ Кори Э.Дж., Луо Г., Лин Л.С. (1997). «Простой энантиоселективный синтез биологически активного тетрациклического морского сестертерпена скаларендиала». Дж. Ам. хим. Соц . 119 (41): 9927–28. дои : 10.1021/ja972690l .
- ^ Эшенмозер А., Феликс Д., Гут М., Мейер Дж., Стадлер П. (1959). «Некоторые аспекты кислотно-катализируемой циклизации терпеноидных полиенов». В Wolstenholme GE, O'Conner M (ред.). Симпозиум Фонда Ciba по биосинтезу терпенов и стероидов . Симпозиумы Фонда Новартис. Лондон: Дж. И А. Черчилль. стр. 217–230. дои : 10.1002/9780470719121.ch14 . ISBN 9780470719121 .
- ^ Сторк Г., Бургстралер А.В. (1955). «Стереохимия циклизации полиенов». Дж. Ам. хим. Соц . 77 (19): 5068–77. дои : 10.1021/ja01624a038 .
- ^ Джонсон В.С., Маршалл Дж.А., Киана Дж.Ф., Франк Р.В., Мартин Д.Г., Бауэр Дж.В. (1966). «Полный синтез стероидов - подход гидрохризена - XVI: рацемический конессин, прогестерон, холестерин и некоторые родственные натуральные продукты». Тетраэдр . 22 : 541–601. дои : 10.1016/S0040-4020(01)90961-5 .
- ^ Бреслоу Р. (январь 2009 г.). «Биомиметическая химия: биология как источник вдохновения» . Журнал биологической химии . 284 (3): 1337–42. дои : 10.1074/jbc.X800011200 . ПМИД 18784073 .
- ^ Ли С.К., Холм Р.Х. (апрель 2003 г.). «Спекулятивная синтетическая химия и проблема нитрогеназы» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (7): 3595–600. дои : 10.1073/pnas.0630028100 . ПМК 152967 . ПМИД 12642670 .
- ^ Бреслоу Р. (1995). «Биомиметическая химия и искусственные ферменты: катализ по замыслу». Отчеты о химических исследованиях . 28 (3): 146–153. дои : 10.1021/ar00051a008 .
- ^ Пьеттр С., Хиткок CH (июнь 1990 г.). «Биомиметический полный синтез протодафнифиллина». Наука . 248 (4962): 1532–4. Бибкод : 1990Sci...248.1532P . дои : 10.1126/science.248.4962.1532 . ПМИД 17818314 . S2CID 37777797 .
- ^ Гао С., Чен С. (2012). «Накитерпиозин» . В Ли Дж., Кори Э. Дж. (ред.). Полный синтез натуральных продуктов: на передовых рубежах органической химии . Берлин: Шпрингер. стр. 25–38. ISBN 978-3-642-34065-9 .
- ^ Хиткок CH , Хансен М.М., Руджери Р.Б., Кэт Дж.К. (1992). «Алкалоиды дафнифилла. 11. Биомиметический тотальный синтез метилгомосекодафнифиллата. Развитие реакции тетрациклизации». Журнал органической химии . 57 (9): 2544–53. дои : 10.1021/jo00035a008 .
- ^ Хиткок CH , Пьеттр С., Руджери Р.Б., Рэган Дж.А., Кэт Дж.К. (1992). «Алкалоиды дафнифиллума. 12. Предлагаемый биосинтез пентациклического скелета. Прото -дафнифиллин». Журнал органической химии . 57 (9): 2554–66. дои : 10.1021/jo00035a009 .
Дальнейшее чтение
[ редактировать ]- Пупон Э, Нет Б, ред. (2011). Биомиметический органический синтез . Алкалоиды. Том. 1. Wiley-VCH Verlag GmbH & Co. КГаА. дои : 10.1002/9783527634606 . ISBN 978-3-527-32580-1 .
- Эшли Э (5 января 2004 г.). «Биомиметический синтез натуральных продуктов» (PDF) . Литературный семинар Исследовательской группы Штольца . Калифорнийский технологический институт. Архивировано из оригинала (PDF) 23 июня 2010 г. Проверено 24 ноября 2013 г.