Уранилхлорид
 | |
| Имена | |
|---|---|
| Название ИЮПАК Дихлордиоксоуран | |
| Другие имена Уран(VI), дихлордиокси | |
| Идентификаторы | |
3D model ( JSmol ) |
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.029.315 |
| Номер ЕС |
|
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| УО 2 Cl 2 | |
| Молярная масса | 340.90 |
| Температура плавления | Разлагается |
| Точка кипения | Разлагается |
| Растворимость в других растворителях | 320 при 18°С |
| Опасности | |
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
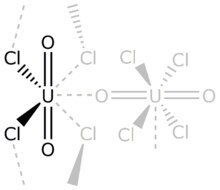
Хлорид уранила относится к неорганическим соединениям формулы UO 2 Cl 2 (H 2 O) n , где n = 0, 1 или 3. Это соли желтого цвета.
Синтез и структуры
[ редактировать ]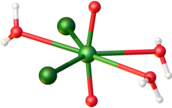
Гидраты получают растворением уранилсульфата или уранилацетата в соляной кислоте с последующей кристаллизацией из концентрированных растворов. В зависимости от метода сушки получают моно- или тригидрат. Моногидрат описывается как желтый сероподобный порошок. Он очень гигроскопичен. [2] Тригидрат зеленовато-желтого цвета. Оба гидрата представляют собой флуоресцентные твердые вещества, хорошо растворимые в воде. [3]
Безводный материал можно получить реакцией кислорода с тетрахлоридом урана :
- UCl 4 + O 2 → UO 2 Cl 2 + Cl 2
По строению все три этих соединения имеют уранильный центр ( транс -UO 2 2+ ) связан с пятью дополнительными лигандами, которые могут включать (мостиковый) хлорид, воду или другой уранильный кислород. [4] [5]
Реакции
[ редактировать ]Водные лиганды могут быть заменены различными донорами, например ТГФ . [6]
Промышленное значение
[ редактировать ]Компания Indian Rare Earths Limited (IREL) разработала процесс добычи урана из песков западных и восточных прибрежных дюн Индии . После предварительной обработки с помощью высокоинтенсивных магнитных сепараторов и тонкого измельчения минеральные пески (известные как монацит ) разлагаются каустической содой при температуре около 120 ° C (248 ° F) и водой. Гидроксидный концентрат далее разлагается концентрированной соляной кислотой для растворения всех гидроксидов с образованием исходного раствора, состоящего из хлоридов урана и других редкоземельных элементов, включая торий . Раствор подвергают жидкостно-жидкостной экстракции с использованием двойной системы растворителей для получения хлорида уранила и оксалата тория . Неочищенный раствор хлорида уранила затем очищают до диураната аммония ядерной чистоты с помощью процесса очистки, включающего осаждение и экстракцию растворителем в нитратной среде.
Ссылки
[ редактировать ]- ^ Дебец, ПК (1968). «Строение хлорида уранила и его гидратов». Acta Crystallographica Раздел B: Структурная кристаллография и кристаллохимия . 24 (3): 400–402. Бибкод : 1968AcCrB..24..400D . дои : 10.1107/S056774086800244X .
- ^ Хефли, Джек Д.; Мэтьюз, Дэниел М.; Эмис, Эдвард С. (1963). «Уранилхлорид 1-гидрат». Неорганические синтезы . Том. 7. С. 146–148. дои : 10.1002/9780470132388.ch41 . ISBN 978-0-470-13238-8 .
- ^ Ф. Хейн, С. Герцог (1963). «Уранилхлорид». В Г. Брауэре (ред.). Справочник по препаративной неорганической химии, 2-е изд . Том. 2. Нью-Йорк, Нью-Йорк: Академик Пресс. п. 1439.
- ^ Тейлор, Дж. К.; Уилсон, PW (1973). «Структура безводного хлорида уранила по данным порошковой нейтронографии». Acta Crystallographica Раздел B: Структурная кристаллография и кристаллохимия . 29 (5): 1073–1076. Бибкод : 1973AcCrB..29.1073T . дои : 10.1107/S0567740873003882 .
- ^ Лири, Джозеф А.; Саттл, Джон Ф. (1957). «Уранилхлорид». Неорганические синтезы . Том. 5. С. 148–150. дои : 10.1002/9780470132364.ch41 . ISBN 978-0-470-13236-4 .
- ^ Вилкерсон, Марианна П.; Бернс, Кэрол Дж.; Пейн, Роберт Т.; Скотт, Брайан Л. (1999). «Синтез и кристаллическая структура UO 2 Cl 2 (THF) 3 : простое приготовление безводного уранильного реагента». Неорганическая химия . 38 (18): 4156–4158. дои : 10.1021/ic990159g .
- "Уран". энциклопедия Британская Том. В27. 1911. с. 788
- Привет, SJ (1998). «Лантаноиды и актиниды» . Четыре лекции по неорганической химии на 2-м курсе . Архивировано из оригинала 23 сентября 2017 года . Проверено 22 ноября 2011 г.
Внешние ссылки
[ редактировать ]- Урегулируй, Фрэнк. «Ядерная химия и сообщество» . www.chemcases.com: Практические примеры по общей химии . Архивировано из оригинала 22 ноября 2011 года . Проверено 22 ноября 2011 г.