3-бензокспин
| |
| Имена | |
|---|---|
| Предпочтительное имя IUPAC
3-бензокспин | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Chemspider | |
PubChem CID
|
|
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 10 H 8 O | |
| Молярная масса | 144.173 g·mol −1 |
| Появление | Желтое твердое вещество [ 1 ] |
| Точка плавления | 84 (83–84 ° C; [ 3 ] 84 ° C. [ 1 ] ) |
| Растворимость | растворимый в аполярных растворителях ( диэтиловый эфир , бензол , тетрахлорметан ) [ 2 ] и спирты ( метанол ) [ 3 ] |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
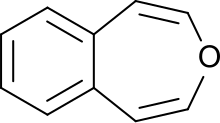
3-бензоксипин -это иннозованная кольцевая система с ароматическим бензольным кольцом и неароматическим, ненасыщенным, содержащим кислород с семью членами гетероциклического кислота . Первый синтез был описан Карлом ДиМротом и коллегами в 1961 году. [ 1 ] Это один из трех изомеров бензоксипинов .
Появление и синтез
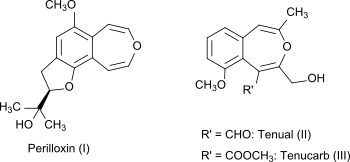
[ редактировать ]3-бензоксипин сам является не натуральным соединением, но бициклическая кольцевая система является частью естественных соединений периллоксин (I) из Perilla Frutescens (вариант acuta ) [ 4 ] и десять (2) и tenucarb (3) из асфодина тоньше . [ 5 ] Периллоксин ингибирует фермент циклооксигеназу с IC 50 из 23,2 мкм. [ 4 ] Нестероидные противовоспалительные препараты, такие как аспирин и ибупрофен, также работают, ингибируя семейство ферментов циклооксигеназы . [ 6 ]
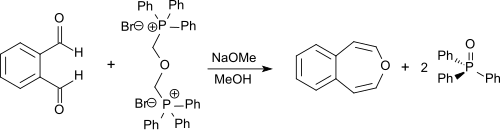
Непоместный 3-бензоксипин может быть синтезирован с помощью двойной реакции остроумия от о -фталальдегида с бис-(α, α'-трифенилфосфониум) -диметилоэтерэфиром-дибромидом. [ 3 ] Последнее соединение может быть синтезировано из α, α'-дибромодиметилового эфира (бис (бромметил) эфира или BBME), который доступен из гидробромической кислоты , параформальдегида , [ 7 ] и трифенилфосфин . Реакция выполняется в сухом метаноле с метоксидом натрия, а продукт получают с выходом 55%. [ 1 ] [ 2 ]
Соединение также может быть получено посредством ультрафиолета определенных производных нафталинов , таких как 1,4-эпокси-1,4-дигидронафталин. [ 8 ]
Он также может быть получен путем фотоокисления 1,4-дигидронафталина, за которым следует пиролиз образованных гидропероксидов . [ 9 ]
Последние синтезы дают 3-бензоксипины с низкими урожаями (4–6%). [ 8 ]
Характеристики
[ редактировать ]3-бензоксипин-это ярко-желтое твердое вещество, которое кристаллизуется в тромбоцитах, с запахом, похожим на нафталин . Материал растворим в аполярных, органических растворителях. Как нафталин, его можно очистить путем сублимации. Твердое вещество относительно устойчиво к кислотному, только при рефлюксе в концентрированных кислотных спиртовых растворах ненасыщенный альдегид образуется (вероятно, инден -3-альдегид). Каталитическое гидрирование с палладиевым катализатором приводит к 1,2,4,5-тетрагидро-3-бензокспину.
Ссылки
[ редактировать ]- ^ Jump up to: а беременный в дюймовый Dimroth, K.; Пол, Г. (1961). «3-бензокспин». Ангев. Химический 73 (12): 436. Bibcode : 1961angch..73..436d . doi : 10.1002/ange.19610731215 .
- ^ Jump up to: а беременный Росоровский, А., изд. (1972). «II. Окспиновые кольцевые системы, содержащие два кольца». Семь членов гетероциклических соединений, содержащих кислород и серы . Химия гетероциклических соединений (на немецком языке). Тол. 26 -й Нью-Йорк: Wiley-Interscience . п. 96. ISBN 0-471-38210-8 .
- ^ Jump up to: а беременный в Dimroth, K.; Пол, Г.; Follmann, H. (1966). «Синтез производных 3-оксопина и фурана через двукратную реакцию Wittig». Хим. (на немецком языке). 99 (2): 634–641. Doi : 10.1002/cber.19660990238 .
- ^ Jump up to: а беременный Лю, Дж. Х.; Steigel, A.; Рейнингер, E.; Бауэр Р. (2000). «Два новых пренилированных производных 3-бензоксипина в качестве ингибиторов циклооксигеназы из периллы Frutescens var. Acuta ». J. Nat Продлевать 63 (3): 403–405. doi : 10.1021/np990362o . PMID 10757731 .
- ^ Ulubelen, A .; Tuzlaci, E.; Атилан, Н. (1989). «Производные оксейпина и антрахиноны из асфоделя Тенуиор и А. Таурика ». Фитохимия . 28 (2): 649–650. Bibcode : 1989pchem..28..649U . doi : 10.1016/0031-9422 (89) 80076-7 .
- ^ Кестер, М.; Карпа, KD; Vrana, KE (2011). "НПВП" . Фармакология . Интегрированный обзор Elsevier. Elsevier Health Sciences . С. 165–166. ISBN 9780323074452 .
- ^ Патент США 20040242799 , Grabranick, M. & Sasson, Y., «Процесс для бромаметилата ароматических соединений», опубликованный 2004-12-02, назначен Grabranick, M. и Sasson, Y.
- ^ Jump up to: а беременный Циглер, Гр (1969). «Механизмы фотохимических реакций в растворе. LVII. Фотореористение 1,4-эпокси-1,4-дигидронафталин к бензу [ F ] окспину». J. Am. Химический Соц 91 (2): 446–449. doi : 10.1021/ja01030a040 .
- ^ Джеффри, Ам; Джерина, Д.М. (1972). «Автооксидирование 1,4-дигидронафталина. Образование 3-бензоксипина посредством пиролиза 2-гидроперокси-1,2-дигидронафталин». J. Am. Химический Соц 94 (11): 4048–4049. doi : 10.1021/ja00766a084 .