Онколитический вирус герпеса
Эта статья требует более надежных медицинских ссылок для проверки или слишком сильно полагается на первичные источники . ( март 2013 г. ) |  |
Части этой статьи (связанные с клиническими испытаниями HSV1716) должны быть обновлены . ( Сентябрь 2015 г. ) |
| Онколитический вирус герпеса | |
|---|---|
| |
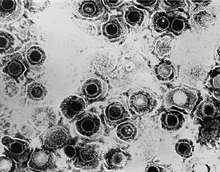
| TEM -микрофотография вируса простого герпеса. | |
| Классификация вирусов | |
| (не вмешательство): | Вирус |
| Область : | Дуплоднавирия |
| Королевство: | Heunggongvirae |
| Филум: | Peploviricata |
| Сорт: | Herviviricetes |
| Заказ: | Герпесвиралс |
| Семья: | Orthoherpesviridae |
| Род: | Simplexvirus |
| Разновидность: | Человеческий альфахерпесвирус 1
|
Многие варианты вируса простого герпеса были рассмотрены для вирусной терапии рака; Раннее развитие их было тщательно рассмотрено в журнале генной терапии рака в 2002 году. [ 1 ] На этой странице описывается (в порядке разработки) наиболее заметные варианты-те проверки в клинических испытаниях: G207, HSV1716, NV1020 и Talimogene LaherparepVEC (ранее OncoveX-GMCSF). Эти ослабленные версии построены путем удаления вирусных генов, необходимых для инфицирования или репликации внутри нормальных клеток, но не раковых клеток, таких как ICP34.5 , ICP6/UL39 и ICP47 .

HSV1716
[ редактировать ]HSV1716 первого поколения, -это онколитический вирус разработанный Институтом вирусологии Глазго , а затем By Biologics Virttu (бывшие Crusade Laboratories, вытекающий из Института вирусологии), для избирательного разрушения раковых клеток. Вирус имеет торговое название сеприрвир . Он основан на вирусе простого герпеса (HSV-1). Штамм HSV1716 имеет делецию гена ICP34.5 . ICP34.5 является геном нейровирулентности (позволяет воспроизвести вирус в нейронах головного и спинного мозга). Удаление этого гена обеспечивает свойство опухоли-селективной репликации в вирусе (т.е. в значительной степени предотвращает репликацию в нормальных клетках, в то же время позволяя репликации в опухолевых клетках), хотя она также снижает репликацию в опухолевых клетках по сравнению с ВПС дикого типа. [ 2 ] [ 3 ]
Жизненно важная часть нормального механизма HSV-1, белок ICP34.5 был предложен для состояния после митотических клеток для репликации вируса . Без гена ICP34.5 вариант HSV-1716 не может преодолеть нормальную защиту здоровых дифференцированных клеток (опосредованных PKR ) для эффективного воспроизведения. Однако опухолевые клетки имеют гораздо более слабую защиту от PKR, что может быть причиной, по которой HSV1716 эффективно убивает широкий спектр линий опухолевых клеток в культуре тканей .
Вариант HSV1716, HSV1716NTR - это онколитический вирус, генерируемый путем вставки фермента NTR в вирус HSV1716 в качестве стратегии GDEPT . [ 4 ] In vivo, введение пролекарства CB1954 для атимических мышей, несущих ксенотрансплантаты опухоли A431 или A2780, через 48 часов после внутрилуморальной инъекции HSV1790 приводили к заметному снижению объемов опухолей и значительному улучшению выживаемости по сравнению с только введением только вируса. Аналогичный подход был принят с вариантом HSV1716, который экспрессирует транспортер норадреналина для доставки радиоактивного йода в отдельные инфицированные раковые клетки, путем помечения белка, который транспортирует раковые клетки. Транспортер с норсиреналином специально транспортирует соединение, содержащее радиоактивный йод через клеточную мембрану, используя гены из вируса. Единственные клетки в организме, которые получают значительную дозу радиации, - это инфицированные и их непосредственные соседи. [ 5 ]
Клинические испытания
[ редактировать ]- высокой степени Глиома : три фазы I были завершены, а два исследования II фазы находятся в подготовке. [ 6 ] [ 7 ]
- Плоскоклеточная карцинома головы и шеи : исследование I фазы было завершено. [ 8 ]
- Злокачественная меланома : исследование I фазы была завершена. [ 9 ]
- Гепатоцеллюлярная карцинома : исследование фазы I/II находится в подготовке.
- Злокачественная плевральная мезотелиома : проходит исследование фазы I/II. [ 10 ]
- не CNS Педиатрический рак : проходит исследование I фазы. [ 11 ]
G207
[ редактировать ]G207 был построен в виде вектора второго поколения из лабораторного штамма HSV-1, с удалением ICP34.5 и геном ICP6, инактивированным путем введения гена E. coli Lacz . [ 12 ]
Два фазы I Клинические испытания в глиоме были завершены. [ 13 ] [ 14 ] [ 15 ] Результаты первого испытания были опубликованы одновременно с первым испытанием HSV1716 в 2000 году, когда комментаторы восхваляли демонстрацию безопасности этих вирусов при введении в опухоли головного мозга, но также выражали разочарование, что репликация вируса не может быть продемонстрирована из -за сложности принятия Биопсия из опухолей головного мозга. [ 16 ]
NV1020
[ редактировать ]NV1020 - это онколитический вирус герпеса, первоначально разработанный Medigene Inc. и лицензированный на разработку Catherex Inc. в 2010 году. [ 17 ] NV1020 имеет только одну копию гена ICP34.5, а ICP6 не повреждена. [ 1 ] Прямое сравнение NV1020 и G207 в мышиной модели перитонеального рака показало, что NV1020 более эффективен в более низких дозах. [ 18 ]
Клинические испытания
[ редактировать ]Исследование фазы I/II завершено в 2008 году, оценивающее NV1020 для лечения метастатического колоректального рака в печени. [ 19 ] Исследование оценило ответ опухоли с помощью компьютерной томографии и сканирования FDG-PET , показывая, что 67% пациентов имели первоначальное увеличение размера опухоли, а затем с последующим снижением 64% пациентов. [ 20 ] [ 18 ]
Talimogene Laherpeccex
[ редактировать ]Talimogene LaherparepVEC -это имя USAN для онколитического вируса, также известного как «Oncovex GM-CSF». Он был разработан Biovex Inc. (Woburn, MA, USA и Oxford, UK) до тех пор, пока Biovex не была приобретена Amgen в январе 2011 года. [ 21 ]
Это вирус простого герпеса второго поколения , основанный на штамме JS1 и экспрессирующий иммунный стимулирующий фактор GM-CSF . [ 22 ] [ 23 ] Как и другие онколитические версии HSV, он имеет делецию гена, кодирующего ICP34.5, который обеспечивает селективность опухоли. [ 24 ] Он также имеет делецию гена, кодирующего ICP47, белка, который ингибирует презентацию антигена, [ 25 ] и вставка гена, кодирующего GM-CSF , иммунного стимулирующего цитокина. [ 2 ] [ 3 ] Удаление гена, кодирующего ICP47, также ставит ген US11 (поздний ген) под контроль непосредственного раннего промотора ICP47. Более ранняя и более высокая экспрессия US11 (также участвующая в преодолении PKR-опосредованных ответов) в значительной степени преодолевает снижение репликации в опухолевых клетках ICP34,5-очищенного HSV по сравнению с вирусом дикого типа, но без снижения селективности опухоли.
- Клинические испытания
В том числе этап III: см. Talimogene LaherparepVEC
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный Варгезе С., Рабкин С.Д. (декабрь 2002 г.). «Онколитический герпес простой векторы вируса вируса рака виротерапии» . Генная терапия рака . 9 (12): 967–78. doi : 10.1038/sj.cgt.7700537 . PMID 12522436 .
- ^ Jump up to: а беременный Mohr I, Gluzman Y (сентябрь 1996 г.). «Генетический элемент герпесвируса, который влияет на трансляцию в отсутствие вирусной функции GADD34» . Embo Journal . 15 (17): 4759–66. doi : 10.1002/j.1460-2075.1996.tb00853.x . PMC 452208 . PMID 8887567 .
- ^ Jump up to: а беременный Лю Б.Л., Робинсон М., Хан З.К., Бранстон Р.Х., Английский С., Рей П. и др. (Февраль 2003 г.). «ICP34.5 удалил вирус простого герпеса с усиленными онколитическими, иммунными стимулирующими и противотумурными свойствами». Генная терапия . 10 (4): 292–303. doi : 10.1038/sj.gt.3301885 . PMID 12595888 . S2CID 11464646 .
- ^ Брэйдвуд Л., Данн П.Д., Харди С., Эванс Т.Р., Браун С.М. (июнь 2009 г.). «Противоопухолевая активность селективно репликации компетентного вируса простого герпеса (HSV) с ферментом пролекарственной терапии» . Противоопухолевые исследования . 29 (6): 2159–66. PMID 19528476 .
- ^ Соренсен А., Марс Р.Дж., Брэйдвуд Л., Джойс С., Коннер Дж., Пимлотт С. и др. (Апрель 2012 г.). «Оценка in vivo стратегии терапии рака, объединяющая HSV1716-опосредованный онколиз с переносом генов и целевой лучевой терапией» . Журнал ядерной медицины . 53 (4): 647–54. doi : 10.2967/jnumed.111.090886 . PMID 22414636 .
- ^ Harrow S, Papanastassiou V, Harland J, Mabbs R, Petty R, Fraser M, et al. (Ноябрь 2004 г.). «Инъекция HSV1716 в мозг, прилегающий к опухоли после хирургической резекции глиомы высокой степени: данные безопасности и долгосрочная выживаемость». Генная терапия . 11 (22): 1648–58. doi : 10.1038/sj.gt.3302289 . PMID 15334111 . S2CID 14604628 .
- ^ Papanastassiou V, Rampling R, Fraser M, Petty R, Hadley D, Nicoll J, et al. (Март 2002 г.). «Потенциал для эффективности модифицированного (ICP 34.5 (-)) вируса простого герпеса HSV1716 после внутрипумуральной инъекции в злокачественную глиому человека: доказательство принципа исследования» . Генная терапия . 9 (6): 398–406. doi : 10.1038/sj.gt.3301664 . PMID 11960316 .
- ^ MACE AT, Ganly I, Soutar DS, Brown SM (август 2008 г.). «Потенциал эффективности вируса простого герпеса 1716 онколитического герпеса 1716 у пациентов с плоскоклеточным карциномой полости рта». Голова и шея . 30 (8): 1045–51. doi : 10.1002/hed.20840 . PMID 18615711 . S2CID 43914133 .
- ^ Маки Р.М., Стюарт Б., Браун С.М. (февраль 2001 г.). «Интралезионная инъекция вируса простого герпеса 1716 при метастатической меланоме». Лансет . 357 (9255): 525–6. doi : 10.1016/s0140-6736 (00) 04048-4 . PMID 11229673 . S2CID 34442464 .
- ^ Клиническое исследование номер NCT01721018 для «внутриплеврального введения HSV1716 для лечения пациентов со злокачественной плевральной мезотелиомой» на клинике.
- ^ Клиническое исследование номер NCT00931931 для «HSV1716 у пациентов с нецентральной нервной системой (не-CNS) солидные опухоли» на клинических.
- ^ Минета Т., Рабкин С.Д., Язаки Т., Хантер В.Д., Мартуза Р.Л. (сентябрь 1995 г.). «Затухание мульти-мутированного вируса простого герпеса-1 для лечения злокачественных глиомов». Природная медицина . 1 (9): 938–43. doi : 10.1038/nm0995-938 . PMID 7585221 . S2CID 8712053 .
- ^ Markert JM, Medlock MD, Rabkin SD, Gillespie GY, Todo T, Hunter WD, et al. (Май 2000). «Угодна, воспроизведение мутанта вируса простого герпеса, G207 для лечения злокачественной глиомы: результаты исследования I фазы» . Генная терапия . 7 (10): 867–74. doi : 10.1038/sj.gt.3301205 . PMID 10845725 .
- ^ Номер клинического исследования NCT00028158 для «исследования безопасности и эффективности G207, вируса, убивающего опухоль, у пациентов с рецидивирующим раком головного мозга» на клинических
- ^ Клиническое исследование номер NCT00157703 для "G207 с последующей лучевой терапией при злокачественной глиоме" на клинике.
- ^ Kirn DH (май 2000). «Сказка о двух испытаниях: избирательно реплицирование герпесвирусов для опухолей головного мозга» . Генная терапия . 7 (10): 815–6. doi : 10.1038/sj.gt.3301213 . PMID 10845717 .
- ^ «Medigene AG -дипломирует программу онколитического герпеса (OHSV) в Catherex, Inc» (пресс -релиз). Medigene Ag. 13 апреля 2010 года. Архивировано с оригинала 29 октября 2013 года . Получено 7 мая 2013 года .
- ^ Jump up to: а беременный Geevarghese SK, Geller Da, De Haan Ha, Hörer M, Knoll AE, Mescheder A, et al. (Сентябрь 2010). «Фаза I/II исследование онколитического вируса простого герпеса NV1020 у пациентов с широко предварительно обработанной рефрактерным колоректальным раком метастатического в печень» . Генная терапия человека . 21 (9): 1119–28. doi : 10.1089/hum.2010.020 . PMC 3733135 . PMID 20486770 .
- ^ Клиническое исследование номер NCT00149396 для «безопасности и эффективности генетически спроектированного вируса простого герпеса NV1020 для лечения метастатического рака колоректального рака» на клинических обращениях.
- ^ Sze Dy, Iaguu AH, Gambhir SS, de Haan Ha, Reid Tr (январь 2012 г.). «Ответ на внутриартериальную онколитическую виротерапию вирусом герпеса NV1020, оцененная [18F] фтородезоксиглюкозой, позитронно-эмиссионная томография и компьютерная томография». Генная терапия человека . 23 (1): 91–7. doi : 10.1089/hum.2011.141 . PMID 21895536 .
- ^ «Amgen, форма 8-K, текущий отчет, дата подачи 26 января 2012 г.» (PDF) . secdatabase.com . Получено 8 января 2013 года .
- ^ «Отправка OncoveXGM-CSF RAC» (PDF) . NIH Генетическая модификация Информационная система клинических исследований (Gemcris®). Архивировано из оригинала (PDF) 28 мая 2010 года . Получено 1 апреля 2013 года .
- ^ Hu JC, Coffin RS, Davis CJ, Graham NJ, Groves N, Guest PJ, et al. (Ноябрь 2006 г.). «Исследование фазы I oncovexgm-CSF, онколитического герпеса, экспрессирующего макрофаг-макрофагов онколитического герпеса, экспрессирующий макрофаги гранулоцитов». Клиническое исследование рака . 12 (22): 6737–47. doi : 10.1158/1078-0432.ccr-06-0759 . PMID 17121894 . S2CID 30005391 .
- ^ Raafat N, Sadowski-Cron C, Mengus C, Heberer M, Spagnoli GC, Zajac P (сентябрь 2012 г.). «Предотвращение вируса вакцинии класса I эпитопов с помощью HSV-ICP47 усиливает иммуногенность эпитопа, независимой от TAP против рака» . Международный журнал рака . 131 (5): E659-69. doi : 10.1002/ijc.27362 . PMID 22116674 .
- ^ Broughton SE, Dhagat U, Hercus TR, Nero TL, Grimbaldeston MA, Bonder CS, et al. (Ноябрь 2012). «Семейство рецепторов цитокинов GM-CSF/IL-3/IL-5: от распознавания лиганда до инициации передачи сигналов». Иммунологические обзоры . 250 (1): 277–302. doi : 10.1111/j.1600-065x.2012.01164.x . PMID 23046136 . S2CID 11220164 .