Дендрален
Дендрален представляет собой дискретный ациклический перекрестно-сопряженный полиен . [ 1 ] [ 2 ] [ 3 ] Простейшим дендраленом является бута-1,3-диен (1) или [2]дендрален, за которым следуют [3]дендрален (2), [4]дендрален (3), [5]дендрален (4) и так далее. [2]дендрален (бутадиен) — единственный, не имеющий перекрестной конъюгации.
Название дендрален составлено из слов дендример , линейный и алкен . Высшие дендралены представляют научный интерес, поскольку они открывают большое количество новых органических соединений из относительно простого предшественника, особенно с помощью химии Дильса-Альдера . Их циклические аналоги метко называются радиенами .
Синтез
[ редактировать ]Винилбутадиен ([3]дендрален) был впервые получен в 1955 году пиролизом триацетата: [ 4 ] [ 5 ]
Это соединение реагирует с двумя эквивалентами малеинового ангидрида в тандемной DA-реакции: [ 6 ]
С бензохиноном продукт реакции представлял собой линейный полимер.
Сообщалось о нескольких синтезах замещенных [3]дендраленов, один через аллен , [ 7 ] один через реакцию Горнера-Уодсворта-Эммонса , [ 8 ] один через реакцию кросс-сочетания [ 9 ] и один из аллильного карбоната. [ 10 ]
Один синтеза путь [4]дендралена начинается с хлоропрена . [ 11 ] Это соединение превращается в реактив Гриньяра под действием металлического магния , который затем вступает в реакцию с хлоридом меди (I) с образованием медьорганического промежуточного продукта, который, в свою очередь, димеризуется с использованием хлорида меди (II) в реакции окислительного сочетания с образованием бутадиена димера , называемого [ 4]дендрален.
Сообщается о газофазной молекулярной структуре [4]дендралена. [ 12 ]
О соединении [8]-дендралена сообщалось в 2009 году: [ 13 ]
в последовательном соединении Кумада-Тамао-Корриу и соединении Негиши .
В 2016 году сообщалось о серии от [9] до [12]-дендраленов. [ 14 ]
Характеристики
[ редактировать ]Четночленные дендралены (например, [6]дендрален, [8]дендрален) имеют тенденцию вести себя как цепочки разделенных и изолированных диеновых звеньев. Максимумы ультрафиолетового поглощения равны максимумам самого бутадиена. Дендралены с нечетным числом алкеновых звеньев более реакционноспособны из-за наличия благоприятных s-цис-диеновых конформаций , и реакции Дильса-Альдера протекают легче с предпочтением концов.
Реакции
[ редактировать ]С помощью простых диенофилов дендралены могут обеспечить быстрый доступ к сложным молекулам в реакциях Дильса-Альдера . Сообщалось о нескольких схемах реакций. [ 11 ] [ 15 ] [ 16 ] [ 17 ] [ 18 ] [ 19 ] [ 20 ] [ 21 ] [ 22 ]
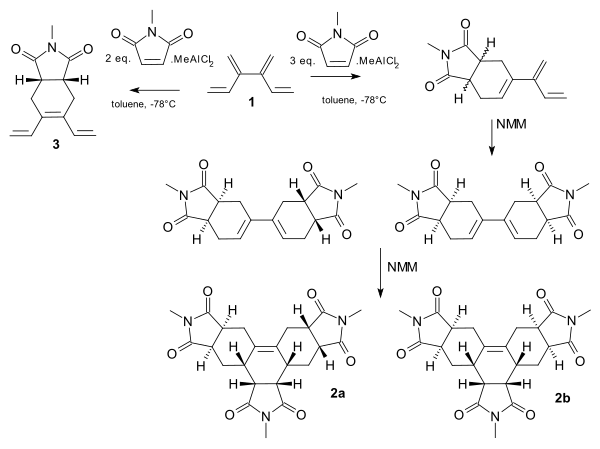
[4]дендрален демонстрирует тандемную реакцию Дильса-Альдера с диенофилом N-метилмалеимидом (NMM). [ 11 ] Полная селективность по сайтам возможна при добавлении кислоты Льюиса метилдихлоралюминия . При одном наборе предварительного смешивания и двух эквивалентах NMM центральная диеновая группа направляется к моноаддукту 3 . С другим набором и большим количеством диенофила концевые группы реагируют и реакция идет от моноаддукта к трисаддуктам 2 и 2b .
Одним из вариантов реакции является циклопропанирование до класса соединений, называемых ивианы , с известным синтезом в реакции Симмонса-Смита ( диэтилцинк / трифторуксусная кислота ). первых 6 членов [ 23 ] Эти 1,1-олигоциклопропаны стабильны (кроме случаев воздействия кислот) и имеют большую теплоту сгорания, причем [6]ивиан превышает теплоту сгорания кубана . Цепи олигоциклопропана принимают спиральную конформацию. Сообщалось о фотохимической реакции циклизации [3] дендралена. [ 24 ]
Производные
[ редактировать ]Сообщалось о бициклическом соединении [4]дендралена. [ 25 ]
Ссылки
[ редактировать ]- ^ Хеннинг Хопф, Классика химии углеводородов , Wiley VCH, 2000.
- ^ Хопф, Х.; Шерберн, Миссисипи (2012). «Дендралены разветвляются: перекрестно-сопряженные олигоены позволяют быстро создавать молекулярную сложность». Angewandte Chemie International Edition на английском языке . 51 (10): 2298–2338. дои : 10.1002/anie.201102987 . ПМИД 22337341 .
- ^ Получение и синтетическая ценность разветвленных углеводородов с π-связями. Майкл С. Шерберн. Отчеты о химических исследованиях, 2015, 48 (7), 1961-1970. doi : 10.1021/acs.accounts.5b00242
- ^ Бейли, Уильям Дж.; Экономика, Джеймс (1955). «Пиролиз эфиров. III. Синтез 2-винилбутадиена». Дж. Ам. хим. Соц . 77 (5): 1133–1136. дои : 10.1021/ja01610a014 .
- ^ Бломквист, AT; Вердоль, Джозеф А. (1955). «2-Винил-1,3-бутадиен». Дж. Ам. хим. Соц . 77 (1): 81–83. дои : 10.1021/ja01606a025 .
- ^ Бейли, Уильям Дж.; Экономика, Джеймс; Гермес, Мэтью Э. (1962). «Полимеры. IV. Полимерные реакции Дильса-Альдера». Дж. Орг. Хим . 27 (9): 3295–3299. дои : 10.1021/jo01056a074 .
- ^ Миеко Арисава, Такумичи Сугихара и Масахико Ямагути Синтез перекрестно-сопряженных триенов путем димеризации алленов с палладий-фенольным катализатором Chem. Коммун. 1998 год; 26:15-26:16 два : 10.1039/A807527A
- ^ Рекха Сингх и Сунил К. Гош Синтез замещенных [3] дендраленов и их уникальные реакции циклоприсоединения Chem. Коммун. 2011 г.; Предварительная статья два : 10.1039/C1CC14211A
- ^ Брэдфорд, Таня А.; Пейн, Алан Д.; Уиллис, Энтони К.; Паддон-Роу, Майкл Н.; Шерберн, Майкл С. (2007). «Кросс-сочетание для кросс-сопряжения:? Практический синтез и реакции Дильса-Альдера [3] дендраленов». Органические письма . 9 (23): 4861–4864. дои : 10.1021/ol7021998 . ПМИД 17929828 .
- ^ Кассем Бейдун, Хуэй-Джун Чжан, Баскер Сундарараджу, Бернар Демерсеман, Матье Ашар, Женфэн Си и Кристиан Брюно Эффективный катализируемый рутением синтез [3] дендраленов из 1,3-диеновых аллильных карбонатов Chem. Коммун. 2009 г.; 6580-6582 дои : 10.1039/B913595B
- ^ Jump up to: а б с Пейн, Алан Д.; Уиллис, Энтони К.; Шерберн, Майкл С. (2005). «Практический синтез и химия Дильса-Альдера [4] дендралена». Журнал Американского химического общества . 127 (35): 12188–12189. дои : 10.1021/ja053772+ . ISSN 0002-7863 . ПМИД 16131173 .
- ^ Молекулярная структура 3,4-диметиленгекса-1,5-диена ([4]дендралена), C8H10, в газовой фазе, определенная методом дифракции электронов и расчетами ab initio Пол Т. Брэйн, Брюс А. Смарт, Хизер Э. Робертсон, Мартин Дж. Дэвис,†, Дэвид У.Х. Рэнкин*, Уильям Дж. Генри и Ян Госни. Журнал органической продукции. Химия 1997 62 (9), 2767-2773. дои : 10.1021/jo962091h
- ^ Практический синтез семейства дендраленов показывает изменение в поведении Алан Д. Пейн, Гомоцанг Боджасе, Майкл Н. Паддон-Роу и Майкл С. Шерберн Ангью. хим. Межд. Эд. 2009 , 48, два : 10.1002/anie.200901733
- ^ Открытие и вычислительная рационализация уменьшения чередования в [n] дендраленах Мехмет Ф. Саглам, Томас Фэллон, Майкл Н. Паддон-Роу и Майкл С. Шерберн Журнал Американского химического общества 2016 138 (3), 1022-1032 два : 10.1021/jacs.5b11889
- ^ Браммонд, Кей М .; Ты, Линфэн (2005). «Последовательная последовательность реакций Альдер-ена/Дильса-Альдера/Дильса-Альдера, катализируемая Rh(I), обеспечивающая быстрый доступ к полициклическим соединениям». Тетраэдр . 61 (26): 6180–6185. дои : 10.1016/j.tet.2005.03.141 .
- ^ Хопф, Х.; Йылдижан, Ш. (2011). «Высокофункциональные ароматические соединения с угловым анеллированием из дендраленов». Европейский журнал органической химии . 2011 (11): 2029–2034. дои : 10.1002/ejoc.201001536 .
- ^ Новый и простой стереоконтролируемый метод синтеза полигидрохинолинов и пиридопиридазинов с помощью диен-трансмиссионной реакции Дильса-Альдера, включающей обратное электронно-потребное гетероциклоприсоединение Дильса-Альдера перекрестно-сопряженных азатриенов Тетраэдр, Том 64, Выпуск 41, 6 октября 2008 г., Страницы 9705-9716 Сатору Кобаяши, Томоки Фуруя, Такаши Отани и Такао Сайто два : 10.1016/j.tet.2008.07.102
- ^ Синтез мощного противомалярийного амфилектена Сергей В. Пронин и Райан А. Шенви Журнал Американского химического общества 2012 134 (48), 19604-19606 дои : 10.1021/ja310129b
- ^ Грин, Нью-Джерси; Лоуренс, Алабама; Бохасе, Г.; Уиллис, AC; Паддон-Роу, Миннесота; Шерберн, Миссисипи (2013). «Органокаскады домино-циклоприсоединения дендраленов». Энджью. хим. Межд. Эд . 52 (32): 8333–8336. дои : 10.1002/anie.201302185 . ПМИД 23804245 .
- ^ Практический синтез и реакционная способность [3] дендралена Таня А. Брэдфорд, Алан Д. Пейн, Энтони К. Уиллис, Майкл Н. Паддон-Роу и Майкл С. Шерберн Журнал органической химии 2010 75 (2), 491- 494 дои : 10.1021/jo9024557
- ^ Многокомпонентные диен-трансмиссивные последовательности Дильса-Ольхи с аминодендраленами С.М. Тан, А.С. Уиллис, М.Н. Паддон-Роу, М.С. Шерберн, Ангью. хим. Межд. Эд. 2016, 55, 3081. два : 10.1002/anie.201510925
- ^ Синтез и реакционная способность Дильса-Альдера замещенных [4] дендраленов Мехмет Ф. Саглам, Али Р. Альборзи, Алан Д. Пейн, Энтони К. Уиллис, Майкл Н. Паддон-Роу и Майкл С. Шерберн Журнал органической химии 2016 81 (4), 1461-1475 два : 10.1021/acs.joc.5b02583
- ^ Боджасе, Гомоцанг; Нгуен, Тхань В.; Пейн, Алан Д.; Уиллис, Энтони К.; Шерберн, Майкл С. (2011). «Синтез и свойства ивианов: исходные 1,1-олигоциклопропаны» (PDF) . хим. Наука . 2 (2): 229–232. дои : 10.1039/C0SC00500B . hdl : 1885/58011 .
- ^ Tetrahedron Letters, том 35, выпуск 29, 18 июля 1994 г., страницы 5251–5252. Новая фотохимическая реакция производных [3] дендралена Кейджи Окада, Кацуджи Маэхара, Масаджи Ода два : 10.1016/S0040-4039(00)77076-6
- ^ Преобразование азуленов в бициклические производные [4] дендралена и гептафульвена посредством фотохимического циклоприсоединения диалкилсилилана Томоюки Косаи, Синтаро Исида, Такеаки Ивамото Chem. Коммун., 2015,51, 10707-10709 два : 10.1039/C5CC03424H



![[4]Схема синтеза дендралена из хлоропрена](http://upload.wikimedia.org/wikipedia/commons/thumb/4/40/4-dendralene.svg/569px-4-dendralene.svg.png)
![Синтез [8]-дендралена](http://upload.wikimedia.org/wikipedia/commons/thumb/9/9d/8-dendralene.svg/411px-8-dendralene.svg.png)