НАПКИ
 | |
| Клинические данные | |
|---|---|
| Другие имена | N -ацетил- п -бензохинонимин; N -ацетилимидохинон |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЭБ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.168.312 |
| Химические и физические данные | |
| Формула | C8H7NOC8H7NO2 |
| Молярная масса | 149.149 g·mol −1 |
| 3D model ( JSmol ) | |
| | |
NAPQI , также известный как NAPBQI или N -ацетил- п -бензохинонимин, представляет собой токсичный побочный продукт, образующийся в ходе метаболизма ксенобиотиков анальгетика парацетамола ( ацетаминофена ). [ 1 ] Обычно он вырабатывается лишь в небольших количествах, а затем почти сразу же детоксицируется в печени.
Однако в некоторых условиях, при которых NAPQI не эффективно детоксифицируется (обычно в случае передозировки парацетамола ), он вызывает серьезное повреждение печени. Это становится очевидным через 3–4 дня после приема внутрь и может привести к смерти от молниеносной печеночной недостаточности через несколько дней после передозировки.
Метаболизм
[ редактировать ]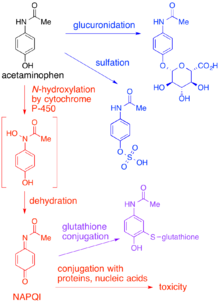
У взрослых основным путем метаболизма парацетамола является глюкуронидация . [ 1 ] В результате образуется относительно нетоксичный метаболит, который выводится с желчью и выводится из организма. Небольшое количество препарата метаболизируется через путь цитохрома P-450 (точнее, CYP3A4 и CYP2E1 ) в NAPQI, который чрезвычайно токсичен для тканей печени, а также является сильным биохимическим окислителем. [ 1 ] У среднестатистического взрослого человека вырабатывается лишь небольшое количество (примерно 10% терапевтической дозы парацетамола) NAPQI, который инактивируется путем конъюгации с глутатионом (GSH). Количество производимого NAPQI различается в разных группах населения. [ нужна ссылка ]
Минимальная дозировка, при которой парацетамол вызывает токсичность, обычно составляет от 7,5 до 10 г для среднестатистического человека. [ 2 ] Смертельная доза обычно составляет от 10 до 15 г. [ нужна ссылка ] Одновременный прием алкоголя значительно снижает эти пороговые значения. Хронические алкоголики могут быть более восприимчивы к побочным эффектам из-за снижения уровня глутатиона. [ 3 ] Другие группы населения могут испытывать эффекты при более низких или более высоких дозах в зависимости от различий в активности фермента P-450 и других факторов, влияющих на количество вырабатываемого NAPQI. Однако в целом основной проблемой является случайная или преднамеренная передозировка парацетамола.
При приеме токсичной дозы парацетамола нормальный путь глюкуронида насыщается и вырабатывается большое количество NAPQI. Запасы глутатиона в печени истощаются в результате конъюгации с избытком NAPQI. Механизм возникновения токсичности сложен, но считается, что он включает реакцию между неконъюгированным NAPQI и важными белками, а также повышенную восприимчивость к окислительному стрессу, вызванному истощением запасов глутатиона. [ 4 ]
Отравление
[ редактировать ]Прогноз благоприятный при передозировке парацетамола, если лечение начато в течение 8 часов после приема препарата. В большинстве больниц имеется антидот ( ацетилцистеин в печени ), который пополняет запасы глутатиона , позволяя NAPQI безопасно метаболизироваться. [ 1 ] Без раннего введения антидота развивается молниеносная печеночная недостаточность , часто в сочетании с почечной недостаточностью, и смерть обычно наступает в течение нескольких дней.
Механизм и противоядие
[ редактировать ]NAPQI становится токсичным, когда GSH истощается в результате передозировки ацетаминофена. Глутатион является важным противоядием от передозировки. Глутатион конъюгируется с NAPQI и помогает его детоксикации. В этом качестве он защищает тиоловые группы клеточных белков, которые в противном случае стали бы ковалентно модифицированными; когда весь GSH израсходован, NAPQI начинает реагировать с клеточными белками , убивая при этом клетки. Предпочтительным лечением передозировки этого обезболивающего является введение N -ацетил- L -цистеина (перорально или внутривенно). [ 5 ] ), который перерабатывается клетками до L -цистеина и используется в de novo синтезе GSH .
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б с д Мехта, С. (25 августа 2012 г.). «Метаболизм парацетамола (ацетаминофена), ацетанилида и фенацетина | Медицинская химия | PharmaXChange.info» . pharmaxchange.info . Архивировано из оригинала 11 мая 2022 года . Проверено 29 августа 2012 г.
- ^ «Токсичность ацетаминофена: основы практики, предыстория, патофизиология» . 5 октября 2021 г.
- ^ «Публикации НИЗ» (PDF) . pubs.niaaa.nih.gov .
- ^ Хинсон Дж. А., Робертс Д. В., Джеймс Л. П. (2010). «Механизмы некроза печени, вызванного ацетаминофеном». Побочные реакции на лекарства . Справочник по экспериментальной фармакологии. Том. 196. стр. 369–405. дои : 10.1007/978-3-642-00663-0_12 . ISBN 978-3-642-00662-3 . ПМЦ 2836803 . ПМИД 20020268 .
- ^ «Фармацевтическая информация – МУКОМИСТ» . RxMed . Проверено 13 февраля 2014 г.
Внешние ссылки
[ редактировать ]- Алсалим В., Фадель М. (июль 2003 г.). «На пути к неотложной медицинской помощи, основанной на фактических данных: лучшие ставки от Королевской больницы Манчестера. Пероральный прием метионина по сравнению с внутривенным N-ацетилцистеином при передозировке парацетамола» . Эмерг Мед Дж . 20 (4): 366–7. дои : 10.1136/emj.20.4.366 . ПМК 1726135 . ПМИД 12835357 .
- ван де Страат Р., де Врис Дж., Дебетс А.Дж., Вермюлен Н.П. (июль 1987 г.). «Механизм предотвращения гепатотоксичности, вызванной парацетамолом, путем замены 3,5-диалкила. Роль истощения глутатиона и окислительного стресса». Биохим. Фармакол . 36 (13): 2065–70. дои : 10.1016/0006-2952(87)90132-8 . ПМИД 3606627 .
- Индукторы, ингибиторы и субстраты цитохрома P-450