Тетрафторборат нитрозония
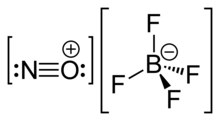
| |
| Имена | |
|---|---|
| Название ИЮПАК
тетрафторборат нитрозония
| |
| Другие имена
нитрозилтетрафторборат
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.035.148 |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| Б Ф 4 Н О | |
| Молярная масса | 116.81 g·mol −1 |
| Появление | бесцветное кристаллическое твердое вещество |
| Плотность | 2,185 г см −3 |
| Температура плавления | 250 ° C (482 ° F; 523 К) (возвышенное состояние) |
| разлагается | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Тетрафторборат нитрозония , также называемый нитрозилтетрафторборатом , представляет собой химическое соединение с химической формулой NOBF 4 . Это бесцветное твердое вещество используется в органическом синтезе в качестве нитрозирующего агента . [ 1 ]
NOBF 4 представляет собой нитрозониевую соль фторборной кислоты и состоит из нитрозония катиона [NO] + и тетрафторборат- анион [BF 4 ] − .
Реакции
[ редактировать ]Доминирующим свойством NOBF 4 является окислительная способность и электрофильный характер катиона нитрозония. Образует цветные комплексы с переносом заряда с гексаметилбензолом и 18-краун-6 . Последний, темно-желтый, позволяет растворять NOBF 4 в дихлорметане. [ 2 ]
Тетрафторборат нитрозония может быть использован для получения солей металлов типа [M II (CH 3 CN) x ][BF 4 ] 2 (M = Cr, Mn, Fe, Co, Ni, Cu). Катион нитрозония действует как окислитель, сам восстанавливаясь до газообразного оксида азота: [ 3 ]
- М + 2НОБФ 4 + х СН 3 CN → [М(СН 3 CN) х ](БФ 4 ) 2 + 2НО
С ферроценом тетрафторборат ферроцения . образуется [ 4 ]
В инфракрасном спектре этой соли ν NO представляет собой сильный пик при 2387 см-1. −1 . [ 5 ]
Ссылки
[ редактировать ]- ^ «А15806 Тетрафторборат нитрозония, 98%» . Альфа-Айсар Сайт . Проверено 4 сентября 2010 г.
- ^ Ли, Кентукки; Кучинка, диджей; Кочи, Джей К. (1990). «Окислительно-восстановительные равновесия катиона нитрозония и его несвязанных комплексов». Неорганическая химия . 29 (21): 4196–4204. дои : 10.1021/ic00346a008 .
- ^ Хайнц, Роберт А.; Смит, Дженнифер А.; Салай, Пол С.; Вайсгербер, Эми; Данбар, Ким Р. (август 2004 г.). «11. Гомолептические катионы ацетонитрила переходных металлов с анионами тетрафторбората или трифторметансульфоната». Неорг. Синтез. 33 : 75–83. дои : 10.1002/0471224502.ch2 . ISBN 978-0-471-46075-6 .
- ^ Роджер М. Нильсон; Джордж Э. МакМанис; Лэнс К. Саффорд; Майкл Дж. Уивер (1989). «Влияние растворителя и электролита на кинетику самообмена ферроцений-ферроцен. Переоценка». Дж. Физ. хим. 93 (5): 2152. doi : 10.1021/j100342a086 .
- ^ Шарп, DWA; Торли, Дж. (1963). «670. Инфракрасный спектр иона нитрозония». Журнал Химического общества (обновленный) : 3557. doi : 10.1039/JR9630003557 .