ПАК-1
 | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.164.322 |
| Химические и физические данные | |
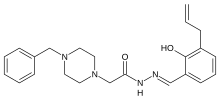
| Формула | С 23 Н 28 Н 4 О 2 |
| Молярная масса | 392.503 g·mol −1 |
| 3D model ( JSmol ) | |
| (проверять) | |
PAC-1 ( первое соединение, активирующее прокаспазу ) представляет собой синтезированное химическое соединение, которое избирательно индуцирует апоптоз в раковых клетках. [ примечание 1 ] присвоило ему статус орфанного препарата В 2016 году FDA .
История
[ редактировать ]PAC-1 был обнаружен в лаборатории профессора Пола Хергенротера в Университете Иллинойса в Урбана-Шампейн во время процесса проверки многих химических веществ на противоопухолевый потенциал. Эта молекула, доставленная в раковые клетки, сигнализирует клеткам о самоуничтожении, активируя белок-"палач" прокаспазу-3 . Затем активированный белок-палач запускает каскад событий, разрушающих механизм клетки. В 2011 году была основана компания Vanquish Oncology Inc. с целью продвижения PAC-1 к клиническим испытаниям на людях. В 2013 году Vanquish объявил о многомиллионных инвестициях в компанию. В 2015 году была открыта фаза I клинического исследования PAC-1 для включения больных раком, а в 2016 году было объявлено, что предоставило PAC-1 статус орфанного препарата для лечения глиобластомы FDA , а в конце 2017 года началась фаза. Начато исследование 1b комбинации PAC-1 с темозоломидом для лечения пациентов с рецидивирующей глиобластомой или анапластической астроцитомой. [ нужна ссылка ]
Механизм действия
[ редактировать ]В клетках белок-палач каспаза-3 хранится в неактивной форме прокаспаза-3. Таким образом, клетка может быстро подвергнуться апоптозу за счет активации уже имеющегося белка. Эта неактивная форма называется зимогеном . Известно, что прокаспаза-3 ингибируется низким уровнем цинка. PAC-1 активирует прокаспазу-3 путем хелатирования цинка, тем самым снимая опосредованное цинком ингибирование. Это позволяет прокаспазе-3 быть активным ферментом, а затем она может расщеплять другую молекулу прокаспазы-3 до активной каспазы-3. Каспаза-3 может дополнительно активировать другие молекулы прокаспазы-3 в клетке, вызывая экспоненциальное увеличение концентрации каспазы-3. PAC-1 облегчает этот процесс и заставляет клетку быстро подвергаться апоптозу. [ 1 ]
Этот способ прямой активации прокаспазы-3 для PAC-1 был подтвержден другими лабораториями: в 2013 году лабораторией Мегени в ходе исследований роли каспазы-3 в кардиомиоцитах, [ 2 ] в 2014 году лабораторией Ву в обширном исследовании противораковой активности и механизма действия PAC-1 и его производных, [ 3 ] и в 2015 году лабораторией Ганди в исследовании потенциала PAC-1 и производного B-PAC-1 для лечения хронического лимфоцитарного лейкоза (ХЛЛ). [ 4 ]
Исследования с нокаутными клетками показали важность прокаспазы-7 как вторичной или альтернативной мишени для PAC-1, особенно в отсутствие прокаспазы-3. Например, эксперименты с использованием эмбриональных фибробластов мыши (MEF) демонстрируют, что двойной нокаут генов CASP3 и CASP7 приводит к образованию клеток, которые нечувствительны к проапоптотическим эффектам соединений класса PAC-1, и снова нокаутируют либо CASP3, либо CASP7. сенсибилизирует эти клетки к соединениям типа PAC-1. [ 5 ] Недавние эксперименты с использованием линий раковых клеток с CRISPR-делецией CASP3 также согласуются с этим результатом. [ 6 ] Активация прокаспазы-7 с помощью PAC-1 согласуется с биохимическими данными, хотя относительная важность мишени прокаспазы-7 в клетках с функциональной прокаспазой-3 неясна. [ нужна ссылка ]
Возникает потенциальная проблема селективности, поскольку прокаспаза-3 присутствует в большинстве клеток организма. Однако было показано, что при многих видах рака, включая некоторые нейробластомы , лимфомы , лейкозы , меланомы и рак печени , прокаспаза-3 присутствует в более высоких концентрациях. [ 1 ] Например, клетки рака легких могут содержать в 1000 раз больше прокаспазы-3, чем нормальные клетки. [ 1 ] Следовательно, контролируя дозировку, можно добиться селективности между нормальными и раковыми клетками.
В дополнение к своей самостоятельной активности было также показано, что PAC-1 заметно взаимодействует с различными одобренными противораковыми препаратами, например, с ингибиторами BRAF и MEK на мышиных моделях меланомы. [ 7 ] и с обычными химиотерапевтическими агентами, такими как доксорубицин, у домашних собак со спонтанным раком, включая лимфому и метастатическую остеосаркому , [ 8 ] и с темозоломидом у домашних собак с естественно возникающей глиомой . [ 9 ]
Vanquish Oncology сообщила о своем намерении начать I фазу клинических испытаний на людях с участием больных раком, которые начнутся в начале 2015 года, и действительно, в феврале 2015 года был открыт набор участников в фазу 1 исследования PAC-1 (NCT02355535). Это исследование проводится в Онкологическом центре Университета Иллинойса в Чикаго, в Онкологическом центре Сидни Киммела при Джонсе Хопкинсе и в Региональной больнице в Сент-Поле, Миннесота. Испытание фазы 1b комбинации PAC-1 плюс темозоломид началось в конце 2017 года в тех же трех центрах (NCT03332355); Пациенты с глиомой высокой степени злокачественности (мультиформная глиобластома (GBM) или анапластическая астроцитома) после прогрессирования после стандартной терапии первой линии имеют право на участие в этом исследовании.
Испытания на животных
[ редактировать ]PAC-1 примечателен тем, что он прошел уникальный путь в клинике, поскольку это, возможно, единственное лекарство от рака, которое впервые было тщательно оценено на домашних собаках со спонтанным раком в качестве прелюдии к клиническим испытаниям на людях. В 2010 году исследование показало, что PAC-1 безопасен для собак, а второе исследование, опубликованное позже в том же году, показало, что производное PAC-1 (называемое S-PAC-1) хорошо переносилось в небольшом клиническом исследовании I фазы. собаки с лимфомой. Совсем недавно, в дополнение к этой активности одного агента, PAC-1 показал мощный синергизм с одобренными противораковыми препаратами, например, с доксорубицином при лечении домашних собак с лимфомой и метастатической остеосаркомой. [ 8 ] и темозоломидом при лечении домашних собак со спонтанной глиомой. [ 9 ]
Клинические испытания на людях
[ редактировать ]PAC-1 тестировался или в настоящее время тестируется в следующих клинических испытаниях на людях:
- Номер клинического исследования NCT02355535 «Соединение-1, активирующее прокаспазу (PAC-1) в лечении запущенных злокачественных опухолей – Компонент 1» на сайте ClinicalTrials.gov.
- Номер клинического исследования NCT03332355 «Соединение-1, активирующее прокаспазу (PAC-1) в лечении запущенных злокачественных опухолей - Компонент 2» на сайте ClinicalTrials.gov.
- Номер клинического исследования NCT03927248 «PAC-1 для лечения рефрактерного метастатического рака почки» на сайте ClinicalTrials.gov.
Примечания
[ редактировать ]- ^ В этой статье речь идет о противоопухолевой молекуле, а не о одноименном антителе, специфичном для активации интегрина a2iib3.
Ссылки
[ редактировать ]- ^ Jump up to: а б с Патт К.С., Чен Г.В., Пирсон Дж.М., Сандхорст Дж.С., Хоугланд М.С., Квон Дж.Т. и др. (октябрь 2006 г.). «Низкомолекулярная активация прокаспазы-3 в каспазу-3 как персонализированная противораковая стратегия». Химическая биология природы . 2 (10): 543–550. дои : 10.1038/nchembio814 . ПМИД 16936720 . S2CID 1689173 .
- ^ Путински С., Абдул-Гани М., Стайлз Р., Брюнетка С., Дик С.А., Фернандо П., Мегени Л.А. (октябрь 2013 г.). «Внутренняя активация каспаз необходима для гипертрофии кардиомиоцитов» . Труды Национальной академии наук Соединенных Штатов Америки . 110 (43): Е4079–Е4087. Бибкод : 2013PNAS..110E4079P . дои : 10.1073/pnas.1315587110 . ПМЦ 3808644 . ПМИД 24101493 .
- ^ Ван Ф., Ван Л., Чжао Ю., Ли Ю., Пин Г., Сяо С. и др. (декабрь 2014 г.). «Новый низкомолекулярный активатор прокаспазы-3 индуцирует апоптоз раковых клеток и уменьшает рост опухоли в ксенотрансплантатах рака молочной железы, печени и желчного пузыря человека» . Молекулярная онкология . 8 (8): 1640–1652. дои : 10.1016/j.molonc.2014.06.015 . ПМЦ 5528581 . ПМИД 25053517 .
- ^ Патель В., Балакришнан К., Китинг М.Дж., Вирда В.Г., Ганди В. (февраль 2015 г.). «Экспрессия прокаспаз-палачей и их активация соединением, активирующим прокаспазу, в клетках хронического лимфоцитарного лейкоза» . Кровь . 125 (7): 1126–1136. дои : 10.1182/blood-2014-01-546796 . ПМЦ 4326772 . ПМИД 25538042 .
- ^ Саркар А., Балакришнан К., Чен Дж., Патель В., Нилапу С.С., МакМюррей Дж.С., Ганди В. (январь 2016 г.). «Молекулярные доказательства хелатирования Zn соединения B-PAC-1, активирующего прокаспазу, при В-клеточной лимфоме» . Онкотаргет . 7 (3): 3461–3476. дои : 10.18632/oncotarget.6505 . ПМЦ 4823120 . ПМИД 26658105 .
- ^ Лин А., Джулиано С.Дж., Палладино А., Джон К.М., Абрамович С., Юань М.Л. и др. (сентябрь 2019 г.). «Нецелевая токсичность является распространенным механизмом действия противораковых препаратов, проходящих клинические испытания» . Наука трансляционной медицины . 11 (509): eaaw8412. doi : 10.1126/scitranslmed.aaw8412 . ПМЦ 7717492 . ПМИД 31511426 .
- ^ Пех Дж., Фан Т.М., Вицисло К.Л., Рот Х.С., Хергенротер П.Дж. (август 2016 г.). «Комбинация вемурафениба и активации прокаспазы-3 синергична при мутантных меланомах BRAF» . Молекулярная терапия рака . 15 (8): 1859–1869. дои : 10.1158/1535-7163.MCT-16-0025 . ПМЦ 4975653 . ПМИД 27297867 .
- ^ Jump up to: а б Ботам Р.К., Рот Х.С., Бук AP, Роуди П.Дж., Фан Т.М., Хергенротер П.Дж. (август 2016 г.). «Активация низкомолекулярной прокаспазы-3 повышает чувствительность рака к лечению различными химиотерапевтическими препаратами» . Центральная научная служба ACS . 2 (8): 545–559. doi : 10.1021/accentsci.6b00165 . ПМЦ 4999974 . ПМИД 27610416 .
- ^ Jump up to: а б Джоши А.Д., Ботам Р.К., Шляйн Л.Дж., Рот Х.С., Мангравити А., Бородовский А. и др. (октябрь 2017 г.). «Синергетическая и таргетная терапия с активатором прокаспазы-3 и темозоломидом увеличивает выживаемость на моделях глиомы на грызунах и возможна для лечения пациентов со злокачественной глиомой у собак» . Онкотаргет . 8 (46): 80124–80138. дои : 10.18632/oncotarget.19085 . ПМЦ 5655184 . ПМИД 29113289 .
Дальнейшее чтение
[ редактировать ]- Петерсон QP, Гуд Д.Р., Вест округ Колумбия, Рэмси К.Н., Ли Дж.Дж., Хергенротер П.Дж. (апрель 2009 г.). «PAC-1 активирует прокаспазу-3 in vitro посредством снятия ингибирования, опосредованного цинком» . Журнал молекулярной биологии . 388 (1): 144–158. дои : 10.1016/j.jmb.2009.03.003 . ПМЦ 2714579 . ПМИД 19281821 .
- Петерсон QP, Сюй Д.К., Гуд Д.Р., Новотный С.Дж., Тоттен Р.К., Хергенротер П.Дж. (сентябрь 2009 г.). «Активация прокаспазы-3 как противораковая стратегия: взаимосвязь структуры и активности соединения 1, активирующего прокаспазу (PAC-1), и его клеточная совместная локализация с каспазой-3» . Журнал медицинской химии . 52 (18): 5721–5731. дои : 10.1021/jm900722z . ПМК 2749958 . ПМИД 19708658 .
- Лукас П.В., Шмит Дж.М., Петерсон К.П., Уэст, округ Колумбия, Сюй, округ Колумбия, Новотный С.Дж. и др. (октябрь 2011 г.). «Фармакокинетика и определение режима противоракового дозирования PAC-1, предпочтительного низкомолекулярного активатора прокаспазы-3, у здоровых собак» . Исследуемые новые лекарства . 29 (5): 901–911. дои : 10.1007/s10637-010-9445-z . ПМЦ 3182491 . ПМИД 20499133 .
- Петерсон К.П., Сюй Д.С., Новотный С.Дж., Уэст Д.К., Ким Д., Шмит Дж.М. и др. (сентябрь 2010 г.). «Открытие и доклиническая оценка на собаках нетоксичного соединения, активирующего прокаспазу-3» . Исследования рака . 70 (18): 7232–7241. дои : 10.1158/0008-5472.can-10-0766 . ПМЦ 3113694 . ПМИД 20823163 .
- Уэст, округ Колумбия, Цинь Ю., Петерсон К.П., Томас Д.Л., Палчаудхури Р., Моррисон К.К. и др. (май 2012 г.). «Дифференциальные эффекты соединений, активирующих прокаспазу-3, на индукцию гибели раковых клеток» . Молекулярная фармацевтика . 9 (5): 1425–1434. дои : 10.1021/mp200673n . ПМЦ 3348238 . ПМИД 22486564 .
- Ботам Р.К., Фан ТМ, Им И, Борст Л.Б., Дириколу Л., Хергенротер П.Дж. (январь 2014 г.). «Двойное нацеливание на прокаспазу-3 с помощью малых молекул резко усиливает активацию зимогена и противораковую активность» . Журнал Американского химического общества . 136 (4): 1312–1319. дои : 10.1021/ja4124303 . ПМЦ 3954530 . ПМИД 24383395 .
Внешние ссылки
[ редактировать ]- Обнаружен «палач» раковой клетки . BBC News, 27 августа 2006 г.
- Раковые клетки «могут жить вечно» . BBC News, 29 апреля 2004 г.
- Победить онкологию
- Ангельские инвестиции помогают продвигать PAC-1 вперед
- FDA предоставило статус орфанного препарата PAC-1 для лечения глиомы
- Клинические испытания фазы 1 PAC-1 на людях, больных раком Clinicaltrials.gov