Онколитический вирус герпеса
Эта статья нуждается в более надежных медицинских ссылках для проверки или слишком сильно полагается на первоисточники . ( март 2013 г. ) |  |
Части этой статьи (относящиеся к клиническим испытаниям HSV1716) необходимо обновить . ( сентябрь 2015 г. ) |
| Онколитический вирус герпеса | |
|---|---|
| |
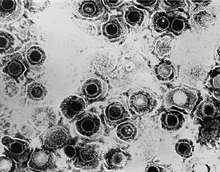
| ПЭМ- микрофотография вируса простого герпеса. | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область : | Дуплоднавирия |
| Королевство: | Хынггунвирэ |
| Тип: | Пепловирикота |
| Сорт: | Гервивирицеты |
| Заказ: | Герпесвирусные инфекции |
| Семья: | Ортогерпесвирусиды |
| Род: | Симплексвирус |
| Разновидность: | Альфагерпесвирус человека 1
|
Многие варианты вируса простого герпеса рассматривались для вирусной терапии рака; их раннее развитие было тщательно рассмотрено в журнале Cancer Gene Therapy в 2002 году. [ 1 ] На этой странице описаны (в порядке разработки) наиболее примечательные варианты, протестированные в клинических испытаниях: G207, HSV1716, NV1020 и Talimogene laherparepvec (ранее Oncovex-GMCSF). Эти ослабленные версии создаются путем удаления вирусных генов, необходимых для заражения или репликации внутри нормальных, но не раковых клеток, таких как ICP34.5 , ICP6/UL39 и ICP47 .

ХСВ1716
[ редактировать ]HSV1716 первого поколения, — онколитический вирус разработанный Институтом вирусологии Глазго , а затем компанией Virttu Biologics (ранее Crusade Laboratories, дочерним предприятием Института вирусологии) для избирательного разрушения раковых клеток. Вирус имеет торговое название SEPREHVIR . В его основе лежит вирус простого герпеса (ВПГ-1). Штамм HSV1716 имеет делецию гена ICP34.5 . ICP34.5 — это ген нейровирулентности (позволяющий вирусу реплицироваться в нейронах головного и спинного мозга). Делеция этого гена обеспечивает свойство опухолеселективной репликации вируса (т.е. в значительной степени предотвращает репликацию в нормальных клетках, в то же время позволяя репликацию в опухолевых клетках), хотя это также снижает репликацию в опухолевых клетках по сравнению с ВПГ дикого типа. [ 2 ] [ 3 ]
Было высказано предположение, что белок ICP34.5, являющийся важной частью нормального механизма ВПГ-1, готовит постмитотические клетки к репликации вируса . Без гена ICP34.5 вариант HSV-1716 не способен преодолеть нормальную защиту здоровых дифференцированных клеток (опосредованную PKR ) для эффективной репликации. Однако опухолевые клетки имеют гораздо более слабую защиту, связанную с PKR, что может быть причиной того, что HSV1716 эффективно убивает широкий спектр линий опухолевых клеток в культуре тканей .
Вариант HSV1716, HSV1716NTR, представляет собой онколитический вирус, созданный путем вставки фермента NTR в вирус HSV1716 в качестве стратегии GDEPT . [ 4 ] In-vivo введение пролекарства CB1954 бестимусным мышам с ксенотрансплантатами опухоли A431 или A2780 через 48 часов после внутриопухолевой инъекции HSV1790 приводило к заметному уменьшению объемов опухоли и значительно улучшало выживаемость по сравнению с введением только вируса. Аналогичный подход был применен к варианту HSV1716, который экспрессирует переносчик норадреналина для доставки радиоактивного йода в отдельные инфицированные раковые клетки путем маркировки белка, который транспортируют раковые клетки. Транспортер норадреналина специфически транспортирует соединение, содержащее радиоактивный йод, через клеточную мембрану, используя гены вируса. Единственные клетки в организме, которые получают значительную дозу радиации, — это инфицированные клетки и их ближайшие соседи. [ 5 ]
Клинические испытания
[ редактировать ]- высокой степени злокачественности Глиома : завершены три исследования фазы I, а два исследования фазы II находятся в стадии подготовки. [ 6 ] [ 7 ]
- Плоскоклеточный рак головы и шеи : завершено исследование I фазы. [ 8 ]
- Злокачественная меланома : завершена фаза I исследования. [ 9 ]
- Гепатоцеллюлярная карцинома : исследование фазы I/II находится в стадии подготовки.
- плевры Злокачественная мезотелиома : продолжается исследование фазы I/II. [ 10 ]
- , не связанный с ЦНС Детский рак : проводится фаза I исследования. [ 11 ]
G207
[ редактировать ]G207 был сконструирован как вектор второго поколения из лабораторного штамма F HSV-1 с удаленным ICP34.5 и инактивированным геном ICP6 путем вставки гена LacZ E. coli . [ 12 ]
две фазы I клинических испытаний при глиоме . Завершены [ 13 ] [ 14 ] [ 15 ] Результаты первого испытания были опубликованы одновременно с первым испытанием HSV1716 в 2000 году. биопсия опухолей головного мозга. [ 16 ]
НВ1020
[ редактировать ]NV1020 — это онколитический вирус герпеса, первоначально разработанный Medigene Inc. и лицензированный для разработки Catherex Inc. в 2010 году. [ 17 ] У NV1020 делеция только одной копии гена ICP34.5, а ICP6 не поврежден. [ 1 ] Прямое сравнение NV1020 и G207 на мышиной модели рака брюшины показало, что NV1020 более эффективен при более низких дозах. [ 18 ]
Клинические испытания
[ редактировать ]В 2008 году завершилось исследование фазы I/II по оценке NV1020 для лечения метастатического колоректального рака в печени. [ 19 ] В исследовании оценивалась реакция опухоли с помощью компьютерной томографии и FDG-ПЭТ , и было показано, что у 67% пациентов первоначально наблюдалось увеличение размера опухоли, а затем уменьшение у 64% пациентов. [ 20 ] [ 18 ]
Талимоген лагерпарепвек
[ редактировать ]Talimogene laherparepvec — это американское название онколитического вируса, также известного как «OncoVEX GM-CSF». Он был разработан компанией BioVex Inc. (Воберн, Массачусетс, США и Оксфорд, Великобритания) до тех пор, пока BioVex не была приобретена компанией Amgen в январе 2011 года. [ 21 ]
второго поколения, Это вирус простого герпеса основанный на штамме JS1 и экспрессирующий иммуностимулирующий фактор GM-CSF . [ 22 ] [ 23 ] Как и другие онколитические варианты ВПГ, он имеет делецию гена, кодирующего ICP34.5, что обеспечивает избирательность опухоли. [ 24 ] У него также есть делеция гена, кодирующего ICP47, белок, который ингибирует презентацию антигена. [ 25 ] и вставку гена, кодирующего GM-CSF , иммуностимулирующий цитокин. [ 2 ] [ 3 ] Удаление гена, кодирующего ICP47, также ставит ген US11 (поздний ген) под контроль непосредственного раннего промотора ICP47. Более ранняя и более высокая экспрессия US11 (также участвующая в преодолении PKR-опосредованных ответов) в значительной степени преодолевает снижение репликации в опухолевых клетках HSV с делецией ICP34.5 по сравнению с вирусом дикого типа, но без снижения селективности опухоли.
- Клинические испытания
Включая фазу III: см. Talimogene laherparepvec.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б Варгезе С., Рабкин С.Д. (декабрь 2002 г.). «Векторы вируса простого онколитического герпеса для виротерапии рака» . Генная терапия рака . 9 (12): 967–78. дои : 10.1038/sj.cgt.7700537 . ПМИД 12522436 .
- ^ Перейти обратно: а б Мор И., Глузман Ю. (сентябрь 1996 г.). «Генетический элемент вируса герпеса, который влияет на трансляцию при отсутствии функции вирусного GADD34» . Журнал ЭМБО . 15 (17): 4759–66. дои : 10.1002/j.1460-2075.1996.tb00853.x . ПМК 452208 . ПМИД 8887567 .
- ^ Перейти обратно: а б Лю Б.Л., Робинсон М., Хан ЗК, Брэнстон Р.Х., Инглиш С., Рей П. и др. (февраль 2003 г.). «Удаленный ICP34.5 вирус простого герпеса с усиленными онколитическими, иммуностимулирующими и противоопухолевыми свойствами». Генная терапия . 10 (4): 292–303. дои : 10.1038/sj.gt.3301885 . ПМИД 12595888 . S2CID 11464646 .
- ^ Брэйдвуд Л., Данн П.Д., Харди С., Эванс Т.Р., Браун С.М. (июнь 2009 г.). «Противоопухолевая активность селективно репликационно компетентного вируса простого герпеса (ВПГ) при ферментной пролекарственной терапии» . Противораковые исследования . 29 (6): 2159–66. ПМИД 19528476 .
- ^ Соренсен А., Майрс Р.Дж., Брэйдвуд Л., Джойс С., Коннер Дж., Пимлотт С. и др. (апрель 2012 г.). «Оценка in vivo стратегии лечения рака, сочетающей онколиз, опосредованный HSV1716, с переносом генов и таргетной лучевой терапией» . Журнал ядерной медицины . 53 (4): 647–54. дои : 10.2967/jnumed.111.090886 . ПМИД 22414636 .
- ^ Харроу С., Папанастассиу В., Харланд Дж., Маббс Р., Петти Р., Фрейзер М. и др. (ноябрь 2004 г.). «Инъекция HSV1716 в мозг, прилегающий к опухоли, после хирургической резекции глиомы высокой степени злокачественности: данные о безопасности и долгосрочная выживаемость». Генная терапия . 11 (22): 1648–58. дои : 10.1038/sj.gt.3302289 . ПМИД 15334111 . S2CID 14604628 .
- ^ Папанастассиу В., Рэмплинг Р., Фрейзер М., Петти Р., Хэдли Д., Николл Дж. и др. (март 2002 г.). «Потенциальная эффективность модифицированного (ICP 34.5(-)) вируса простого герпеса HSV1716 после внутриопухолевой инъекции в злокачественную глиому человека: доказательство принципа исследования» . Генная терапия . 9 (6): 398–406. дои : 10.1038/sj.gt.3301664 . ПМИД 11960316 .
- ^ Мейс А.Т., Ганли И., Сутар Д.С., Браун С.М. (август 2008 г.). «Потенциал эффективности онколитического вируса простого герпеса 1716 у пациентов с плоскоклеточным раком полости рта». Голова и шея . 30 (8): 1045–51. дои : 10.1002/изд.20840 . ПМИД 18615711 . S2CID 43914133 .
- ^ Макки Р.М., Стюарт Б., Браун С.М. (февраль 2001 г.). «Внутриочаговая инъекция вируса простого герпеса 1716 при метастатической меланоме». Ланцет . 357 (9255): 525–6. дои : 10.1016/S0140-6736(00)04048-4 . ПМИД 11229673 . S2CID 34442464 .
- ^ Номер клинического исследования NCT01721018 «Внутриплевральное введение HSV1716 для лечения пациентов со злокачественной мезотелиомой плевры» на сайте ClinicalTrials.gov.
- ^ Номер клинического исследования NCT00931931 «HSV1716 у пациентов с солидными опухолями не в центральной нервной системе (не в ЦНС)» на сайте ClinicalTrials.gov.
- ^ Минета Т., Рабкин С.Д., Язаки Т., Хантер В.Д., Мартуза Р.Л. (сентябрь 1995 г.). «Аттенуированный мультимутантный вирус простого герпеса-1 для лечения злокачественных глиом». Природная медицина . 1 (9): 938–43. дои : 10.1038/nm0995-938 . ПМИД 7585221 . S2CID 8712053 .
- ^ Маркерт Дж.М., Медлок М.Д., Рабкин С.Д., Гиллеспи Г.Я., Тодо Т., Хантер В.Д. и др. (май 2000 г.). «Условно реплицирующийся мутант вируса простого герпеса G207 для лечения злокачественной глиомы: результаты исследования фазы I» . Генная терапия . 7 (10): 867–74. дои : 10.1038/sj.gt.3301205 . ПМИД 10845725 .
- ^ Номер клинического исследования NCT00028158 «Исследование безопасности и эффективности G207, убивающего опухоли вируса, у пациентов с рецидивирующим раком головного мозга» на сайте ClinicalTrials.gov.
- ^ Номер клинического исследования NCT00157703 «G207 с последующей лучевой терапией при злокачественной глиоме» на сайте ClinicalTrials.gov.
- ^ Кирн Д.Х. (май 2000 г.). «История двух испытаний: избирательное воспроизведение герпесвирусов при опухолях головного мозга» . Генная терапия . 7 (10): 815–6. дои : 10.1038/sj.gt.3301213 . ПМИД 10845717 .
- ^ «MediGene AG продает программу по борьбе с онколитическим вирусом простого герпеса (oHSV) компании Catherex, Inc» (пресс-релиз). МедиДжин АГ. 13 апреля 2010 года. Архивировано из оригинала 29 октября 2013 года . Проверено 7 мая 2013 г.
- ^ Перейти обратно: а б Гиваргезе С.К., Геллер Д.А., де Хаан Х.А., Хёрер М., Нолл А.Е., Мешедер А. и др. (сентябрь 2010 г.). «Исследование фазы I/II онколитического вируса простого герпеса NV1020 у пациентов с рефрактерным колоректальным раком, метастатическим в печень, который предварительно лечили» . Генная терапия человека . 21 (9): 1119–28. дои : 10.1089/hum.2010.020 . ПМЦ 3733135 . ПМИД 20486770 .
- ^ Номер клинического исследования NCT00149396 «Безопасность и эффективность генно-инженерного вируса простого герпеса NV1020 для лечения метастазов колоректального рака в печень» на сайте ClinicalTrials.gov.
- ^ Сзе Д.Ю., Ягару А.Х., Гамбхир С.С., Де Хаан Х.А., Рид Т.Р. (январь 2012 г.). «Ответ на внутриартериальную онколитическую виротерапию вирусом герпеса NV1020, оцененную с помощью позитронно-эмиссионной томографии с [18F] фтордезоксиглюкозой и компьютерной томографии». Генная терапия человека . 23 (1): 91–7. дои : 10.1089/hum.2011.141 . ПМИД 21895536 .
- ^ «Amgen, Форма 8-K, Текущий отчет, дата подачи 26 января 2012 г.» (PDF) . secdatabase.com . Проверено 8 января 2013 г.
- ^ «Представление OncoVEXGM-CSF RAC» (PDF) . Информационная система клинических исследований NIH по генетической модификации (GeMCRIS®). Архивировано из оригинала (PDF) 28 мая 2010 года . Проверено 1 апреля 2013 г.
- ^ Ху Дж.К., Коффин Р.С., Дэвис С.Дж., Грэм Н.Дж., Гровс Н., Гость П.Дж. и др. (ноябрь 2006 г.). «Фаза I исследования OncoVEXGM-CSF, онколитического вируса простого герпеса второго поколения, экспрессирующего колониестимулирующий фактор гранулоцитов-макрофагов». Клинические исследования рака . 12 (22): 6737–47. дои : 10.1158/1078-0432.CCR-06-0759 . ПМИД 17121894 . S2CID 30005391 .
- ^ Раафат Н., Садовски-Крон С., Менгус С., Хеберер М., Спаньоли Г.К., Заяк П. (сентябрь 2012 г.). «Предотвращение презентации эпитопов класса I вируса коровьей оспы с помощью HSV-ICP47 повышает иммуногенность TAP-независимого эпитопа противораковой вакцины» . Международный журнал рака . 131 (5): Е659-69. дои : 10.1002/ijc.27362 . ПМИД 22116674 .
- ^ Бротон С.Э., Дагат Ю., Геркус Т.Р., Неро Т.Л., Гримбалдестон М.А., Бондер К.С. и др. (ноябрь 2012 г.). «Семейство цитокиновых рецепторов GM-CSF/IL-3/IL-5: от распознавания лигандов до инициации передачи сигналов». Иммунологические обзоры . 250 (1): 277–302. дои : 10.1111/j.1600-065X.2012.01164.x . ПМИД 23046136 . S2CID 11220164 .