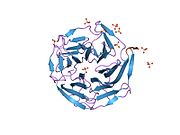
КЕАП1
| КЕАП1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | KEAP1 , INrf2, KLHL19, kelch-подобный ECH-ассоциированный белок 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 606016 ; МГИ : 1858732 ; Гомологен : 8184 ; GeneCards : KEAP1 ; OMA : KEAP1 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Келх-подобный ECH-ассоциированный белок 1 представляет собой белок , который у человека кодируется Keap1 геном . [ 5 ]
Структура
[ редактировать ]Keap1 имеет четыре дискретных белковых домена. N -концевой комплекс Broad, домен Tramtrack и Bric-à-Brac (BTB) содержит остаток Cys151, который является одним из важных цистеинов при чувствительности к стрессу. Домен промежуточной области (IVR) содержит два критических остатка цистеина, Cys273 и Cys288, которые представляют собой вторую группу цистеинов, важных для восприятия стресса. Двойной глициновый повтор (DGR) и домены C-концевой области взаимодействуют, образуя структуру β-пропеллера , в которой Keap1 взаимодействует с Nrf2 .
Взаимодействия
[ редактировать ]
Было показано, что Keap1 взаимодействует с Nrf2 , главным регулятором антиоксидантной реакции, который важен для уменьшения окислительного стресса . [ 6 ] [ 7 ] [ 8 ]
В условиях покоя Nrf2 закрепляется в цитоплазме посредством связывания с Keap1, что, в свою очередь, облегчает и последующий протеолиз Nrf2 убиквитинирование . Такая секвестрация и дальнейшая деградация Nrf2 в цитоплазме являются механизмами репрессивного воздействия Keap1 на Nrf2 . Keap1 является не только геном- супрессором опухоли , но и геном- супрессором метастазирования . [ 9 ]
Недавно несколько интересных исследований также выявили скрытую цепь в правилах NRF2. В мышином гене Keap1 (INrf2) Lee et al. [ 10 ] обнаружили, что ARE, расположенные на отрицательной цепи, могут тонко связывать активацию Nrf2 с транскрипцией Keap1. Изучая заселенность NRF2 в лимфоцитах человека, Чорли и его коллеги определили, что локус размером примерно 700 п.о. в области промотора KEAP1 постоянно имеет верхний ранг, даже в масштабе всего генома. [ 11 ] Эти основные результаты отражают взаимовлияние между NRF2 и KEAP1. NRF2-управляемая экспрессия KEAP1, характерная для рака человека, особенно для плоскоклеточного рака человека, [ 12 ] описали новую перспективу в понимании регуляции передачи сигналов NRF2.
Как мишень для наркотиков
[ редактировать ]Поскольку активация Nrf2 приводит к скоординированному антиоксидантному и противовоспалительному ответу, а Keap1 подавляет активацию Nrf2 , Keap1 стал очень привлекательной мишенью для лекарств. [ 13 ] [ 14 ] [ 15 ] [ 16 ]
Ряд синтетических олеан- тритерпеноидных соединений, известных как антиоксидантные модуляторы воспаления (AIM), разрабатываются компанией Reata Pharmaceuticals, Inc. и являются мощными индукторами пути Keap1- Nrf2 , блокируя Keap1-зависимое убиквитинирование Nrf2 и приводя к стабилизации и ядерной транслокации Nrf2 и последующей индукции генов-мишеней Nrf2. [ нужна ссылка ] Ведущее соединение в этой серии, бардоксолон метил (также известный как CDDO-Me или RTA 402), находилось на поздней стадии клинических исследований по лечению хронической болезни почек (ХБП) у пациентов с сахарным диабетом 2 типа и продемонстрировало способность улучшить показатели функции почек у этих пациентов. [ нужна ссылка ] Однако исследование фазы 3 было остановлено из соображений безопасности.
Здоровье человека
[ редактировать ]Мутации в KEAP1 , которые приводят к потере функции, не связаны с семейным раком, хотя они действительно предрасполагают людей к многоузловому зобу . Предполагаемый механизм, приводящий к образованию зоба, заключается в том, что окислительно-восстановительный возникающий, когда щитовидная железа вырабатывает гормоны, приводит к потере гетерозиготности KEAP1 стресс , , что приводит к зобу. [ 17 ]
Галерея
[ редактировать ]-
(а) белковые домены NRF2 и KEAP1; (б) KEAP1 гомодимеризуется через домен BTB, а через домены Кельха KEAP1 взаимодействует с NRF2 по мотивам ETGE и DLG. [ 17 ]
-
Связь пути NRF2/KEAP1 с клеточным метаболизмом [ 17 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с GRCh38: Ensembl, выпуск 89: ENSG00000079999 – Ensembl , май 2017 г.
- ^ Перейти обратно: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000003308 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ген Энтрез: KEAP1 kelch-подобный ECH-ассоциированный белок 1» .
- ^ Куллинан С.Б., Чжан Д., Ханнинк М., Арвисайс Э., Кауфман Р.Дж., Диль Дж.А. (октябрь 2003 г.). «Nrf2 является прямым субстратом PERK и эффектором PERK-зависимого выживания клеток» . Молекулярная и клеточная биология . 23 (20): 7198–209. дои : 10.1128/mcb.23.20.7198-7209.2003 . ПМК 230321 . ПМИД 14517290 .
- ^ Шибата Т., Охта Т., Тонг К.И., Кокубу А., Одогава Р., Цута К. и др. (сентябрь 2008 г.). «Связанные с раком мутации в NRF2 нарушают его распознавание лигазой E3 Keap1-Cul3 и способствуют злокачественному развитию» . Труды Национальной академии наук Соединенных Штатов Америки . 105 (36): 13568–73. Бибкод : 2008PNAS..10513568S . дои : 10.1073/pnas.0806268105 . ПМЦ 2533230 . ПМИД 18757741 .
- ^ Ван XJ, Сунь Z, Чен В, Ли Ю, Вильнёв Н.Ф., Чжан Д.Д. (август 2008 г.). «Активация Nrf2 арсенитом и монометиларсоновой кислотой не зависит от Keap1-C151: усиление взаимодействия Keap1-Cul3» . Токсикология и прикладная фармакология . 230 (3): 383–9. дои : 10.1016/j.taap.2008.03.003 . ПМК 2610481 . ПМИД 18417180 .
- ^ Лигнитто Л., ЛеБёф С.Е., Гомер Х., Цзян С., Аскенази М., Каракуси Т.Р. и др. (июль 2019 г.). «Активация Nrf2 способствует метастазированию рака легких, подавляя деградацию Bach1» . Клетка . 178 (2): 316–329.e18. дои : 10.1016/j.cell.2019.06.003 . ПМК 6625921 . ПМИД 31257023 .
- ^ Ли ОХ, Джайн А.К., Папуша В., Джайсвал А.К. (декабрь 2007 г.). «Петля авторегуляции между датчиками стресса INrf2 и Nrf2 контролирует численность их клеток» . Журнал биологической химии . 282 (50): 36412–20. дои : 10.1074/jbc.M706517200 . ПМИД 17925401 .
- ^ Чорли Б.Н., Кэмпбелл М.Р., Ван Х, Карача М., Самбандан Д., Бангура Ф. и др. (август 2012 г.). «Идентификация новых генов, регулируемых NRF2, с помощью ChIP-Seq: влияние на альфа-рецептор ретиноида X» . Исследования нуклеиновых кислот . 40 (15): 7416–29. дои : 10.1093/nar/gks409 . ПМЦ 3424561 . ПМИД 22581777 .
- ^ Тянь Ю, Лю Ц, Ю С, Чу Ц, Чэнь Ю, Ву К, Ван Л (октябрь 2020 г.). «NRF2-управляемая транскрипция KEAP1 при раке легких человека» . Молекулярные исследования рака . 18 (10): 1465–1476. дои : 10.1158/1541-7786.MCR-20-0108 . ПМИД 32571982 . S2CID 219989242 .
- ^ Абед Д.А., Гольдштейн М., Албаньян Х., Джин Х., Ху Л. (июль 2015 г.). «Открытие прямых ингибиторов белок-белкового взаимодействия Keap1-Nrf2 как потенциальных терапевтических и профилактических средств» . Акта Фармацевтика Синика Б. 5 (4): 285–99. дои : 10.1016/j.apsb.2015.05.008 . ПМЦ 4629420 . ПМИД 26579458 .
- ^ Лу MC, Цзи JA, Цзян ZY, Ю QD (сентябрь 2016 г.). «Путь Keap1-Nrf2-ARE как потенциальная профилактическая и терапевтическая цель: обновленная информация». Обзоры медицинских исследований . 36 (5): 924–63. дои : 10.1002/мед.21396 . ПМИД 27192495 . S2CID 30047975 .
- ^ Дешмукх П., Унни С., Кришнаппа Г., Падманабхан Б. (февраль 2017 г.). «Путь Keap1-Nrf2: многообещающая терапевтическая мишень для противодействия АФК-опосредованному повреждению при раке и нейродегенеративных заболеваниях» . Биофизические обзоры . 9 (1): 41–56. дои : 10.1007/s12551-016-0244-4 . ПМЦ 5425799 . ПМИД 28510041 .
- ^ Керр Ф., Софола-Адесакин О., Иванов Д.К., Гатлифф Дж., Гомес Перес-Ниевас Б., Бертран Х.К. и др. (март 2017 г.). «Прямое нарушение Keap1-Nrf2 как потенциальная терапевтическая мишень при болезни Альцгеймера» . ПЛОС Генетика . 13 (3): e1006593. дои : 10.1371/journal.pgen.1006593 . ПМК 5333801 . ПМИД 28253260 .
- ^ Перейти обратно: а б с Ву В.Л., Папагианнакопулос Т. (09.03.2020). «Плейотропная роль пути KEAP1/NRF2 при раке» . Ежегодный обзор биологии рака . 4 (1): 413–435. doi : 10.1146/annurev-cancerbio-030518-055627 . ISSN 2472-3428 .
Дальнейшее чтение
[ редактировать ]- Чжан Д.Д. (2007). «Механистические исследования сигнального пути Nrf2-Keap1». Обзоры метаболизма лекарств . 38 (4): 769–89. CiteSeerX 10.1.1.600.2452 . дои : 10.1080/03602530600971974 . ПМИД 17145701 . S2CID 7627379 .
- Нагасе Т., Секи Н., Танака А., Исикава К., Номура Н. (август 1995 г.). «Прогнозирование кодирующих последовательностей неопознанных генов человека. IV. Кодирующие последовательности 40 новых генов (KIAA0121-KIAA0160), выведенные путем анализа клонов кДНК из линии клеток человека KG-1» . Исследование ДНК . 2 (4): 167–74, 199–210. дои : 10.1093/dnares/2.4.167 . ПМИД 8590280 .
- Ито К., Вакабаяши Н., Като Й., Исии Т., Игараси К., Энгель Дж.Д., Ямамото М. (январь 1999 г.). «Keap1 подавляет ядерную активацию элементов, чувствительных к антиоксидантам, с помощью Nrf2 посредством связывания с аминоконцевым доменом Neh2» . Гены и развитие . 13 (1): 76–86. дои : 10.1101/gad.13.1.76 . ПМК 316370 . ПМИД 9887101 .
- Дакшинамурти С., Джайсвал А.К. (июнь 2001 г.). «Функциональная характеристика и роль INrf2 в экспрессии, опосредованной элементом антиоксидантного ответа, и антиоксидантной индукции гена NAD(P)H:хиноноксидоредуктазы1» . Онкоген . 20 (29): 3906–17. дои : 10.1038/sj.onc.1204506 . ПМИД 11439354 .
- Сехар К.Р., Шпитц Д.Р., Харрис С., Нгуен Т.Т., Мередит М.Дж., Холт Дж.Т. и др. (апрель 2002 г.). «Окислительно-чувствительное взаимодействие между KIAA0132 и Nrf2 опосредует индуцированную индометацином экспрессию гамма-глутамилцистеинсинтетазы». Свободно-радикальная биология и медицина . 32 (7): 650–62. дои : 10.1016/S0891-5849(02)00755-4 . ПМИД 11909699 .
- Величкова М., Гуттман Дж., Уоррен С., Энг Л., Клайн К., Фогль А.В., Хэссон Т. (март 2002 г.). «Человеческий гомолог Drosophila kelch связывается с миозином-VIIa в специализированных адгезионных соединениях» . Подвижность клеток и цитоскелет . 51 (3): 147–64. дои : 10.1002/см.10025 . ПМИД 11921171 .
- Зиппер Л.М., Малкахи RT (сентябрь 2002 г.). «Функция димеризации Keap1 BTB/POZ необходима для секвестрации Nrf2 в цитоплазме» . Журнал биологической химии . 277 (39): 36544–52. дои : 10.1074/jbc.M206530200 . ПМИД 12145307 .
- Сехар К.Р., Ян XX, Фриман М.Л. (октябрь 2002 г.). «Деградация Nrf2 по протеасомному пути убиквитина ингибируется KIAA0132, человеческим гомологом INrf2» . Онкоген . 21 (44): 6829–34. дои : 10.1038/sj.onc.1205905 . ПМИД 12360409 .
- Блум Д.А., Джайсвал А.К. (ноябрь 2003 г.). «Фосфорилирование Nrf2 по Ser40 протеинкиназой C в ответ на антиоксиданты приводит к высвобождению Nrf2 из INrf2, но не требуется для стабилизации/накопления Nrf2 в ядре и активации транскрипции опосредованного элементом антиоксидантного ответа NAD(P)H: Экспрессия гена хиноноксидоредуктазы-1» . Журнал биологической химии . 278 (45): 44675–82. дои : 10.1074/jbc.M307633200 . ПМИД 12947090 .
- Куллинан С.Б., Чжан Д., Ханнинк М., Арвисайс Э., Кауфман Р.Дж., Диль Дж.А. (октябрь 2003 г.). «Nrf2 является прямым субстратом PERK и эффектором PERK-зависимого выживания клеток» . Молекулярная и клеточная биология . 23 (20): 7198–209. дои : 10.1128/MCB.23.20.7198-7209.2003 . ПМК 230321 . ПМИД 14517290 .
- Колланд Ф., Жак Икс, Труплен В., Мужен С., Гроазело С., Гамбургер А. и др. (июль 2004 г.). «Функциональное протеомное картирование сигнального пути человека» . Геномные исследования . 14 (7): 1324–32. дои : 10.1101/гр.2334104 . ПМК 442148 . ПМИД 15231748 .
- Кобаяши А., Кан М.И., Окава Х., Оцудзи М., Зенке Ю., Чиба Т. и др. (август 2004 г.). «Датчик окислительного стресса Keap1 действует как адаптер для лигазы E3 на основе Cul3, регулируя протеасомную деградацию Nrf2» . Молекулярная и клеточная биология . 24 (16): 7130–9. дои : 10.1128/MCB.24.16.7130-7139.2004 . ПМЦ 479737 . ПМИД 15282312 .
- Страчан Г.Д., Морган К.Л., Отис Л.Л., Кальтагароне Дж., Гиттис А., Баузер Р., Джордан-Скиутто К.Л. (сентябрь 2004 г.). «Фетальный клон Alz-50 1 взаимодействует с человеческим ортологом Kelch-подобного Ech-ассоциированного белка» . Биохимия . 43 (38): 12113–22. дои : 10.1021/bi0494166 . ПМК 3670950 . ПМИД 15379550 .
- Ли X, Чжан Д., Ханнинк М., Бимер Л.Дж. (декабрь 2004 г.). «Кристаллическая структура домена Кельха человека Keap1» . Журнал биологической химии . 279 (52): 54750–8. дои : 10.1074/jbc.M410073200 . ПМИД 15475350 .
- Чжан Д.Д., Ло С.К., Cross JV, Templeton DJ, Hannink M (декабрь 2004 г.). «Keap1 представляет собой редокс-регулируемый субстратный адаптерный белок для Cul3-зависимого комплекса убиквитинлигазы» . Молекулярная и клеточная биология . 24 (24): 10941–53. дои : 10.1128/MCB.24.24.10941-10953.2004 . ПМЦ 533977 . ПМИД 15572695 .
- Ли X, Чжан Д., Ханнинк М., Бимер Л.Дж. (декабрь 2004 г.). «Кристаллизация и первоначальный кристаллографический анализ домена Кельха человека Keap1». Акта Кристаллографика. Раздел D. Биологическая кристаллография . 60 (Часть 12, Часть 2): 2346–8. Бибкод : 2004AcCrD..60.2346L . CiteSeerX 10.1.1.631.1273 . дои : 10.1107/S0907444904024825 . ПМИД 15583386 .
- Фурукава М., Сюн Ю. (январь 2005 г.). «Белок BTB Keap1 нацелен на антиоксидантный фактор транскрипции Nrf2 для убиквитинирования лигазой Cullin 3-Roc1» . Молекулярная и клеточная биология . 25 (1): 162–71. дои : 10.1128/MCB.25.1.162-171.2005 . ПМК 538799 . ПМИД 15601839 .
- Хосоя Т., Маруяма А., Кан М.И., Каватани Ю., Сибата Т., Учида К. и др. (июль 2005 г.). «Дифференциальные реакции системы Nrf2-Keap1 на ламинарные и колебательные напряжения сдвига в эндотелиальных клетках» . Журнал биологической химии . 280 (29): 27244–50. дои : 10.1074/jbc.M502551200 . ПМИД 15917255 .





![(а) белковые домены NRF2 и KEAP1; (б) KEAP1 гомодимеризуется через домен BTB, а через домены Кельха KEAP1 взаимодействует с NRF2 по мотивам ETGE и DLG[17]](http://upload.wikimedia.org/wikipedia/commons/thumb/2/28/KEAP1_NRF2_signaling_pathway.jpg/370px-KEAP1_NRF2_signaling_pathway.jpg)
![Связь пути NRF2/KEAP1 с клеточным метаболизмом[17]](http://upload.wikimedia.org/wikipedia/commons/thumb/e/e0/KEAP1_and_NRF2_interacting_with_cellular_metabolism.jpg/355px-KEAP1_and_NRF2_interacting_with_cellular_metabolism.jpg)