Связь металл-металл

В неорганической химии связи металл-металл описывают притягивающие взаимодействия между металлоцентрами. Простейшие примеры встречаются в биметаллических комплексах. Связи металл-металл могут быть «поддержанными», т. е. сопровождаться одним или несколькими мостиковыми лигандами , или «неподдержанными». Они также могут различаться в зависимости от порядка облигаций. Тема связи металл-металл обычно обсуждается в рамках координационной химии . [1] но эта тема связана с расширенной металлической связью , которая описывает взаимодействия между металлами в протяженных твердых телах, таких как объемные металлы и субгалогениды металлов. [2]
Необеспеченные связи металл-металл
[ редактировать ]Пример связи металл-металл находится в декакарбониле димарганца , Mn 2 (CO) 10 . Как подтверждено методом рентгеновской кристаллографии , пара звеньев Mn(CO) 5 связана связью между атомами Mn. Расстояние Мн-Мн (290 м .) небольшое. [3] Mn 2 (CO) 10 представляет собой простой и понятный случай связи металл-металл, поскольку никакие другие атомы не связывают два атома Mn вместе.
Когда несколько металлов связаны связями металл-металл, соединение или ион называется металлическим кластером . Многие металлические кластеры содержат несколько незакрепленных связей М–М. Некоторыми примерами являются M 3 (CO) 12 (M = Ru, Os) и Ir 4 (CO) 12 .
Подклассом неподдерживаемых массивов металл-металл являются линейные цепные соединения . В таких случаях связь М-М слабая, о чем свидетельствуют более длинные связи М-М и склонность таких соединений к диссоциации в растворе.
Поддерживаемые связи металл-металл
[ редактировать ]Во многих соединениях связи металл-металл сопровождаются мостиковыми лигандами . В таких случаях трудно однозначно утверждать, что связь металл-металл представляет собой силу сцепления, связывающую два металла вместе. дижелезононакарбонил Одним из таких примеров является . Другим примером закрепленной связи металл-металл является димер циклопентадиенилирондикарбонила железа , [(C 5 H 5 )Fe(CO) 2 ] 2 . В преобладающих изомерах этого комплекса два Fe-центра соединены не только связью Fe–Fe, но и мостиковыми лигандами CO . Родственный димер циклопентадиенилрутения имеет незакрепленную связь Ru-Ru. Многие металлические кластеры содержат несколько закрепленных связей М–М. Другими примерами являются Fe 3 (CO) 12 и Co 4 (CO) 12 .
Множественные связи металл-металл
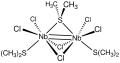
[ редактировать ]- Nb 2 Cl 6 (SMe 2 ) 3 , имеющий двойную связь металл-металл.
- Гекса( трет- бутокси)вольфрам(III) с тройной связью W – W.
- Ацетат хрома (II) с четверной связью металл-металл.
- [Ru 2 (OAc) 4 Cl] n , где порядок связи металл–металл равен 2,5.
Помимо одинарных связей М–М, пары металлов могут быть соединены двойными, тройными, четверными и в некоторых случаях пятикратными связями . [4] Изолируемые комплексы с кратными связями наиболее распространены среди переходных металлов в середине d-блока , таких как рений , вольфрам , технеций , молибден и хром . Типичными ко- лигандами являются π-доноры, а не π-акцепторы. [5] Хорошо изученными примерами являются тетраацетаты , такие как тетраацетат димолибдена (четверная связь) и тетраацетат диродия (одинарная связь). Тетраацетаты друтения смешанной валентности имеют дробный порядок связи М–М, т.е. 2,5 для [Ru 2 (OAc) 4 (H 2 O) 2 ] + . [6]
Комплексы Nb 2 X 6 (SR 2 ) 3 принимают биооктаэдрическую структуру с общими гранями (X = Cl, Br; SR 2 = тиоэфир). Как димеры Nb(III), они имеют двойные связи металл-металл, максимально возможные для пары металлов с d 2 конфигурация. [7] Гекса( трет -бутокси)дивольфрам(III) является хорошо изученным примером комплекса с тройной связью металл-металл. [8]
Ссылки
[ редактировать ]- ^ Берри, Джон Ф.; Лу, Конни С. (2017). «Металл-металлические облигации: от основ к применению» . Неорганическая химия . 56 (14): 7577–7581. doi : 10.1021/acs.inorgchem.7b01330 . ПМИД 28715854 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8 .
- ^ Даль, Л.Ф.; Рандл, RE (10 мая 1963 г.). «Кристаллическая структура димарганцевого декакарбонила Mn 2 (CO) 10 » . Акта Кристаллографика . 16 (5): 419–426. дои : 10.1107/S0365110X63001080 . ISSN 0365-110X .
- ^ Радиус, У.; Бреер, Ф. (2006). « Смело преодолеть четверную связь металл-металл». Энджью. хим. Межд. Эд. 45 (19): 3006–3010. дои : 10.1002/anie.200504322 . ПМИД 16642513 .
- ^ Коттон, ФА; Уолтон, РА (1993). Множественные связи между атомами металлов . Оксфорд: Издательство Оксфордского университета . ISBN 0-19-855649-7 .
- ^ Акино, Мануэль А.С. (1998). «Тетракарбоксилаты дирутения и диосмия: синтез, физические свойства и применение». Обзоры координационной химии . 170 : 141–202. дои : 10.1016/S0010-8545(97)00079-9 .
- ^ Какея, Масаки; Фудзихара, Такаши; Нагасава, Акира (2006). «Ди-μ-хлор-μ-(диметилсульфид)-бис[дихлор(диметилсульфид)ниобий(III)]». Acta Crystallographica Раздел E. 62 (3): м553–м554. дои : 10.1107/S1600536806005149 .
- ^ Бродерик, Эрин М.; Браун, Сэмюэл К.; Джонсон, Марк Дж.А. (2014). «Димолибден и дивольфрам гекса (алкоксиды)». Неорганические синтезы: Том 36 . Том. 36. С. 95–102. дои : 10.1002/9781118744994.ch18 . ISBN 9781118744994 .
![[Ru2(OAc)4Cl]n, где порядок связи металл–металл равен 2,5.](http://upload.wikimedia.org/wikipedia/commons/thumb/5/50/Ru2%28OAc%294Cl.svg/120px-Ru2%28OAc%294Cl.svg.png)