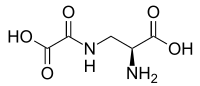
Оксалилдиаминопропионовая кислота
| |
| Имена | |
|---|---|
| Систематическое название ИЮПАК
(2 S )-2-амино-3-(оксалоамино)пропановая кислота | |
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 3DMeet | |
| Сокращения |
|
| КЭБ | |
| ХимическийПаук | |
| КЕГГ | |
| МеШ | оксалилдиаминопропионовая+кислота |
ПабХим CID
|
|
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 5 Н 8 Н 2 О 5 | |
| Молярная масса | 176.128 g·mol −1 |
| Родственные соединения | |
Родственные соединения
|
Бета-метиламино-L-аланин |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Оксалилдиаминопропионовая кислота ( ОДАП ) является структурным аналогом нейромедиатора обнаруженного глутамата, в горохе Lathyrus sativus . Это нейротоксин, синдром дегенерации двигательных нейронов ответственный за латиризм, . [ 1 ]
Источники
[ редактировать ]ODAP обнаруживается в семенах бобовых L. sativus , растения гороха, в пределах 0,5% по весу. [ 2 ] L. sativus можно найти в районах Южной, Центральной и Восточной Европы, Средиземноморского бассейна, Ирака и Афганистана, а также в районах Азии и Африки. [ 3 ]
История
[ редактировать ]В некоторых регионах, включая Индийский субконтинент, Бангладеш, Эфиопию и Непал, горох стал основным продуктом питания. [ 3 ] Растение обладает высокой устойчивостью к условиям окружающей среды, что делает его единственным доступным источником пищи во времена голода или засухи. После нескольких месяцев засухи могут возникнуть эпидемии нейролатиризма. [ 4 ] Последний случай такой эпидемии (по состоянию на 2013 год) был в Эфиопии во время засухи 1995-1997 годов. [ 5 ] в течение которого 2000 человек стали инвалидами. [ 3 ]
Биологические эффекты
[ редактировать ]является агонистом ионотропных ОДАП [ 6 ] Глутаматный рецептор АМРА . [ 5 ] Известно, что он вызывает у людей нейролатиризм — дегенеративное заболевание двигательных нейронов, характеризующееся дегенерацией нейронов пирамидных путей в спинном мозге и в области коры головного мозга, контролирующей ноги, что приводит к параличу нижней части тела. [ 6 ] Не существует одного прямого объяснения того, как ODAP вызывает нейролатиризм; однако были доказательства, подтверждающие некоторые биологические эффекты. Одной из причин, по которой механизм действия не совсем ясен, может быть то, что до сих пор не найдена хорошая животная модель воздействия ODAP на человека. [ 5 ] LD также 50 неизвестен.
Эксайтотоксичность
[ редактировать ]ODAP активирует рецепторы AMPA, которые могут вызывать эксайтотоксичность или чрезмерную стимуляцию рецепторов глутамата. Высвобождение слишком большого количества глютамата сразу или в течение длительного периода времени приведет к повышению уровня кальция. 2+
в цитоплазме. Поскольку Ка 2+
является сигнальным ионом высвобождения глутамата в синапс, это может привести к потенцированию цикла высвобождения глутамата и распространению экситотоксического повреждения на соседние нейроны. Внутри нейрона дополнительный Ca 2+
покинет цитоплазму и попадет либо в митохондрии , либо в эндоплазматический ретикулум (ЭР), что может привести к накоплению неправильно свернутых или развернутых белков в ЭР и, в конечном итоге, к гибели клеток в обоих случаях. Помимо действия в качестве агониста, есть данные, показывающие, что ODAP транспортируется в клетку с помощью антипортера , который одновременно транспортирует глутамат в синапс. [ 6 ]
Окислительный стресс
[ редактировать ]Вторым биологическим эффектом ODAP является окислительный стресс . Активные формы кислорода (АФК) генерируются в митохондриях во время метаболизма, и в организме есть механизмы нейтрализации этих молекул, прежде чем они нанесут ущерб. Окислительный стресс возникает в результате нарушения нормального функционирования этих путей. Одним из антиоксидантов пути нейтрализации является глутатион (GSH), для синтеза которого требуются серосодержащие аминокислоты метионин и цистеин в качестве предшественников. Считается, что ODAP, возможно, вследствие индуцированной эксайтотоксичности, снижает поступление цистеина через его антипортер . Это ингибирует синтез GSH, что приводит к увеличению производства АФК и повреждению митохондрий. Мотонейроны могут быть наиболее чувствительны к отравлению ODAP, поскольку они проявляют большую зависимость от метионина, предшественника GSH. Кроме того, L. sativus в качестве пищи имеет дефицит серосодержащих аминокислот, что усиливает воздействие ODAP на уровне рецепторов на выработку GSH при приеме внутрь. [ 6 ]
Синтез
[ редактировать ]Биосинтез
[ редактировать ]У L. sativus ODAP синтезируется в молодых проростках из предшественника (β-изоксазолин-5-он-2-ил)аланина, также известного как BIA. BIA не был обнаружен в зрелых частях растений и созревающих семенах. Путь начинается с образования БИА из О-ацетил-L-серина (ОАС) и изоксазолин-5-она. Раскрытие кольца приводит к образованию короткоживущего промежуточного продукта 2,3-L-диаминопропановой кислоты (DAPRO), который затем оксалилизируется оксалилкоферментом А с образованием ODAP. [ 7 ]

Химический синтез
[ редактировать ]ОДАП можно синтезировать из L-α,β-диаминопропионовой кислоты и диметилоксалата при pH 4,5–5. Оксид меди можно использовать для временной защиты группы α-NH2 L-α,β-диаминопропионовой кислоты во время реакции. [ 2 ]

См. также
[ редактировать ]- β-Метиламино- L -аланин , родственный токсин
Ссылки
[ редактировать ]- ^ Jump up to: а б Вольдеамануэль, Йоханнес В.; Хасан, Анхар; Зенебе, Гута (12 ноября 2011 г.). «Нейролатиризм: два сообщения о случаях заболевания в Эфиопии и обзор литературы» . Журнал неврологии . 259 (7): 1263–1268. дои : 10.1007/s00415-011-6306-4 . ISSN 0340-5354 . ПМИД 22081101 . S2CID 27543906 .
- ^ Jump up to: а б Рао, С; Адига, П; Сарма, П. (март 1964 г.). «Выделение и характеристика β-N-оксалил-L-α,β-диаминопропионовой кислоты: нейротоксина из семян Lathyrus sativus». Биохимия . 3 (3): 432–436. дои : 10.1021/bi00891a022 . ПМИД 14155110 .
- ^ Jump up to: а б с 2016. Горох посевной (Lathyrus sativus). Feedpedia, программа INRA, CIRAD, AFZ и ФАО. 3 Последнее обновление 19 апреля 2016, 15:
- ^ «Исследования Латираса» . Университет Гента . Архивировано из оригинала 16 апреля 2015 года . Проверено 8 апреля 2015 г.
- ^ Jump up to: а б с Сингх, С; Рао, С. (июль 2013 г.). «Уроки нейролатиризма: болезнь прошлого и будущего Lathyrus sativus (Khesari dal)» . Индийский журнал медицинских исследований . 138 (1): 32–37. ПМЦ 3767245 . ПМИД 24056554 .
- ^ Jump up to: а б с д Мурхем, М; Ламбейн, Ф; Лайберт, Л. (март 2011 г.). «Раскрытие механизма эксайтотоксичности и окислительного стресса, вызываемого β-N-оксалил-α,β-диаминопропионовой кислотой (β-ODAP), актуальность для профилактики нейролатиризма». Пищевая и химическая токсикология . 49 (3): 550–555. дои : 10.1016/j.fct.2010.03.054 . ПМИД 20510327 .
- ^ Куо, Ю; Хан, Дж; Ламбейн, Ф (март 1994 г.). «Биосинтез нейротоксина β-одап в развивающихся стручках Lathyrus sativus». Фитохимия . 35 (4): 911–913. Бибкод : 1994PChem..35..911K . дои : 10.1016/s0031-9422(00)90637-x .