Невинный лиганд
В химии (окислительно-восстановительный) неиннокентный лиганд — это лиганд в металлокомплексе , степень окисления которого не определена. прозрачный. Обычно комплексы, содержащие невинные лиганды, проявляют окислительно-восстановительную активность при умеренных потенциалах . Эта концепция предполагает, что окислительно-восстановительные реакции в металлокомплексах локализованы либо в металле, либо в лиганде, что является упрощением, хотя и полезным. [ 1 ]
К. К. Йоргенсен впервые описал лиганды как «невинные» и «подозрительные»: «Лиганды безвредны, если они позволяют определить степени окисления центральных атомов. Простейший случай подозрительного лиганда — NO …» [ 2 ]
Окислительно-восстановительные реакции комплексов невинных и невинных лигандов
[ редактировать ]Обычно окислительно-восстановительные реакции координационных комплексов считают металлоцентрическими. Восстановление MnO 4 − до MnO 4 2− описывается изменением степени окисления марганца от 7+ до 6+. Оксидные . лиганды не меняют степень окисления, оставаясь 2- [ 3 ] Оксид – невинный лиганд. Другим примером традиционной металлоцентрированной окислительно- восстановительной пары является [Со(NH 3 ) 6 ] 3+ /[Co(NH 3 ) 6 ] 2+ . Аммиак невиновен в этом превращении.
Редокс-неинвинентное поведение лигандов иллюстрируется бис(стильбендитиолатом) никеля ([Ni(S 2 C 2 Ph 2 ) 2 ] С ). Поскольку все бис(1,2-дитиоленовые) комплексы n d 8 ионов металлов можно выделить три степени окисления : z = 2-, 1- и 0. Если лиганды всегда считать дианионными (как это делается при формальном подсчете степеней окисления), то z = 0 требует, чтобы этот никель имел формальная степень окисления +IV. Таким образом, формальная степень окисления центрального атома никеля в указанных выше превращениях находится в диапазоне от +II до +IV (см. рисунок). Однако формальная степень окисления отличается от реальной (спектроскопической) степени окисления, основанной на (спектроскопической) конфигурации d-электронов металла. Стильбен-1,2-дитиолат ведет себя как окислительно-восстановительный неиннокентный лиганд, и процессы окисления фактически происходят на лигандах, а не на металле. Это приводит к образованию лиганд-радикальных комплексов. Зарядно-нейтральный комплекс (z = 0), демонстрирующий частичный синглетный дирадикальный характер, [ 4 ] поэтому лучше описать как Ni 2+ производное аниона-радикала S 2 C 2 Ph 2 •− . Диамагнетизм этого комплекса возникает в результате антиферромагнитной связи между неспаренными электронами двух лиганд-радикалов. Другой пример — высшие степени окисления медных комплексов диамидофенильных лигандов, стабилизированных внутримолекулярной многоцентровой водородной связью. [ 5 ]
Типичные невинные лиганды
[ редактировать ]- Нитрозил (NO) связывается с металлами в одной из двух крайних геометрий - изогнутой, где NO рассматривается как псевдогалогенид (NO − ) и линейный, где NO рассматривается как NO + .
- Дикислород может быть невинным, так как он существует в двух степенях окисления: супероксид (O 2 − ) и пероксид (O 2 2− ). [ 6 ]
Лиганды с расширенной пи-делокализацией, такие как порфирины , фталоцианины и корролы. [ 7 ] и лиганды с обобщенными формулами [D-CR=CR-D] п- (D = O, S, NR' и R, R' = алкил или арил ) часто небезопасны. Напротив, [D-CR=CR-CR=D] − такие как NacNac или Acac, невиновны.
- катехолаты и родственные 1,2-диоксалены. [ 8 ]
- дитиолены , такие как малеонитрилдитиолат (см. пример [Ni(S 2 C 2 Ph 2 ) 2 ] п- выше).
- 1,2- диимины, такие как производные 1,2-диамидобензола, 2,2'-бипиридина и диметилглиоксима . Комплекс Cr( 2,2'-бипиридин ) 3 представляет собой производное Cr(III), связанное с тремя бипиридинами. 1− лиганды. С другой стороны, одноэлектронное окисление [Ru(2,2'-бипиридин) 3 ] 2+ локализован на Ru, и бипиридин в этом случае ведет себя как нормальный, невинный лиганд.
- лиганды, содержащие ферроцен, могут иметь события окисления, сосредоточенные на ферроценовом железном центре, а не на каталитически активном металлическом центре. [ 9 ]
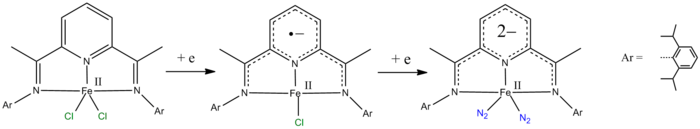
- пиридин-2,6-дииминовые лиганды могут восстанавливаться на один и два электрона. [ 10 ] [ 11 ]
Редокс-неиннокентные лиганды в биологии и гомогенном катализе
[ редактировать ]В некоторых ферментативных процессах окислительно-восстановительные невинные кофакторы обеспечивают окислительно-восстановительные эквиваленты, дополняющие окислительно-восстановительные свойства металлоферментов. Конечно, в большинстве окислительно-восстановительных реакций в природе участвуют невинные системы, например кластеры [4Fe-4S] . Дополнительные окислительно-восстановительные эквиваленты, обеспечиваемые окислительно-восстановительными невинными лигандами, также используются в качестве контролирующих факторов для управления гомогенным катализом. [ 12 ] [ 13 ] [ 14 ]
Гемы
[ редактировать ]
Порфириновые лиганды могут быть безвредными (2-) и неиннокентными (1-). В ферментах хлорпероксидазе и цитохроме P450 порфириновый лиганд поддерживает окисление во время каталитического цикла, особенно при образовании I. Соединения В других гемовых белках, таких как миоглобин , лиганд-центрированного окислительно-восстановительного процесса не происходит, и порфирин невиновен.
Галактозооксидаза
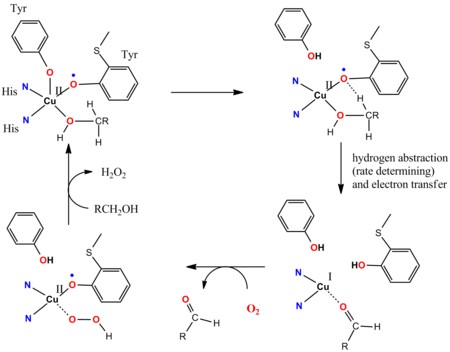
[ редактировать ]Каталитический цикл галактозооксидазы (GOase) иллюстрирует участие невинных лигандов. [ 15 ] [ 16 ] GOase окисляет первичные спирты в альдегиды с помощью O 2 и высвобождения H 2 O 2 . Активный центр фермента ГОазы содержит тирозил, координированный с Cu. II ион. На ключевых этапах каталитического цикла совместный центр лиганда Бренстеда-основного лиганда депротонирует спирт, а затем атом кислорода тирозинильного радикала отрывает атом водорода от функциональной группы альфа-СН координированного алкоксидного субстрата. Тирозинильный радикал участвует в каталитическом цикле: 1e-окисление осуществляется парой Cu(II/I), а 1e-окисление осуществляется тирозильным радикалом, что приводит к общему изменению 2e. Радикальная абстракция быстрая. Антиферромагнитная связь между неспаренными спинами тирозинового радикального лиганда и d 9 С II центр приводит к возникновению основного диамагнитного состояния, что согласуется с синтетическими моделями. [ 17 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Гангули, Сумит; Гош, Абхик (16 июля 2019 г.). «Семь ключей к невиновности лигандов: парадигма металлокоррола». Отчеты о химических исследованиях . 52 (7): 2003–2014. дои : 10.1021/acs.accounts.9b00115 . ISSN 0001-4842 . ПМИД 31243969 . S2CID 195695184 .
- ^ Йоргенсен К.К. (1966). «Различия между четырьмя галогенидными лигандами и замечания по обсуждению тригонально-бипирамидальных комплексов, степеней окисления и диагональных элементов с одноэлектронной энергией». Обзоры координационной химии . 1 (1–2): 164–178. дои : 10.1016/S0010-8545(00)80170-8 .
- ^ Хотя более тщательное изучение электронной структуры окислительно-восстановительных партнеров показывает, что окислительно-восстановительное изменение влияет на оксидные лиганды, этот эффект незначителен, и формальная степень окисления кислорода остается прежней.
- ^ Арагони, М. Карла; Кальтаджироне, Клаудия; Липполис, Вито; Подда, Генри; Славин, Александра М.З.; Вуллинз, Дж. Дерек; Пинтус, Анна; Арка, Массимилиано (07.12.2020). «Дирадикальный характер нейтральных гетеролептических бис(1,2-дитиолен)металлических комплексов: пример [Pd(Me2timdt)(mnt)] (Me2timdt = 1,3-диметил-2,4,5-тритиоксоимидазолидин; mnt2– =. " 1,2-дициано-1,2-этилендитиолат)» . Неорганическая химия . 59 (23): 17385–17401. doi : 10.1021/acs.inorgchem.0c02696 . ISSN 0020-1669 . ПМЦ 7735710 . ПМИД 33185438 .
- ^ Раджабимогадам, Хашаяр; Дарвиш, Юсеф; Башир, Умиина; Питман, Дилан; Эйхельбергер, Сидней; Зиглер, Максим А.; Сварт, Марсель; Гарсиа-Бош, Исаак (2018). «Каталитическое аэробное окисление спиртов комплексами меди, несущими редокс-активные лиганды с перестраиваемыми группами водородных связей» . Журнал Американского химического общества . 140 (48): 16625–16634. дои : 10.1021/jacs.8b08748 . ПМК 6645702 . ПМИД 30400740 .
- ^ Каим В., Шведерски Б. (2010). «Невинные лиганды в бионеорганической химии. Обзор». Обзоры координационной химии . 254. (13–14) (13–14): 1580–1588. дои : 10.1016/j.ccr.2010.01.009 .
- ^ Гош, Абхик (22 февраля 2017 г.). «Электронная структура производных корролов: данные молекулярных структур, спектроскопии, электрохимии и квантово-химических расчетов». Химические обзоры . 117 (4): 3798–3881. doi : 10.1021/acs.chemrev.6b00590 . ISSN 0009-2665 . ПМИД 28191934 .
- ^ Занелло П., Корсини М. (2006). «Гомолептические моноядерные комплексы переходных металлов 1,2-диоксоленов: обновление их электрохимических и структурных (рентгеновских) свойств». Обзоры координационной химии . 250 (15–16): 2000–2022 гг. дои : 10.1016/j.ccr.2005.12.017 .
- ^ Ван X, Тевенон А, Бросмер Дж.Л., Ю И, Хан С.И., Мехрходаванди П., Диаконеску П.Л. (август 2014 г.). «Окислительно-восстановительный контроль активности полимеризации с раскрытием кольца металла 4-й группы по отношению к L-лактиду и ε-капролактону» . Дж. Ам. хим. Соц . 136 (32): 11264–7. дои : 10.1021/ja505883u . ПМИД 25062499 . S2CID 22098566 .
- ^ де Брюин Б., Билл Э., Боте Э., Вейгермюллер Т., Вигхардт К. (июнь 2000 г.). «Молекулярное и электронное строение бис(пиридин-2,6-диимин)металлокомплексов [ML2](PF6)n (n = 0, 1, 2, 3; M = Mn, Fe, Co, Ni, Cu, Zn) ". Неорг хим . 39 (13): 2936–47. дои : 10.1021/ic000113j . ПМИД 11232835 .
- ^ Чирик П.Дж., Вигхардт К. (февраль 2010 г.). «Химия. Радикальные лиганды придают благородство катализаторам на основе неблагородных металлов». Наука . 327 (5967): 794–5. дои : 10.1126/science.1183281 . ПМИД 20150476 . S2CID 29393215 .
- ^ Лясковский В, де Брюин Б (2012). «Окислительно-восстановительные невинные лиганды: новые универсальные инструменты для контроля каталитических реакций». АКС-катализ . 2 (2): 270–279. дои : 10.1021/cs200660v .
- ^ Лука О.Р., Крэбтри Р.Х. (февраль 2013 г.). «Окислительно-восстановительные лиганды в катализе». Chem Soc Rev. 42 (4): 1440–59. дои : 10.1039/c2cs35228a . ПМИД 22975722 .
- ^ Кирила, Андрей; Дас, Враджа Гопал; Куйперс, Петрус Ф.; Синха, Вивек; Брюин, Бас де (2018), «Применение стимул-реагирующих и «небезвредных» лигандов в катализе неблагородными металлами», Катализ неблагородных металлов , John Wiley & Sons, Ltd, стр. 1–31, doi : 10.1002/ 9783527699087.ch1 , ISBN 9783527699087 , S2CID 104403649
- ^ Уиттакер М.М., Уиттакер Дж.В. (март 1993 г.). «Взаимодействие лигандов с галактозооксидазой: понимание механизма» . Биофиз. Дж . 64 (3): 762–72. Бибкод : 1993BpJ....64..762W . дои : 10.1016/S0006-3495(93)81437-1 . ПМЦ 1262390 . ПМИД 8386015 .
- ^ Ван Ю, Дюбуа Дж.Л., Хедман Б., Ходжсон К.О., Стэк Т.Д. (январь 1998 г.). «Модели каталитической галактозооксидазы: биомиметическая реакционная способность Cu (II)-феноксильного радикала». Наука . 279 (5350): 537–40. Бибкод : 1998Sci...279..537W . дои : 10.1126/science.279.5350.537 . ПМИД 9438841 .
- ^ Мюллер Дж., Вейхермюллер Т., Билл Э., Хильдебрандт П., Ульд-Мусса Л., Глейзер Т., Вигхардт К. (март 1998 г.). «Почему активная форма галактозооксидазы обладает диамагнитным основным состоянием?». Энджью. хим. Межд. Эд. англ . 37 (5): 616–619. doi : 10.1002/(SICI)1521-3773(19980316)37:5<616::AID-ANIE616>3.0.CO;2-4 . ПМИД 29711069 .
Дальнейшее чтение
[ редактировать ]- Дзик, Висконсин; Чжан, XP; де Брюин, Б. (2011). «Окислительно-восстановительная невиновность карбеновых лигандов: карбеновые радикалы в (каталитическом) образовании CC-связи». Неорганическая химия . 50 (20): 9896–9903. дои : 10.1021/ic200043a . ПМИД 21520926 .
- Бюттнер, Т.; Гейер, Дж.; Фрисон, Г.; Хармер, Дж.; Калле, К.; Швайгер, А.; Шенберг, Х.; Грюцмахер, Х. (2005). «Стабильный аминил-радикальный металлокомплекс». Наука . 307. 307 (5707): 235–238. Бибкод : 2005Sci...307..235B . дои : 10.1126/science.1106070 . ПМИД 15653498 . S2CID 6625217 .
- Хеттершайд, DGH; Кайзер, Дж.; Рейджерс, Э.; Питерс, TPJ; Тьювиссен, С.; Блок, АНЖ; Смитс, JMM; де Гелдер, Р.; де Брюин, Б. (2005). "Они II (этен): металл или углеродный радикал?». Журнал Американского химического общества . 127 (6): 1895–1905. doi : 10.1021/ja0439470 . PMID 15701024 .
- Бланшар, С.; Дерат, Э.; Десаж-Эль Мурр, М.; Фенстербанк, Л. ; Малакрия, М; Мурье-Мансюи, В. (2012). «Неневинные лиганды: новые возможности железного катализа». Европейский журнал неорганической химии . 2012 (3): 376–389. дои : 10.1002/ejic.201100985 .
- Каим, В. (2012). «Сжимающийся мир невинных лигандов: обычные и нетрадиционные окислительно-восстановительные лиганды». Европейский журнал неорганической химии . 2012 (3): 343–348. дои : 10.1002/ejic.201101359 .