Фталоцианин
 | |
 | |
| Имена | |
|---|---|
Другие имена
| |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЭБИ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.008.527 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 32 Ч 18 Н 8 | |
| Молярная масса | 514.552 g·mol −1 |
| Опасности | |
| СГС Маркировка : | |
 [1] [1] | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Фталоцианин ( H 2 Pc крупное ароматическое макроциклическое органическое формулы соединение ) — (C 8 H 4 N 2 ) 4 H 2 и представляет теоретический или специализированный интерес в области химических красителей и фотоэлектричества.
Он состоит из четырех изоиндольных единиц. [а] соединены кольцом атомов азота. (С 8 ЧАС 4 N 2 ) 4 ЧАС 2 = H 2 Pc имеет двумерную геометрию и кольцевую систему, состоящую из 18 π-электронов . Обширная делокализация π-электронов придает молекуле полезные свойства, пригодные для применения в красителях и пигментах. Металлокомплексы производные ПК 2−
, сопряженное основание H 2 Pc ценны в катализе , органических солнечных элементах и фотодинамической терапии .
Характеристики
[ редактировать ]
Фталоцианин и комплексы производных металлов (MPc) склонны к агрегации и, таким образом, имеют низкую растворимость в обычных растворителях. [3] Бензол при 40°С растворяет менее миллиграмма H 2 ПК или CuPc на литр. H 2 Pc и CuPc легко растворяются в серной кислоте за счет протонирования атомов азота, замыкающих пиррольные кольца. Многие фталоцианиновые соединения термически очень стабильны и не плавятся, но могут сублимироваться . CuPc сублимируется при температуре выше 500 °C в инертных газах ( азот , СО 2 ). [4] Замещенные фталоцианиновые комплексы часто имеют гораздо более высокую растворимость. [5] Они менее термически стабильны и часто не поддаются сублимации. Незамещенные фталоцианины сильно поглощают свет в диапазоне от 600 до 700 нм , поэтому эти материалы имеют синий или зеленый цвет. [3] Замещение может сместить поглощение в сторону более длинных волн, меняя цвет с чисто синего на зеленый и бесцветный (когда поглощение находится в ближней инфракрасной области ).
Существует множество производных исходного фталоцианина, в которых либо атомы углерода макроцикла заменены на атомы азота, либо периферийные атомы водорода заменены функциональными группами, такими как галогены , гидроксилы , амины , алкилы , арилы , тиолы , алкокси и нитрозильные группы. Эти модификации позволяют настраивать электрохимические свойства молекулы, такие как длины волн поглощения и излучения, а также проводимость. [6]
История
[ редактировать ]В 1907 году было сообщено о неопознанном синем соединении, ныне известном как фталоцианин. [7] В 1927 году швейцарские исследователи по счастливой случайности обнаружили фталоцианин меди, нафталоцианин меди и октаметилфталоцианин меди при попытке превращения о -дибромбензола в фталонитрил . Они отметили огромную устойчивость этих комплексов, но не дали им дальнейшей характеристики. [8] В том же году фталоцианин железа был обнаружен на предприятии Scottish Dyes в Грейнджмуте , Шотландия (позже ICI ). [9] Лишь в 1934 году сэр Патрик Линстед охарактеризовал химические и структурные свойства фталоцианина железа. [10]
Синтез
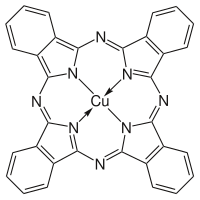
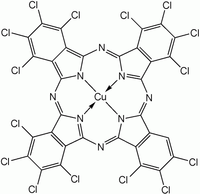
[ редактировать ]Фталоцианин образуется в результате циклотетрамеризации различных производных фталевой кислоты, включая фталонитрил , дииминоизоиндол , фталевый ангидрид и фталимиды . [11] Альтернативно, нагревание фталевого ангидрида в присутствии мочевины дает Н 2 шт . [12] С использованием таких методов в 1985 году было произведено около 57 000 тонн (63 000 британских тонн) различных фталоцианинов. [12] Чаще всего MPc синтезируют, а не H 2 Pc из-за большего исследовательского интереса к первому. Для получения этих комплексов синтез фталоцианинов проводят в присутствии солей металлов. Два фталоцианина меди показаны на рисунке ниже.
Галогенированные и сульфированные производные фталоцианинов меди имеют промышленное значение в качестве красителей. Такие соединения получают CuPc хлором . , бромом или олеумом обработкой
Приложения
[ редактировать ]
При первоначальном открытии ПК его использование в основном ограничивалось красителями и пигментами. [13] Модификация заместителей, присоединенных к периферийным кольцам, позволяет регулировать поглощательные и эмиссионные свойства Pc для получения красителей и пигментов разного цвета. С тех пор были проведены значительные исследования H 2 Pc и MPc, которые привели к широкому спектру применений в таких областях, как фотоэлектрическая энергия , фотодинамическая терапия , конструирование наночастиц и катализ. [14] Электрохимические свойства MPc делают их эффективными донорами и -акцепторами электронов. В результате были разработаны органические солнечные элементы на основе MPc с эффективностью преобразования энергии не более 5%. [15] [16] Кроме того, МПК использовались в качестве катализаторов окисления метана, фенолов, спиртов, полисахаридов и олефинов; MPcs также можно использовать для катализа образования связей C–C и различных реакций восстановления. [17] Фталоцианины кремния и цинка были разработаны в качестве фотосенсибилизаторов для неинвазивного лечения рака. [18]
Различные MPcs также продемонстрировали способность образовывать наноструктуры, которые имеют потенциальное применение в электронике и биосенсорстве . [19] [20] [21] Фталоцианин также используется в некоторых записываемых DVD. [22]
Токсичность и опасности
[ редактировать ]Никаких доказательств острой токсичности или канцерогенности фталоцианиновых соединений не поступало. LD ( 50 крысы, перорально) составляет 10 г/кг. [12]
Родственные соединения
[ редактировать ]Фталоцианины структурно родственны другим тетрапиррольным макроциклам, включая порфирины и порфиразины . Они состоят из четырех пирролоподобных субъединиц, связанных между собой с образованием 16-членного внутреннего кольца, состоящего из чередующихся атомов углерода и азота. К более крупным аналогам относятся нафталоцианины . Пирролоподобные кольца внутри H 2 Pc тесно связаны с изоиндолом . И порфирины, и фталоцианины действуют как плоские тетрадентатные диаионные лиганды , которые связывают металлы через четыре выступающих внутрь азотных центра. Такие комплексы формально являются производными от ПК 2− , сопряженное основание Н 2 шт .

Сноски
[ редактировать ]- ^ Одна « изоиндольная единица» С 8 Н 4 Н 2 ; четыре в конфигурации с азотистым кольцом обозначаются символом Pc = (С 8 Н 4 Н 2 ) 4 .
Ссылки
[ редактировать ]- ^ «Пигмент синий 16» . pubchem.ncbi.nlm.nih.gov . Пубхим. США Национальный институт здравоохранения . Архивировано из оригинала 07.11.2017 . Проверено 8 апреля 2018 г.
- ^ Яннуцци, Марселла; Тран, Фабьен; Видмер, Роланд; Динель, Томас; Радикан, Кевин; Дин, Юн; Хуттер, Юрг; Грёнинг, Оливер (2014). «Сайт-селективная адсорбция фталоцианина на наносетке h-BN/Rh(111)» . Физическая химия Химическая физика . 16 (24): 12374–12384. Бибкод : 2014PCCP...1612374I . дои : 10.1039/C4CP01466A . ПМИД 24828002 .
- ^ Jump up to: а б Гани, Фатима; Кристен, Джулиана; Риглер, Ганс (9 февраля 2012 г.). «Свойства растворимости незамещенных фталоцианинов металлов в различных типах растворителей». Журнал химических и инженерных данных . 57 (2): 439–449. дои : 10.1021/je2010215 . ISSN 0021-9568 .
- ^ Вагнер, Ганс Дж.; Лутфи, Рафик О.; Сяо, Чэн-Куо (1 октября 1982 г.). «Очистка и характеристика фталоцианинов». Журнал материаловедения . 17 (10): 2781–2791. Бибкод : 1982JMatS..17.2781W . дои : 10.1007/bf00644652 . ISSN 0022-2461 . S2CID 96336392 .
- ^ Немыкин Виктор Н.; Лукьянец, Евгений А. (18 февраля 2010 г.). «Синтез замещенных фталоцианинов» . Аркивок . 2010 (1): 136. doi : 10.3998/ark.5550190.0011.104 . hdl : 2027/spo.5550190.0011.104 .
- ^ Сайлз, ПФ; Хан, Т.; Салван, Г.; Кнупфер, М.; Чжу, Ф.; Зан, DRT; Шмидт, О.Г. (21 апреля 2016 г.). «Настраиваемые свойства переноса заряда в гетеропереходах металл-фталоцианин» . Наномасштаб . 8 (16): 8607–8617. Бибкод : 2016Nanos...8.8607S . дои : 10.1039/c5nr08671j . ISSN 2040-3372 . ПМИД 27049842 .
- ^ Браун, А.; Черняк, Дж. (1907). «О продуктах реакции уксусного ангидрида с фталамидом» . Отчеты Немецкого химического общества (на немецком языке). 40 (2): 2709–2714. дои : 10.1002/cber.190704002202 . Архивировано из оригинала 16 сентября 2017 г. Проверено 15 сентября 2015 г.
- ^ де Дисбах, Анри; фон дер Вейд, Эдмонд (1927). «Некоторые комплексные соли о -динитрилов с медью и пиридином » . Helvetica Chimica Acta (на французском языке). 10 : 886–888. дои : 10.1002/hlca.192701001110 .
- ^ «Открытие нового пигмента: история Монастральского синего от Imperial Chemical Industries» . colorantshistory.org . Архивировано из оригинала 25 июля 2009 г. Проверено 18 января 2010 г.
{{cite web}}: CS1 maint: неподходящий URL ( ссылка ) - ^ Линстед, Р.П. (1 января 1934 г.). «212. Фталоцианины. Часть I. Новый тип синтетических красящих веществ». Журнал Химического общества . (возобновлено): 1016. doi : 10.1039/jr9340001016 . ISSN 0368-1769 .
- ^ Сакамото, Кейичи; Оно-Окумура, Эйко (28 августа 2009 г.). «Синтез и функциональные свойства фталоцианинов» . Материалы . 2 (3): 1127–1179. Бибкод : 2009Mate....2.1127S . дои : 10.3390/ma2031127 . ПМЦ 5445737 .
- ^ Jump up to: а б с Лёбберт, Герд. «Фталоцианины». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a20_213 . ISBN 978-3527306732 .
- ^ Дален, Майлз А. (1 июля 1939 г.). «Фталоцианины: новый класс синтетических пигментов и красителей». Промышленная и инженерная химия . 31 (7): 839–847. дои : 10.1021/ie50355a012 . ISSN 0019-7866 .
- ^ Классенс, Кристиан Г.; Хан, Уве; Торрес, Томас (2008). «Фталоцианины: от выдающихся электронных свойств к новым применениям». Химическая запись . 8 (2): 75–97. дои : 10.1002/tcr.20139 . ISSN 1528-0691 . ПМИД 18366105 .
- ^ Кумар, Чаллури Виджай; Сфири, Грузия; Раптис, Димитриос; Стататос, Элиас; Лианос, Панайотис (10 декабря 2014 г.). «Перовскитный солнечный элемент с дешевым Cu-фталоцианином в качестве материала для переноса дырок». РСК Прогресс . 5 (5): 3786–3791. дои : 10.1039/c4ra14321c . ISSN 2046-2069 . S2CID 84832945 .
- ^ Юэнь, Эйвери П.; Йованович, Стивен М.; Хор, А-Ми; Кленклер, Ричард А.; Девеньи, Габриэль А.; Лутфи, Рафик О.; Престон, Джон С. (2012). «Фотоэлектрические свойства органических солнечных элементов М-фталоцианин / фуллерен». Солнечная энергия . 86 (6): 1683–1688. Бибкод : 2012SoEn...86.1683Y . doi : 10.1016/j.solener.2012.03.019 . S2CID 55531280 .
- ^ Сорокин, Александр Б. (09 октября 2013 г.). «Фталоцианиновые металлокомплексы в катализе». Химические обзоры . 113 (10): 8152–8191. дои : 10.1021/cr4000072 . ISSN 0009-2665 . ПМИД 23782107 .
- ^ Миллер, Дж.; Барон, Э.; Скалл, Х.; Ся, А.; Берлин, Дж.; Маккормик, Т.; Колусси, В.; Кенни, М.; Купер, К. (2007). «Фотодинамическая терапия с фталоцианиновым фотосенсибилизатором Pc 4: практический опыт доклинических механистических и ранних клинико-трансляционных исследований» . Токсикология и прикладная фармакология . 224 (3): 290–299. дои : 10.1016/j.taap.2007.01.025 . ПМК 2128784 . ПМИД 17397888 .
- ^ Каран, Сантану; Басак, Дхрубаджьоти; Маллик, Бисванат (2007). «Наночастицы фталоцианина меди и наноцветы». Письма по химической физике . 434 (4–6): 265–270. Бибкод : 2007CPL...434..265K . дои : 10.1016/j.cplett.2006.12.007 .
- ^ ван Керен, Эдвард; Кость, Алисия; Ма, Чанбао (1 июня 2008 г.). «Образование наночастиц фталоцианина в пересыщенных растворах». Ленгмюр . 24 (12): 6079–6084. дои : 10.1021/la800290s . ISSN 0743-7463 . ПМИД 18479155 .
- ^ Локеш, К.С.; Шиварадж, Ю.; Даянанда, БП; Чандра, Судешна (2009). «Синтез наночастиц родия, стабилизированных фталоцианином, и их применение в биосенсорстве цитохрома с». Биоэлектрохимия . 75 (2): 104–109. doi : 10.1016/j.bioelechem.2009.02.005 . ПМИД 19303822 .
- ^ «Mitsui Gold Archival DVD-R и DVD+R» . www.conservationresources.com . Архивировано из оригинала 26 ноября 2018 г. Проверено 13 апреля 2020 г.
Внешние ссылки
[ редактировать ]- «Общество порфиринов и фталоцианинов» . spp-jpp.org .
- Оценка Wiki (21 марта 2006 г.), автор Генри Рзепа. Сэр Патрик Линстед: Фталоцианины . Кафедра химии. ХимВики (видео). Великобритания: Имперский колледж .
- «Журнал порфиринов и фталоцианинов» . worldscinet.com/jpp/ . Архивировано из оригинала 2 июня 2020 г. Проверено 19 августа 2009 г.
- «Открытие ICI Грейнджмут» (видео). Архивировано из оригинала 18 августа 2006 г. на сайте colorantshistory.org.
{{cite web}}: CS1 maint: неподходящий URL ( ссылка )