Дифосфиновые лиганды

Дифосфины , иногда называемые бисфосфанами , представляют собой фосфорорганические соединения, наиболее часто используемые в качестве бидентатных фосфиновых лигандов в неорганической и металлоорганической химии . Они идентифицируются по наличию двух фосфиногрупп, связанных основной цепью, и обычно являются хелатирующими . [ 1 ] Было синтезировано большое количество дифосфинов с различными линкерами и R-группами. Изменение линкера и R-групп изменяет электронные и стерические свойства лигандов, что может привести к различной геометрии координации и каталитическому поведению в гомогенных катализаторах .
Синтез
[ редактировать ]
Из фосфидных строительных блоков
[ редактировать ]
Многие широко используемые дифосфиновые лиганды имеют общую формулу Ar 2 P(CH 2 ) n PAr 2 . Эти соединения можно получить реакцией X(CH 2 ) n X (X = галоген) и MPPH 2 (M = щелочной металл): [ 2 ]
- Cl(CH 2 ) n Cl + 2 NaPPh 2 → Ph 2 P(CH 2 ) n PPh 2 + 2 NaCl
Дифосфиновые лиганды также можно получить из дилитированных реагентов и хлорфосфинов: [ 3 ]
- XLi 2 + 2 ClPAr 2 → X(PAr 2 ) 2 + 2 LiCl (X = углеводородная основная цепь)
Этот подход подходит для установки двух диалкилфосфиногрупп с использованием таких реагентов, как хлордиизопропилфосфин .
Другой популярный метод, подходящий для получения несимметричных дифосфинов, предполагает присоединение вторичных фосфинов к винилфосфинам :
- Ф 2 PH + 2 CH 2 =CHPAr 2 → Ph 2 PCH 2 -CH 2 PAr 2
(2-Литиофенил)дифенилфосфин также можно использовать для получения несимметричных дифосфинов. Литированный реагент доступен из (2-бромфенил)дифенилфосфина :
- Ph 2 P(C 6 H 4 Br) + BuLi → Ph 2 P(C 6 H 4 Li) + BuBr
- Ph 2 P(C 6 H 4 Li) + R 2 PCli → Ph 2 P(C 6 H 4 PR 2 ) + LiCl
Из предшественников бис(дихлорфосфина)
[ редактировать ]Многие дифосфины получают из соединений типа X(PCl 2 ) 2 , где X = (CH 2 ) n или C 6 H 4 . Ключевые реагенты — 1,2-бис(дихлорфосфино)этан и 1,2-бис(дихлорфосфино)бензол .

Длина цепи и координационные свойства
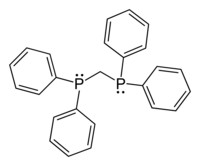
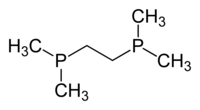
[ редактировать ]Короткоцепочечный дифосфин dppm имеет тенденцию способствовать взаимодействиям металл-металл, как показано на примере комплексов с А-каркасом . Когда два фосфиновых заместителя связаны двумя-четырьмя углеродными центрами, образующиеся лиганды часто образуют хелатные кольца с одним металлом. Распространенным дифосфиновым лигандом является dppe , который образует пятичленное хелатное кольцо с большинством металлов.
Некоторые дифосфины, такие как исключительный случай т Бу 2 П(СН 2 ) 10 П т Bu 2 , дают макроциклические комплексы, содержащие до 72 атомов в кольце. [ 6 ]
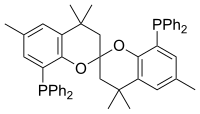
Чтобы расположить транс-донорные группы фосфина в координационной сфере, необходимо несколько атомов, чтобы связать донорные центры, а длинноцепочечные дифосфины обычно гибкие и плохо хелатируются. Эта проблема была решена с помощью длинного, но жесткого дифосфина SPANphos. [ 7 ] Угол прикуса дифосфина влияет на реакционную способность металлоцентра. [ 8 ]
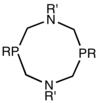
Также существуют некоторые примеры нехелатирующего дифосфина. Из-за стерического эффекта эти атомы фосфора не могут реагировать ни с чем, кроме протона. [ 9 ] Его можно изменить с нехелатирующего дифосфина на хелатирующий дифосфин, регулируя длину соединительного плеча. [ 10 ]
Репрезентативные лиганды
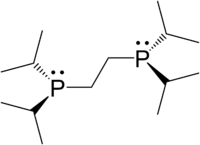
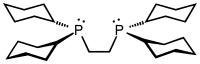
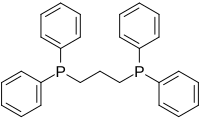
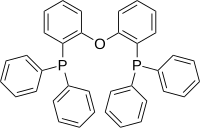
[ редактировать ]Наиболее распространенные дифосфиновые лиганды показаны в таблице ниже: [ 11 ]
См. также
[ редактировать ]Диалкилбиарилфосфиновые лиганды
Ссылки
[ редактировать ]- ^ Хартвиг, Дж. Ф. Химия органопереходных металлов, от связывания к катализу; Университетские научные книги: Нью-Йорк, 2010. ISBN 189138953X
- ^ Уилкинсон, Г.; Гиллард, Р.; МакКлеверти, Дж. Комплексная координационная химия: синтез, реакции, свойства и применение координационных соединений , том 2.; Pergamon Press: Оксфорд, Великобритания, 1987; п. 993. ISBN 0-08-035945-0
- ^ Гарет Дж. Роулендс «Планарные хиральные фосфины, полученные из [2.2] парациклофана», Израильский химический журнал, 2012 г., том 52, выпуск 1-2, страницы 60–75. дои : 10.1002/ijch.201100098
- ^ Берт, Роджер Дж.; Чатт, Джозеф; Хусейн, Васиф; Ли, Дж. Джеффри (1979). «Удобный синтез 1,2-бис(дихлорфосфино)этана, 1,2-бис(диметилфосфино)этана и 1,2-бис(диэтилфосфино)этана». Журнал металлоорганической химии . 182 (2): 203–206. дои : 10.1016/S0022-328X(00)94383-3 .
- ^ Молой, Кеннет Г.; Петерсен, Джеффри Л. (1995). «N-пирролилфосфины: неиспользованный класс фосфиновых лигандов с исключительным .pi.-акцепторным характером». Журнал Американского химического общества . 117 (29): 7696–7710. дои : 10.1021/ja00134a014 .
- ^ Коттон, ФА; Уилкинсон, Г. Продвинутая неорганическая химия: подробный текст , 4-е изд.; Публикации Wiley-Interscience: Нью-Йорк, Нью-Йорк, 1980; стр.246. ISBN 0-471-02775-8
- ^ З. Фрейша, М.С. Бентджес, Г.Д. Батема, CB Дилеман, GPF v. Стрейдонк, Дж. Н. Х. Рик, П. К. Камер, Дж. Фраанже, К. Губитц и PWNM Ван Леувен (2003). «СПАНфос: AC 2 -симметричный транс -координационный дифосфан-лиганд». Прикладная химия . 42 (11): 1322–1325. дои : 10.1002/anie.200390330 . ПМИД 12645065 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Биркхольц, М.-Н., Фрейша, З., ван Леувен, PWNM, «Эффекты угла прикуса дифосфинов в связях CC и CX, образующих реакции перекрестного сочетания», Chem. Соц. Ред. 2009 г., том. 38, 1099
- ^ Зонг Дж., Дж. Т. Мэг, К. М. Крамл и Р. А. Паскаль-младший, Застой в дифосфине, Org. Летт. 2013, 15, 2179-2181.
- ^ Зонг, Дж., Дж. Т. Мэг и Р. А. Паскаль-младший, «Инкапсуляция неводородных атомов с помощью ин-, ин-бис (триарэлемент)-содержащих циклофанов». Тетраэдр, 2017, 73, 455-460.
- ^ http://old.iupac.org/reports/provisional/abstract04/RB-prs310804/TableVII-3.04.pdf [ только URL-адрес PDF ]











![Общий лиганд Йозифоса[3]](http://upload.wikimedia.org/wikipedia/commons/thumb/6/63/Josiphos.png/200px-Josiphos.png)