Йозифосные лиганды

Лиганд Josiphos представляет собой тип хирального дифосфина , который был модифицирован для субстрат -специфичности; они широко используются для энантиоселективного синтеза . [ 2 ] Они широко используются в асимметричном катализе. [ 3 ]
История
[ редактировать ]
В современном энантиоселективном синтезе обычно используется хорошо подобранный гомогенный катализатор на ключевых стадиях . Лиганды . этих катализаторов придают хиральность Семейство привилегированных лигандов Josiphos обеспечивает особенно высокие выходы в энантиоселективном синтезе. [ 4 ] [ 5 ]
Ciba (ныне Novartis ). В начале 1990-х годов Антонио Тони начал обучение в Центральной исследовательской лаборатории [ 6 ] ранее известный [ 7 ] ферроценильные лиганды для Au(I) катализируемой альдольной реакции, . [ 6 ] Команда Тони начала рассматривать дифосфиновые лиганды, а техник Джози Пулео приготовил первые лиганды с помощью вторичных фосфинов. Команда применила продукты Puleo в Ru , катализируемом енамидов синтезе гидрирования ; при значительном успехе реакция имела ee >99% и частоту оборота (TOF) 0,3 с. −1 . [ 6 ] [ 7 ] Тот же лиганд оказался полезным при производстве (S)-метолахлора , активного ингредиента самого распространенного гербицида в Соединенных Штатах. Синтез требует энантиоселективного имина гидрирования ; после введения катализатора реакция протекает со 100% конверсией, числом оборотов (TON) >7млн и частотой оборотов >0,5 мс. −1 . Этот процесс представляет собой крупнейшее применение энантиоселективного гидрирования, позволяющее производить более 10 килотонн желаемого продукта в год с 79% э.э. [ 2 ] [ 1 ]
в неэнантиоселективных реакциях: катализируемой Pd реакции арилхлоридов и арилвинилтозилатов Лиганды йозифоса также используются с TON 20 000 или выше, [ 8 ] каталитическое карбонилирование, [ 9 ] или Гриньяра и Негиши . муфты [ 10 ] [ 11 ] Различные лиганды Josiphos коммерчески доступны по лицензии от Solvias . (RS) и его энантиомер обеспечивают более высокие выходы и энантиоселективность, чем диастереомер (R,R). [ 1 ]
Ферроценовый каркас оказался универсальным. [ 3 ] [ 12 ] [ 13 ] [ 14 ] [ 15 ] Одним из структурных параметров, влияющих на реактивность, является угол прикуса. П 1 -МП 2 угол имеет среднее значение 92,7°. [ 3 ]
По общему мнению, индивидуальный лиганд сокращается как (R)-(S)-R 2 PF-PR' 2 . Заместитель в Cp написан перед F, а R в хиральном центре после F. [ 2 ]
Реакции с использованием лигандов Йозифоса
[ редактировать ]Некоторые реакции, которые осуществляются с использованием комплексов M-Йозифоса в качестве катализатора, перечислены ниже. Другими реакциями, в которых могут быть использованы лиганды Йозифоса, являются: гидрирование связей C=N, C=C и C=O , катализируемое аллильное замещение , гидрокарбоксилирование , присоединение Михаэля , аллильное алкилирование , реакции типа Хека , оксабицикла раскрытие кольца и аллиламина. изомеризация . [ нужна ссылка ]
- Гидроборирование стирола
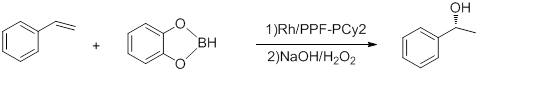
- Вышеупомянутая реакция, проведенная при -78 °C, имеет ee до 92% и время TOF 5-10 часов. −1 . [ 16 ] Комплекс Rh-бинап Хаяши дает лучший урожай. [ 17 ]
- Гидроформилирование стирола

- Эта схема реакции дает до 78% э.и. продукта (R), но низкие значения TON и TOF: 10–210 и 1–14 ч. −1 (соответственно). [ 2 ] [ 18 ]
- Восстановительное аминирование
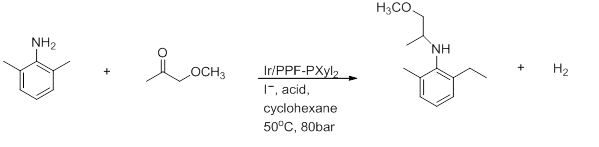
- Выше представлено получение (S)-метолахлора . Для хороших выходов и 100%-ной конверсии необходим растворитель AcOH. [ 17 ]
- Гидрирование экзоциклического метилимина

- Этот ключевой этап синтеза ВИЧ-интегразы ингибитора Криксивана является одной из немногих известных реакций гидрирования гомогенных гетероаренов . Громоздкие группы R повышают производительность катализатора: ee 97%, а время TON и TOF составляет 1 тыс. и 8 мин. −1 , соответственно. [ 19 ] [ 20 ]
- Асимметричный синтез производных хроманоилпиридина
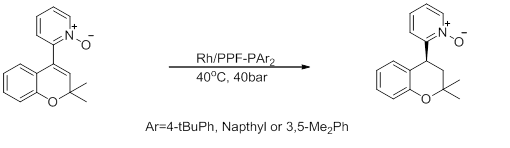
- Эта реакция, являющаяся промежуточным продуктом синтеза гипотензивного и противоалопетического производного хроманоилпиридина , демонстрирует высокую энантиоселективность, но низкую активность. [ 21 ]
Модифицированные лиганды Йозифоса
[ редактировать ]Сообщалось о многих вариациях лигандов Йозифоса. Одно семейство получают из амина Уги .

Важным улучшением начального синтеза стало использование N(CH 3 ) 2 в качестве уходящей группы по сравнению с ацетатом , хотя растворитель уксусная кислота дает лучшие выходы. [ 6 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Блазер, Ганс Ульрих; Пугин, Бенуа; Шпиндлер, Феликс (2021). «Развлечение (и коммерческий успех) с иозифосом и родственными хиральными лигандами на основе ферроцена». Helvetica Chimica Acta . 104 . дои : 10.1002/hlca.202000192 . S2CID 229427019 .
- ^ Jump up to: а б с д Блазер, Ганс-Ульрих; Бриден, Уолтер; Пугин, Бенуа; Шпиндлер, Феликс; Штудер, Мартин; Тони, Антонио (2002). «Сольвиас Йозифос Лиганды: от открытия к техническому применению» . Темы катализа . 19 (1): 3–16. дои : 10.1023/A:1013832630565 .
- ^ Jump up to: а б с Блазер, Ганс-Ульрих; Пугин, Бенуа; Шпиндлер, Феликс; Мехия, Эстебан; Тони, Антонио (6 апреля 2011 г.). Чжоу, Ци-Лин (ред.). Йозифосские лиганды: от открытия к техническому применению (1-е изд.). Уайли. стр. 93–136. дои : 10.1002/9783527635207.ch3 . ISBN 978-3-527-32704-1 .
- ^ Спессард, Гэри О.; Мисслер, Гэри Л. (2010). Металлоорганическая химия (2-е изд.). Нью-Йорк: Издательство Оксфордского университета. стр. 378–379. ISBN 978-0-19-533099-1 .
- ^ Эльшенбройх, Кристофер (2006). Металлоорганические соединения: Третье издание. стр.518-519
- ^ Jump up to: а б с д Тони, Антонио (27 марта 1996 г.). «Разработка новых хиральных ферроценильных лигандов для асимметричного катализа: личный отчет» . ХИМИЯ . 50 (3): 86. doi : 10.2533/chimia.1996.86 . ISSN 2673-2424 .
- ^ Jump up to: а б Ито, Ёсихико.; Савамура, Масая.; Хаяси, Тамио. (октябрь 1986 г.). «Каталитическая асимметричная альдольная реакция: реакция альдегидов с изоцианоацетатом, катализируемая хиральным комплексом ферроценилфосфин-золото (I)» . Журнал Американского химического общества . 108 (20): 6405–6406. дои : 10.1021/ja00280a056 . ISSN 0002-7863 .
- ^ Литтке, Адам Ф.; Фу, Грегори К. (15 ноября 2002 г.). «Катализируемые палладием реакции сочетания арилхлоридов» . Angewandte Chemie, международное издание . 41 (22): 4176–4211. doi : 10.1002/1521-3773(20021115)41:22<4176::AID-ANIE4176>3.0.CO;2-U . ПМИД 12434342 .
- ^ Цай, Чаосянь; Ривера, Нело Р.; Балселлс, Жауме; Сидлер, Рик Р.; Маквильямс, Дж. Кристофер; Шульц, К. Скотт; Сунь, Юнкуй (01 октября 2006 г.). «Эффективный катализатор Pd-катализируемого карбонилирования арилареносульфонатов» . Органические письма . 8 (22): 5161–5164. дои : 10.1021/ol062208g . ISSN 1523-7060 . PMID 17048868 .
- ^ Лиммерт, Майкл Э.; Рой, Эми Х.; Хартвиг, Джон Ф. (1 ноября 2005 г.). «Сочетание Кумада арил- и винилтозилатов в мягких условиях» . Журнал органической химии . 70 (23): 9364–9370. дои : 10.1021/jo051394l . ISSN 0022-3263 . ПМИД 16268609 .
- ^ Во, Джанг Д.; Хартвиг, Джон Ф. (12 августа 2009 г.). «Катализируемое палладием сочетание аммиака с арилхлоридами, бромидами, йодидами и сульфонатами: общий метод получения первичных ариламинов» . Журнал Американского химического общества . 131 (31): 11049–11061. дои : 10.1021/ja903049z . ISSN 0002-7863 . ПМЦ 2823124 . ПМИД 19591470 .
- ^ Блазер, Ганс-Ульрих; Малан, Кристоф; Пугин, Бенуа; Шпиндлер, Феликс; Штайнер, Хайнц; Студер, Мартин (январь 2003 г.). «Селективное гидрирование для продуктов тонкой химии: последние тенденции и новые разработки» . Расширенный синтез и катализ . 345 (1–2): 103–151. дои : 10.1002/adsc.200390000 . ISSN 1615-4150 .
- ^ Уайтселл, Джеймс К. (1 ноября 1989 г.). «С2-симметрия и асимметричная индукция» . Химические обзоры . 89 (7): 1581–1590. дои : 10.1021/cr00097a012 . ISSN 0009-2665 .
- ^ Иногути, Киёси; Сакураба, Сюндзи; Ачива, Кадзуо (1992). «Концепции разработки высокоэффективных хиральных бисфосфиновых лигандов в асимметричном гидрировании, катализируемом родием» . Синлетт . 1992 (3): 169–178. дои : 10.1055/s-1992-21306 . ISSN 0936-5214 . S2CID 196807901 .
- ^ Чен, В. и Блазер, Ху, 2008, Фосфорные лиганды в асимметричном катализе: синтез и применение. (ред. А. Борнер), стр. 359-393.
- ^ Т. Хаяши, Комплексный асимметричный катализатор, ред. Э. Н. Якобсен, А. Пфальц и Х. Ямамото, 1999, стр. 247.
- ^ Jump up to: а б Блазер, Ганс-Ульрих; Бузер, Ханс-Петер; Джалетт, Ханс-Петер; Пугин, Бенуа; Шпиндлер, Феликс (31 декабря 1999 г.). «Энантиоселективное восстановительное алкилирование затрудненного анилина, катализируемое иридием ферроценилдифосфином» . Синлетт . 1999 (Дополнение 1): 867–868. дои : 10.1055/s-1999-3106 . ISSN 0936-5214 . S2CID 99845649 .
- ^ Годар, Сирил; Руис, Аврора; Клавер, Кармен (август 2006 г.). «Систематическое исследование асимметричного метоксикарбонилирования стирола, катализируемого палладиевыми системами, содержащими хиральные ферроценилдифосфиновые лиганды» . Helvetica Chimica Acta . 89 (8): 1610–1622. дои : 10.1002/hlca.200690161 . ISSN 0018-019Х .
- ^ Р.Фукс, EP 803502 (1996), переданный Lonza AG.
- ^ Штудер, Мартин; Ведемейер-Эксл, Кристина; Шпиндлер, Феликс; Блазер, Ганс-Ульрих (13 декабря 2000 г.). «Энантиоселективное гомогенное гидрирование монозамещенных пиридинов и фуранов» . Monatshefte fuer Chemie/Ежемесячный журнал по химии . 131 (12): 1335–1343. дои : 10.1007/s007060070013 .
- ^ Э. Брогер, Ю. Крамери и П. Джонс, WO 99/01 453. (1997), передано Hoffman-La Roche.




