История полимеразной цепной реакции
Возможно, эту статью необходимо реорганизовать, чтобы она соответствовала рекомендациям Википедии по оформлению . ( Май 2017 г. ) |
- (Эта статья предполагает знакомство с терминами и компонентами, используемыми в процессе ПЦР.)



Историю полимеразной цепной реакции (ПЦР) по-разному описывают как классическую «Эврику!» момент, [ 1 ] или как пример совместной работы разрозненных исследователей. [ 2 ] Ниже приводится список событий до, во время и после его разработки:
Прелюдия
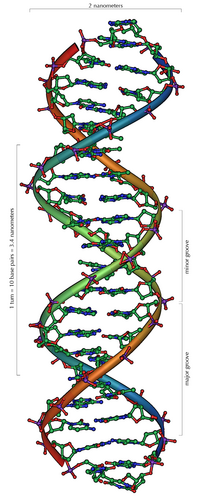
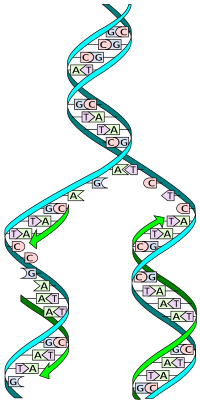
[ редактировать ]- Джеймс 25 апреля 1953 года Д. Уотсон и Фрэнсис Крик опубликовали «радикально иную структуру» ДНК . [ 3 ] тем самым основав область молекулярной генетики . Их структурная модель включала две цепи комплементарной ДНК, спаренные основаниями , идущие в противоположных направлениях в виде двойной спирали. В заключение они заявили, что «от нашего внимания не ускользнуло то, что специфическое спаривание, которое мы постулировали, сразу предполагает возможный механизм копирования генетического материала». За это открытие они были удостоены Нобелевской премии в 1962 году .
- Начиная с середины 1950-х годов , Артур Корнберг приступил к изучению механизма репликации ДНК . [ 4 ] К 1957 году он идентифицировал первую ДНК-полимеразу . [ 5 ] Фермент был ограничен: он создавал ДНК только в одном направлении и требовал наличия существующего праймера для инициирования копирования цепи матрицы. В целом процесс репликации ДНК удивительно сложен: для открытия спирали ДНК, поддержания ее открытой, создания праймеров , синтеза новой ДНК, удаления праймеров и соединения всех частей вместе требуются отдельные белки. Корнберг был удостоен Нобелевской премии в 1959 году .
- В начале 1960-х годов Х. Гобинд Корана добился значительных успехов в выяснении генетического кода . После этого он инициировал большой проект по полному синтезу функционального человеческого гена . [ 6 ] Чтобы добиться этого, Корана стал пионером многих методов, необходимых для создания и использования синтетических ДНК олигонуклеотидов . Специфические для последовательности олигонуклеотиды использовались как в качестве строительных блоков гена, так и в качестве праймеров и матриц для ДНК-полимеразы. В 1968 году Хорана был удостоен Нобелевской премии за работу над генетическим кодом.
- В 1969 году Томас Д. Брок сообщил об выделении нового вида бактерий из горячего источника в Йеллоустонском национальном парке . Термус водный [ 7 ] (Taq) стал стандартным источником ферментов, способных выдерживать более высокие температуры, чем ферменты E. coli .
- В 1970 году Кленов сообщил о модифицированной версии ДНК-полимеразы I из E. coli . [ 8 ] Обработка протеазой устраняла «прямую» нуклеазную активность этого фермента. Таким образом, общая активность полученного фрагмента Кленова смещена в сторону синтеза ДНК, а не ее деградации.
- К 1971 году исследователи проекта Кораны, обеспокоенные выходом ДНК, начали изучать «синтез восстановления» — искусственную систему праймеров и матриц, которая позволяет ДНК-полимеразе копировать сегменты гена, который они синтезируют. Несмотря на то, что они похожи на ПЦР в использовании повторных применений ДНК-полимеразы, процесс, который они обычно описывают, [ 9 ] использует только один комплекс праймер-матрица и, следовательно, не приводит к экспоненциальной амплификации, наблюдаемой в ПЦР.
- Примерно в 1971 году Кьелл Клеппе , исследователь из лаборатории Кораны, предложил процесс, очень похожий на ПЦР. В конце статьи о более ранней технике: [ 10 ] он описал, как система с двумя праймерами может привести к репликации определенного сегмента ДНК: [ 10 ]
- можно было бы надеяться получить две структуры, каждая из которых содержит полную длину цепи матрицы, соответствующим образом комплексованной с праймером. ДНК-полимераза будет добавлена для завершения процесса репарационной репликации. В результате должны получиться две молекулы исходного дуплекса. Весь цикл можно было повторить, добавляя каждый раз новую дозу фермента.
- Никаких результатов там не показано, а упоминание о неопубликованных экспериментах в другой статье [ 9 ] может (или не может) относиться к системе репликации с двумя праймерами. (Эти ранние предшественники ПЦР были тщательно изучены в патентном иске и обсуждаются в главах книги Маллиса « Полимеразная цепная реакция» (1994). [ 11 ] )
- Также в 1971 году в Cetus Corporation была основана Беркли, Калифорния , Рональдом Кейпом, Питером Фарли и Дональдом Глейзером . Первоначально компания проверяла микроорганизмы, способные производить компоненты, используемые при производстве продуктов питания, химикатов, вакцин или фармацевтических препаратов. Переехав в соседний Эмеривилл , они начали проекты, связанные с новой биотехнологической отраслью, в первую очередь клонированием и экспрессией человеческих генов, а также разработкой диагностических тестов на генетические мутации.
- В 1976 году ДНК -полимераза [ 12 ] был выделен из T. aquaticus . Было обнаружено, что он сохраняет свою активность при температуре выше 75 °C.
- В 1977 году Фредерик Сэнгер сообщил о методе определения последовательности ДНК. [ 13 ] В этом методе использовались олигонуклеотидный праймер , ДНК-полимераза и модифицированные предшественники нуклеотидов , которые блокируют дальнейшее расширение праймера в зависимости от последовательности. За это нововведение он был удостоен Нобелевской премии в 1980 году .
К 1980 году все компоненты, необходимые для проведения ПЦР-амплификации, были известны научному сообществу. Использование ДНК-полимеразы для удлинения олигонуклеотидных праймеров было обычной процедурой секвенирования ДНК и получения кДНК для клонирования и экспрессии . Использование ДНК-полимеразы для трансляции никнеймов было наиболее распространенным методом мечения ДНК-зондов для Саузерн-блоттинга .
Тема
[ редактировать ]- В 1979 году корпорация Cetus наняла Кэри Маллиса для синтеза олигонуклеотидов для различных научно-исследовательских проектов компании. [ 14 ] Эти олигонуклеотиды использовались в качестве зондов для скрининга клонированных генов, в качестве праймеров для секвенирования ДНК и синтеза кДНК, а также в качестве строительных блоков для конструирования генов. Первоначально синтезируя эти олигонуклеотиды вручную, Муллис позже оценил ранние прототипы автоматических синтезаторов. [ 1 ]
- К маю 1983 года Муллис синтезировал олигонуклеотидные зонды для проекта Cetus по анализу мутации серповидноклеточной анемии . Сэнгера Услышав о проблемах в их работе, Маллис предложил альтернативную технику, основанную на методе секвенирования ДНК . [ 14 ] Понимая, насколько сложно сделать метод Сэнгера специфичным для одного участка генома, Муллис затем модифицировал идею, добавив второй праймер на противоположную цепь. Повторное применение полимеразы может привести к цепной реакции репликации определенного участка генома – ПЦР.
- Позже в 1983 году Муллис начал проверять свою идею. Его первый эксперимент [ 2 ] не включал термоциклирование – он надеялся, что полимераза сможет продолжать репликацию самостоятельно. Более поздние эксперименты в том же году включали повторные термические циклы и были нацелены на небольшие сегменты клонированного гена. Муллис посчитал эти эксперименты успешными, но не смог убедить других исследователей.
- В июне 1984 года Cetus провела свое ежегодное собрание в Монтерее, Калифорния . Его ученые и консультанты представили свои результаты и рассмотрели будущие проекты. Муллис представил плакат о производстве олигонуклеотидов в своей лаборатории и представил некоторые результаты своих экспериментов с ПЦР. [ 2 ] Только Джошуа Ледерберг , консультант Cetus, проявил интерес. [ 14 ] Позже на встрече Маллис был вовлечен в физическую ссору с другим исследователем Cetus из-за спора, не связанного с ПЦР. [ 2 ] Другой учёный покинул компанию, а Муллиса сняли с поста руководителя лаборатории синтеза олигонуклеотидов.
Разработка
[ редактировать ]- В сентябре 1984 года Том Уайт, вице-президент по исследованиям Cetus (и его близкий друг), оказал давление на Муллиса, чтобы тот поделился своей идеей с группой, разрабатывающей анализ генетических мутаций. Вместе они провели следующие месяцы, разрабатывая эксперименты, которые могли бы убедительно показать, что ПЦР работает с геномной ДНК. К сожалению, ожидаемый продукт амплификации не был виден при электрофорезе в агарозном геле . [ 15 ] что приводит к путанице относительно того, была ли реакция специфичной для целевого региона.
- В ноябре 1984 года [ 2 ] продукты амплификации анализировали с помощью Саузерн-блоттинга , который ясно продемонстрировал увеличение количества ожидаемого размером 110 п.н. продукта ДНК [ 16 ] Получив первый видимый сигнал, исследователи начали оптимизировать процесс. Позже амплифицированные продукты были клонированы и секвенированы, что показало, что большая часть амплифицированной ДНК была желаемой мишенью и что фрагмент Кленова лишь изредка включал неправильные нуклеотиды во время репликации. используемый тогда [ 15 ]
Экспозиция
[ редактировать ]- Следуя обычной производственной практике, Маллис применил [ 17 ] на патент, попросило его охватывающий основную идею ПЦР и многие потенциальные применения, и Управление по технической документации включить дополнительные результаты. группа 28 марта 1985 года разработчиков Муллиса подала заявку. [ 18 ] основное внимание уделялось анализу мутаций серповидноклеточной анемии с помощью ПЦР и ограничения олигомеров . После внесения изменений оба патента были утверждены 28 июля 1987 года .
- Весной 1985 года группа разработчиков начала применять метод ПЦР к другим мишеням. Праймеры и зонды были разработаны для вариабельного сегмента гена человеческого лейкоцитарного антигена DQα . Эта реакция была гораздо более специфичной, чем реакция для мишени β-гемоглобина – ожидаемого продукта ПЦР. [ 15 ] непосредственно виден при электрофорезе в агарозном геле . Продукты амплификации из различных источников также были клонированы и секвенированы, что стало первым определением новых аллелей с помощью ПЦР. [ 15 ] В то же время первоначальный метод анализа олигомер-рестрикции был заменен более общим методом аллель-специфических олигонуклеотидов . [ 19 ]
- Также в начале 1985 года группа начала использовать термостабильную ДНК-полимеразу ( фермент , использованный в исходной реакции, разрушается на каждом этапе нагревания). В то время [ 1 ] были описаны только два из Taq и Bst . Отчет о Taq-полимеразе [ 12 ] был более подробным, поэтому для тестирования был выбран именно он. Позже выяснилось, что Bst-полимераза непригодна для ПЦР. [ нужна ссылка ] . Тем летом Муллис попытался изолировать фермент, и для его изготовления заключили контракт с группой за пределами Цетуса, но все безуспешно. Осенью 1985 года Сюзанне Стоффель и Дэвиду Гельфанду из Cetus удалось создать полимеразу, и Рэнди Сайки сразу же обнаружил, что она поддерживает процесс ПЦР.
- После получения патентов началась работа по представлению информации о ПЦР широкому научному сообществу. Тезисы докладов для Американского общества генетики человека встречи в Солт-Лейк-Сити были представлены в апреле 1985 года , а первое заявление о ПЦР было сделано Сайки в октябре . [ 20 ] Были запланированы две публикации: «идея» от Маллиса и «приложение» от всей группы разработчиков. Маллис представил свою рукопись в журнал Nature , который отклонил ее из-за отсутствия результатов. Другая статья, в основном описывающая анализ OR , была представлена в журнал Science 20 сентября 1985 г. и принята в ноябре. После отклонения отчета Маллиса в декабре подробности процесса ПЦР были поспешно добавлены во второй документ, который появился 20 декабря 1985 года . [ 16 ]
- В мае 1986 года Маллис представил ПЦР на симпозиуме в Колд-Спринг-Харборе. [ 21 ] и гораздо позже опубликовал модифицированную версию своей оригинальной рукописи «идеи». [ 22 ] Первый отчет, не относящийся к цетусам, с использованием ПЦР, был представлен 5 сентября 1986 г. [ 23 ] показывая, как быстро другие лаборатории начали внедрять эту технику. Группа разработчиков Cetus опубликовала подробный анализ последовательности продуктов ПЦР 8 сентября 1986 года . [ 15 ] и использование ими ASO зондов 13 ноября 1986 года . [ 19 ]
- Об использовании Taq-полимеразы в ПЦР было объявлено Генри Эрлихом на встрече в Берлине 20 сентября 1986 года , представлено к публикации в октябре 1987 года и опубликовано в начале следующего года». [ 24 ] Патент на ПЦР с Taq-полимеразой был подан 17 июня 1987 года и выдан 23 октября 1990 года . [ 25 ]
Вариация
[ редактировать ]В декабре 1985 года было создано совместное предприятие Cetus и Perkin-Elmer по разработке инструментов и реагентов для ПЦР. Сложные термоциклеры были созданы для усиления на основе Кленова, но так и не поступили на рынок. Были разработаны более простые машины для ПЦР на основе Taq, и 19 ноября 1987 года в пресс-релизе было объявлено о коммерческой доступности «Термального циклера PCR-1000» и «ДНК-полимеразы AmpliTaq». Весной 1985 года Джон Снински из Cetus начал использовать ПЦР для решения сложной задачи измерения количества ВИЧ, циркулирующего в крови. О жизнеспособном тесте было объявлено 11 апреля 1986 г. и опубликовано в мае 1987 г. [ 26 ] Затем донорскую кровь можно будет проверить на наличие вируса и напрямую контролировать эффект противовирусных препаратов.
В 1985 году Норм Арнхейм, также являвшийся членом команды разработчиков, завершил творческий отпуск в Cetus и занял академическую должность в Университете Южной Калифорнии . Он начал исследовать использование ПЦР для амплификации образцов, содержащих только одну копию целевой последовательности. К 1989 году его лаборатория разработала мультиплексную ПЦР на одиночных сперматозоидах для прямого анализа продуктов мейотической рекомбинации. [ 27 ] Эти однокопийные амплификации, которые впервые были проведены во время характеристики Taq-полимеразы, [ 24 ] стало жизненно важным для изучения древней ДНК , а также генетического типирования предимплантированных эмбрионов.
В 1986 году Эдвард Блейк, судмедэксперт, работавший в здании Cetus, сотрудничал с Генри Эрлихом, исследователем Cetus, чтобы применить ПЦР для анализа доказательств уголовных преступлений. Панель образцов ДНК из старых случаев была собрана, закодирована и проанализирована Сайки вслепую с использованием анализа HLA DQα. Когда код был взломан, все улики и преступники совпали. Группа Блейка и Эрлиха почти сразу же применила эту технику в деле Пенсильвания против Пестиникаса . [ 28 ] первое применение ПЦР в уголовном деле. Этот тест DQα разработан компанией Cetus как один из их наборов «Ampli-Type» и стал частью ранних протоколов проверки судебно-медицинских доказательств, например, в деле об убийстве О. Дж. Симпсона .
К 1989 году Алек Джеффрис , который ранее разработал и применил первые тесты по дактилоскопии ДНК , применил ПЦР для повышения их чувствительности. [ 29 ] После дальнейшей модификации амплификация высокополиморфных локусов тандемных повторов с вариабельным числом (VNTR) стала стандартным протоколом для национальных баз данных ДНК, таких как Объединенная система индексов ДНК (CODIS).
В 1987 году Рассу Хигучи удалось амплифицировать ДНК человеческого волоса. [ 30 ] Эта работа расширилась за счет разработки методов амплификации ДНК из сильно деградированных образцов, таких как древняя ДНК и судебно-медицинские доказательства.
Кода
[ редактировать ]- журнал 22 декабря 1989 года Science наградил Taq-полимеразу (и ПЦР) своей первой «Молекулой года». Документ «Taq PCR» [ 24 ] стала на несколько лет самой цитируемой публикацией по биологии.
- После публикации первой статьи о ПЦР [ 16 ] Правительство Соединенных Штатов направило Рэнди Сайки суровое письмо, упрекая его за публикацию отчета о «цепных реакциях» без необходимого предварительного рассмотрения и одобрения Министерства энергетики США . Цет ответил, объяснив разницу между ПЦР и атомной бомбой . [ нужна ссылка ]
- Cetus 23 июля 1991 года объявила о своей продаже соседней биотехнологической компании Chiron . В рамках продажи права на патенты на ПЦР были проданы за 300 миллионов долларов США компании Hoffman-La Roche (которая в 1989 году купила ограниченные права на ПЦР). Многие исследователи Cetus PCR перешли в дочернюю компанию Roche Molecular Systems .
- Кэри 13 октября 1993 года Маллис , покинувший Cetus в 1986 году , был удостоен Нобелевской премии по химии . Утром своей благодарственной речи [ 1 ] он чуть не был арестован шведскими властями за «ненадлежащее использование лазерной указки». [ 31 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д Нобелевская лекция Кэри Маллиса, 8 декабря 1993 г.
- ^ Jump up to: а б с д и Рабинов, Пол (1996). Создание ПЦР: история биотехнологии . Издательство Чикагского университета. ISBN 978-0-226-70146-2 . [ нужна страница ]
- ^ Уотсон Дж.Д., Крик FHC «Структура нуклеиновой кислоты дезоксирибозы», Nature vol. 171, стр. 737–738 (1953). [1]
- ^ (Открытие Артуром Корнбергом ДНК-полимеразы I) J. Biol. хим. том. 280, с. 46. [2]
- ^ Леман, И.Р., Бессман М.Дж., Симмс Э.С., Корнберг А. «Ферментативный синтез дезоксирибонуклеиновой кислоты. I. Получение субстратов и частичная очистка фермента из Escherichia coli» J. Biol. хим. том. 233 (1), стр. 163–170 (1958).
- ^ Хорана Х.Г. и др. «Тотальный синтез структурного гена предшественника тирозин-супрессорной транспортной РНК из Escherichia coli. 1. Общее введение» J. Biol. хим. том. 251 (3), стр. 565–70 (1976).
- ^ Брок Т.Д., Freeze H «Thermus aquaticus, экстремальный термофил, не образующий спор», J. Bacteriol. том. 98 (1), стр. 289–297 (1969).
- ^ Кленов Х. и Хеннингсен I «Селективное устранение экзонуклеазной активности полимеразы дезоксирибонуклеиновой кислоты из Escherichia coli B путем ограниченного протеолиза» Proc Natl Acad Sci vol. 65 стр. 168–75 (1970).
- ^ Jump up to: а б Панет А., Хорана Х.Г. «Исследования полинуклеотидов» J. Biol. хим. том. 249 (16), стр. 5213–21 (1974).
- ^ Jump up to: а б Клеппе К., Оцука Э., Клеппе Р., Молино И., Корана Х.Г. «Исследования полинуклеотидов. XCVI. Репликация коротких синтетических ДНК, катализируемая ДНК-полимеразами». Дж. Молек. Биол. том. 56, стр. 341–61 (1971).
- ^ Муллис КБ, Ферре Ф., Гиббс Р.А. "Полимеразная цепная реакция" Birkhäuser Press (1994) ISBN 0-8176-3750-8
- ^ Jump up to: а б Чиен А., Эдгар Д.Б., Трела Дж.М. «Полимераза дезоксирибонуклеиновой кислоты из крайних термофилов Thermus aquaticus» J. Bacteriol. том. 174 стр. 1550–1557 (1976).
- ^ Сэнгер Ф., Никлен С., Коулсон А.Р. «Секвенирование ДНК с ингибиторами обрыва цепи» Proc Natl Acad Sci vol. 74 (12), стр. 5463–7 (1977).
- ^ Jump up to: а б с Муллис КБ «Необычное происхождение полимеразной цепной реакции» Scientific American, vol. 262, стр. 56–65 (апрель 1990 г.).
- ^ Jump up to: а б с д и Шарф, Стивен; Хорн, Гленн; Эрлих, Генри (5 сентября 1986 г.). «Прямое клонирование и анализ последовательностей ферментативно амплифицированных геномных последовательностей» . Наука . 233 (4768): 1076–8. дои : 10.1126/science.3461561 . ПМИД 3461561 . Проверено 8 февраля 2024 г.
- ^ Jump up to: а б с Сайки Р.К. и др. «Ферментативная амплификация геномных последовательностей β-глобина и анализ сайтов рестрикции для диагностики серповидноклеточной анемии» Science vol. 230 стр. 1350–54 (1985).
- ^ Муллис КБ «Процесс амплификации последовательностей нуклеиновых кислот». Патент США 4683202 .
- ^ Муллис, КБ и др. «Процесс амплификации, обнаружения и/или клонирования последовательностей нуклеиновых кислот». Патент США 4683195 .
- ^ Jump up to: а б Сайки и др. «Анализ ферментативно амплифицированной ДНК β-глобина и HLA DQα с помощью аллель-специфичных олигонуклеотидных зондов». Природа об. 324 (6093), стр. 163–6 (1986).
- ^ Сайки, Р. и др. «Новый метод пренатальной диагностики серповидноклеточной анемии», Amer. Соц. Генетика человека, 9–13 октября 1985 г.
- ^ Муллис КБ и др. «Специфическая ферментативная амплификация ДНК in vitro: полимеразная цепная реакция». Холодный источник Харб. Симп. Квант. Биол. том. 51 стр. 263–73 (1986).
- ^ Муллис КБ и Фалуна Ф.А. «Специфический синтез ДНК in vitro посредством цепной реакции, катализируемой полимеразой». Методы энзимологии, том. 155(F), стр. 335–50 (1987).
- ^ Верлаан-де Врис М и др. «Процедура дот-блот-скрининга мутировавших онкогенов ras с использованием синтетических олигодезоксинуклеотидов». Джин об. 50(1–3) стр. 313–20 (1986).
- ^ Jump up to: а б с Сайки и др. «Праймер-направленная ферментативная амплификация ДНК с помощью термостабильной ДНК-полимеразы». Наука том. 239 стр. 487–91 (1988).
- ^ Муллис, КБ и др. «Процесс амплификации, обнаружения и/или клонирования последовательностей нуклеиновых кислот с использованием термостабильного фермента». Патент США 4965188 .
- ^ Квок С и др. «Идентификация последовательностей ВИЧ с помощью ферментативной амплификации in vitro и обнаружения расщепления олигомеров». Дж. Вирол. том. 61 (5), стр. 1690–4 (1987).
- ^ Boehnke M et al. «Генетическое картирование тонкой структуры хромосом человека с использованием полимеразной цепной реакции на одиночном сперматозоиде». Am J Hum Genet vol. 45 (1), стр. 21–32 (1989).
- ^ «Хронология судебно-медицинской экспертизы (PDF)» (PDF) . Архивировано из оригинала (PDF) 9 июля 2008 г. Проверено 12 апреля 2008 г.
- ^ Джеффрис А. и др. «Усиление человеческих миниспутников». Исследования нуклеиновых кислот, том. 23 стр. 10953-71 (1988).
- ^ Хигучи Р. и др. «Типирование ДНК по одиночным волоскам». Природа об. 332 (6164), стр. 543–6 (1988).
- ^ Mullis KB "Танцы обнаженными в поле разума" Pantheon Books (1998) ISBN 0-679-44255-3