Динитрогенный комплекс переходного металла


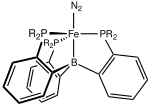
Комплексы переходного металла с азотом представляют собой координационные соединения , содержащие переходные металлы в качестве ионных центров и молекулы азота (N 2 ) в качестве лигандов . [2]
Историческая справка
[ редактировать ]Комплексы переходных металлов N 2 изучаются с 1965 года, когда Аллен и Сенофф сообщили о первом комплексе. [3] Этот диамагнитный комплекс [Ru(NH 3 ) 5 (N 2 )] 2+ , синтезирован из гидразингидрата и трихлорида рутения и состоит из [Ru(NH 3 ) 5 ] 2+ центр прикреплен к одному концу N 2 . [4] [5] Существование N 2 в качестве лиганда в этом соединении было идентифицировано по ИК-спектру с сильной полосой в районе 2170–2100 см-1. −1 . [4] В 1966 году молекулярная структура [Ru(NH 3 ) 5 (N 2 )]Cl 2 была определена Боттомли и Нюбургом методом рентгеновской кристаллографии . [6]
Диназотный комплекс транс- [IrCl(N 2 )(PPh 3 ) 2 ] получают обработкой комплекса Васки ароматическими ацилазидами . Имеет плоскую геометрию. [7]
О первом получении комплекса металл-диазот с использованием динитрога сообщили в 1967 году Ямамото и его коллеги. Они получили [Co(H)(N 2 )(PPh 3 ) 3 ] восстановлением Co(acac) 3 с помощью AlEt 2 OEt в атмосфере N 2 . Содержащий как гидридо, так и лиганды N 2 , комплекс потенциально имел отношение к фиксации азота. [8]
С конца 1960-х годов были получены различные комплексы переходного металла с азотом, в том числе с железом, [9] молибден [10] и ванадий [11] как металлоцентры. Интерес к таким комплексам возникает потому, что N 2 составляет большую часть атмосферы и многие полезные соединения содержат азот. Биологическая фиксация азота , вероятно, происходит посредством связывания N 2 с металлическими центрами фермента нитрогеназы , за которым следует ряд стадий, включающих перенос электронов и протонирование . [12]
Режимы склеивания
[ редактировать ]С точки зрения связи с переходными металлами N 2 связан с CO и ацетиленом, поскольку все три соединения имеют тройные связи . Охарактеризованы различные способы соединения. В зависимости от того, являются ли молекулы N 2 общими еще для двух металлоцентров, комплексы можно разделить на моноядерные и мостиковые. В зависимости от геометрического соотношения между молекулой N 2 и металлическим центром комплексы можно разделить на типы «конец» или «бок». В режимах связи с торца комплексов переходного металла с азотом вектор NN можно рассматривать на одной линии с центром иона металла, тогда как в режимах с боковым расположением связь металл-лиганд, как известно, перпендикулярна вектору NN. . [13]
Мононуклеарный, концевой
[ редактировать ]В качестве лиганда N 2 обычно связывается с металлами как «концевой» лиганд, как показано [Ru(NH 3 ) 5 N 2 ] 2+ . Такие комплексы обычно аналогичны родственным производным CO. Эту связь иллюстрирует пара комплексов IrCl(CO)(PPh 3 ) 2 и IrCl(N 2 )(PPh 3 ) 2 . [14] В этих моноядерных случаях N 2 выступает как σ-донором, так и π-акцептором. Валентные углы MNN близки к 180°. [2] N 2 является более слабым пи-акцептором, чем CO, что отражает природу π*-орбиталей CO по сравнению с N 2 . По этой причине существует мало примеров комплексов, содержащих как N 2 CO, так и лиганд .
Комплексы переходного металла с азотом могут содержать более одного N 2 в качестве «концевых» лигандов, например мер- [Mo(N 2 ) 3 (PPr н 2 Ph) 3 ], имеющий октаэдрическую геометрию. [15] В другом примере динитрогенный лиганд в Mo(N 2 ) 2 (Ph 2 PCH 2 CH 2 PPh 2 ) 2 может быть восстановлен с получением аммиака. [16] Поскольку многие нитрогеназы содержат Mo, особый интерес вызывают комплексы Mo- N2 .
Перемычка, окончание
[ редактировать ]N 2 также служит мостиковым лигандом, связывающимся «концом» с двумя металлическими центрами, как показано {[Ru(NH 3 ) 5 ] 2 (μ-N 2 )} 4+ . Эти комплексы еще называют многоядерными диазотными комплексами. В отличие от своего моноядерного аналога их можно получать как из ранних, так и из поздних переходных металлов. [2]
В 2006 году исследование комплексов железа с азотом, проведенное Холландом и его коллегами, показало, что связь N–N значительно ослабляется при комплексообразовании с атомами железа с низким координационным числом. В состав комплекса входят бидентатно-хелатирующие лиганды, присоединенные к атомам железа в ядре Fe-N-N-Fe, в котором N 2 выступает в качестве мостикового лиганда между двумя атомами железа. Увеличение координационного числа железа за счет модификации хелатирующих лигандов и добавления еще одного лиганда на атом железа показало увеличение прочности связи N–N в образующемся комплексе. Таким образом, предполагается, что Fe в среде с низкой координацией является ключевым фактором фиксации азота ферментом нитрогеназой , поскольку его кофактор Fe-Mo также содержит Fe с низкими координационными числами. [17]
Средняя длина связи этих комплексов диазота с мостиком-концом составляет около 1,2 Å. В некоторых случаях длина связи может достигать 1,4 Å, что аналогично длине одинарных связей NN. [18] Хасанайн и его коллеги показали, что структуры Льюиса мостиковых комплексов можно определить на основе занятости π-молекулярных орбиталей по аналогии с простыми тетратомными органическими молекулами. Например, ядра N 2 -мостиковых комплексов с 8, 10 или 12 π-электронами обычно можно сформулировать соответственно как M≡NN≡M, M=N=N=M и MN≡NM по аналогии с органические молекулы с 8, 10 и 12 π-электронами HC≡CC≡CH, O=C=C=O и FC≡CF. [19]
Мононуклеарный, боковой
[ редактировать ]По сравнению со своим боковым аналогом моноядерные боковые динитрогенные комплексы обычно имеют более высокую энергию и примеры их редки. Динитроген действует как π-донор в комплексах такого типа. Фомичев и Коппенс сообщили о первых кристаллографических доказательствах боковой координации N 2 с одним металлическим центром в фотоиндуцированном метастабильном состоянии. При обработке УФ-светом комплекс переходного металла с азотом [Os(NH 3 ) 5 (N 2 )] 2+ в твердом состоянии может переходить в метастабильное состояние [Os(NH 3 ) 5 (η 2 -N 2 )] 2+ , где вибрация динитрогена сместилась с 2025 до 1831 см −1 .
Считается, что некоторые другие примеры существуют в переходных состояниях изомеризации внутримолекулярных связей. Армор и Таубе сообщили об этой изомеризации, используя 15 N-меченый диазот в качестве лигандов. [20]
Перемычка, боковая
[ редактировать ]Известны биметаллические комплексы второго способа образования мостиков, в которых вектор NN перпендикулярен вектору MM, что можно рассматривать как боковой способ. Одним из примеров является [(η 5 -C 5 Me 4 H) 2 Zr] 2 ( µ 2 , n 2 ,или 2 -Н 2 ). [21] Диметаллический комплекс может реагировать с H 2 для достижения искусственной фиксации азота за счет восстановления N 2 . [22] Родственный комплекс тетрагидрида дитантала также может восстанавливать N 2 . [23]
Реактивность
[ редактировать ]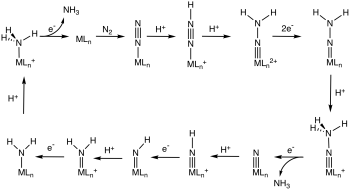
Расщепление до нитридов
[ редактировать ]При получении нитридокомплексов металлов из N2 предполагается промежуточное положение диазотного комплекса.Некоторые комплексы Mo(III) также расщепляют N 2 : [24]
- 2 Mo(NR 2 ) 3 + N 2 → (R 2 N) 3 Mo-N 2 -Mo(NR 2 ) 3
- (R 2 N) 3 Mo-N 2 -Mo(NR 2 ) 3 → 2 N≡Mo(NR 2 ) 3
Атака электрофилов
[ редактировать ]Некоторые богатые электронами комплексы металла и азота чувствительны к атаке электрофилов на азот. Когда электрофилом является протон, реакция представляет интерес в контексте абиологической фиксации азота . Некоторые комплексы металл-дитроген даже катализируют гидрирование N 2 до аммиака в цикле, включающем N-протонирование восстановленного комплекса MN 2 . [25] [26]
См. также
[ редактировать ]- Абиологическая фиксация азота
- Активация динитрогена, опосредованная элементами основной группы
- Нитридный комплекс переходного металла
Ссылки
[ редактировать ]- ^ Чалкли, Мэтью Дж.; Дровер, Маркус В.; Питерс, Джонас К. (2020). «Каталитическая конверсия N 2 - в NH 3 (или -N 2 H 4 ) с помощью четко определенных молекулярных координационных комплексов» . Химические обзоры . 120 (12): 5582–5636. doi : 10.1021/acs.chemrev.9b00638 . ПМЦ 7493999 .
- ^ Jump up to: а б с д Ёсиаки Нишибаяси, изд. (2019). Комплексы переходного металла с азотом: получение и реакционная способность . Вайли-ВЧ. ISBN 978-3-527-34425-3 .
- ^ Сенофф, Цезарь В. (1990). «Открытие [Ru(NH 3 ) 5 N 2 ] 2+ : Случай случайности и научного метода». Журнал химического образования . 67 (5): 368. Бибкод : 1990JChEd..67..368S . doi : 10.1021/ed067p368 .
- ^ Jump up to: а б А.Д. Аллен; К.В. Сенофф (1965). «Комплексы азотопентамминрутения (II)». Журнал Химического общества, Chemical Communications (24): 621. doi : 10.1039/C19650000621 .
- ^ Фрызук, Майкл Д. (2013). «Координация N 2 ». хим. Коммун . 49 (43): 4866–4868. дои : 10.1039/C3CC42001A . ПМИД 23609888 .
- ^ Боттомли, Ф.; Нюбург, Южная Каролина (15 октября 1968 г.). «Молекулярный азот как лиганд. Кристаллическая структура дихлорида азотпентаамминрутения(II) и родственных солей» . Acta Crystallographica Раздел B. 24 (10): 1289–1293. дои : 10.1107/S056774086800419X . ISSN 0567-7408 .
- ^ Коллман, Джеймс П.; Кубота, Мицуру.; Вастин, Фредерик Д.; Сунь, Цзюй Юань; Канг, Юнг В. (сентябрь 1968 г.). «Иридиевые комплексы молекулярного азота». Журнал Американского химического общества . 90 (20): 5430–5437. дои : 10.1021/ja01022a018 . ISSN 0002-7863 .
- ^ Ямамото, Акио; Китадзуме, Сёдзи; Пу, Лён Сунь; Икеда, Сакудзи (январь 1971 г.). «Синтез и свойства гидридодинтрогентрис(трифенилфосфин)кобальта(I) и родственных фосфин-кобальтовых комплексов». Журнал Американского химического общества . 93 (2): 371–380. дои : 10.1021/ja00731a012 . ISSN 0002-7863 .
- ^ Ареста, М.; Джанноккаро, П.; Росси, М.; Сакко, А. (1 марта 1971 г.). «Азотфиксация.: II. Динитрог-комплексы железа». Неорганика Химика Акта . 5 : 203–206. дои : 10.1016/S0020-1693(00)95914-0 . ISSN 0020-1693 .
- ^ Хидай, М.; Томинари, К.; Учида, Ю.; Мисоно, А. (1969). «Комплекс молибдена, содержащий молекулярный азот». Журнал Химического общества D: Chemical Communications (14): 814. doi : 10.1039/c29690000814 . ISSN 0577-6171 .
- ^ Сон, Чжэ Ин; Гамбаротта, Сандро (октябрь 1996 г.). «Получение, характеристика и реакционная способность диамагнитного нитрида ванадия». Химия - Европейский журнал . 2 (10): 1258–1263. дои : 10.1002/chem.19960021012 . ISSN 0947-6539 .
- ^ Ли, Цзяньхао; Ю, Чао; Си, Чжэньфэн (2017). преобразование N2 в N-содержащие органические соединения» . « на китайском языке) ( Прямое .дои / : 10.6023 . ISSN 0567-7351 a17040170
- ^ Фрызук, Майкл Д. (20 января 2009 г.). «Боковой связанный азот: режим активированного связывания, который облегчает функционализацию молекулярного азота». Отчеты о химических исследованиях . 42 (1): 127–133. дои : 10.1021/ar800061g . ISSN 0001-4842 . ПМИД 18803409 .
- ^ Коллман, JP; Хоффман, Северо-Запад; Хоскинг, JW (2000). транс -Хлор(азот)бис(трифенилфосфин)иридий (I) . Неорганические синтезы. Том. 12. С. 8–11. дои : 10.1002/9780470132432.ch2 . ISBN 978-0-470-13171-8 .
- ^ Андерсон, С.Н.; Хьюз, Д.Л.; Ричардс, Р.Л. (1984). «Трис-динитрогенный комплекс. Получение и кристаллическая структура мер- [Mo(N 2 ) 3 (PPr н 2 Ph) 3 ]». Журнал Химического общества, Chemical Communications (15): 958–959. doi : 10.1039/C39840000958 .
- ^ Современная координационная химия: наследие Джозефа Чатта» Г. Дж. Ли, Северо-Западный Винтертон Спрингер Верлаг (2002). ISBN 0-85404-469-8
- ^ Смит, Джереми М.; Садик, Азвана Р.; Кундари, Томас Р.; Роджерс, Кентон Р.; Лукат-Роджерс, Гудрун; Лашикотт, Рене Дж.; Флашенрим, Кристин Дж.; Вела, Хавьер; Холланд, Патрик Л. (1 января 2006 г.). «Исследование низкокоординированных железо-диазотных комплексов» . Журнал Американского химического общества . 128 (3): 756–769. дои : 10.1021/ja052707x . ISSN 0002-7863 . ПМИД 16417365 .
- ^ Фрызук, Майкл Д.; Хаддад, ТС; Милваганам, Муругесапиллай; МакКонвилл, Дэвид Х.; Реттиг, Стивен Дж. (1 апреля 1993 г.). «Концевое и боковое соединение динитрога с биядерными комплексами ранних переходных металлов». Журнал Американского химического общества . 115 (7): 2782–2792. дои : 10.1021/ja00060a028 . ISSN 0002-7863 .
- ^ Хасанайн, Фарадж; Холланд, Патрик Л.; Голдман, Алан С.; Миллер, Александр Дж. М. (16 февраля 2023 г.). «Структуры Льюиса и классификация связей мостиковых комплексов азотистых переходных металлов с торца» . Журнал Американского химического общества . дои : 10.1021/jacs.2c12243 . ISSN 0002-7863 . ПМЦ 9983020 .
- ^ Армор, Джон Н.; Таубе, Генри. (апрель 1970 г.). «Изомеризация связей в меченном азотом [Ru(NH3)5N2]Br2». Журнал Американского химического общества . 92 (8): 2560–2562. дои : 10.1021/ja00711a066 . ISSN 0002-7863 .
- ^ Бернскоеттер, штат Вашингтон; Лобковский Е.; Чирик, П.Дж. (2005). «Кинетика и механизм гидрирования N 2 в бис(циклопентадиенил)циркониевых комплексах и функционализация азота 1,2-присоединением насыщенной связи CH». Журнал Американского химического общества . 127 (40): 14051–14061. дои : 10.1021/ja0538841 . ПМИД 16201827 .
- ^ Пул, Хайме А.; Лобковский, Эмиль; Чирик, Пол Дж. (2004). «Гидрирование и расщепление диазота до аммиака циркониевым комплексом». Природа . 427 (6974): 527–530. Бибкод : 2004Natur.427..527P . дои : 10.1038/nature02274 . ПМИД 14765191 . S2CID 4379465 .
- ^ Фрызук, Майкл Д. (20 сентября 2008 г.). «Боковой связанный азот: режим активированного связывания, который облегчает функционализацию молекулярного азота». Отчеты о химических исследованиях . 42 (1): 127–133. дои : 10.1021/ar800061g . ПМИД 18803409 .
- ^ Лаплаза, Каталина Э.; Джонсон, Марк Дж.А.; Питерс, Джонас К.; Одом, Аарон Л.; Ким, Эстер; Камминс, Кристофер С.; Джордж, Грэм Н.; Пикеринг, Ингрид Дж. (1996). «Расщепление динитрогена трехкоординационными комплексами молибдена (III): механистические и структурные данные1». Журнал Американского химического общества . 118 (36): 8623–8638. дои : 10.1021/ja960574x .
- ^ Яндулов Дмитрий В.; Шрок, Ричард Р. (4 июля 2003 г.). «Каталитическое восстановление азота до аммиака в едином молибденовом центре». Наука . 301 (5629): 76–78. Бибкод : 2003Sci...301...76Y . дои : 10.1126/science.1085326 . ISSN 0036-8075 . ПМИД 12843387 . S2CID 29046992 .
- ^ Арашиба, Казуя; Мияке, Ёсихиро; Нишибаяси, Ёсиаки (2011). «Комплекс молибдена, содержащий клещевые лиганды типа PNP, приводит к каталитическому восстановлению динитрогена в аммиак». Природная химия . 3 (2): 120–125. Бибкод : 2011НатЧ...3..120А . дои : 10.1038/nchem.906 . ПМИД 21258384 .