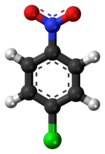
4-Нитрохлорбензол
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
1-хлор-4-нитробензол | |||
| Другие имена
4-Хлор-1-нитробензол
4-хлорнитробензол п -Нитрохлорбензол ПНКБО | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.002.554 | ||
| КЕГГ | |||
ПабХим CID
|
|||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 6 Н 4 Cl NO 2 | |||
| Молярная масса | 157.55 g·mol −1 | ||
| Появление | Светло-желтое твердое вещество | ||
| Запах | сладкий [ 1 ] | ||
| Плотность | 1,52 г/см 3 (20 °С) | ||
| Температура плавления | 83,6 ° С (182,5 ° F; 356,8 К) | ||
| Точка кипения | 242,0 ° С (467,6 ° F; 515,1 К) | ||
| нерастворимый | |||
| Растворимость в других растворителях | Растворим в толуоле, эфире, ацетоне, горячем этаноле. | ||
| Давление пара | 0,2 мм рт.ст. (30°С) [ 1 ] | ||
| Опасности | |||
| точка возгорания | 12 ° C (54 ° F; 285 К) | ||
| Летальная доза или концентрация (LD, LC): | |||
ЛД 50 ( средняя доза )
|
812 мг/кг (крыса, перорально) 1414 мг/кг (мыши, перорально) 440 мг/кг (мыши, перорально) 420 мг/кг (крыса, перорально) [ 1 ] | ||
ЛК 50 ( средняя концентрация )
|
164 мг/м 3 (кот, 7 часов) [ 1 ] | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
ПЭЛ (допустимо)
|
СВВ 1 мг/м 3 [кожа] [ 1 ] | ||
РЕЛ (рекомендуется)
|
Что [ 1 ] | ||
IDLH (Непосредственная опасность)
|
Са [100 мг/м 3 ] [ 1 ] | ||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
4-Нитрохлорбензол – органическое соединение формулы ClC 6 H 4 NO 2 . Это бледно-желтое твердое вещество. 4-Нитрохлорбензол является распространенным промежуточным продуктом в производстве ряда промышленно полезных соединений, включая антиоксиданты, обычно встречающиеся в каучуке . Другие изомеры формулы ClC 6 H 4 NO 2 включают 2-нитрохлорбензол и 3-нитрохлорбензол.
Подготовка
[ редактировать ]4-Нитрохлорбензол получают в промышленности нитрованием хлорбензола :
- ClC 6 H 5 + HNO 3 → ClC 6 H 4 NO 2 + H 2 O
Эта реакция дает как 2-, так и 4-нитропроизводные в соотношении примерно 1:2. Эти изомеры разделяют сочетанием кристаллизации и перегонки. [ 2 ] 4-Нитрохлорбензол был первоначально получен нитрованием 4 -бромхлорбензола Холлеманом и его сотрудниками. [ 3 ]
Приложения
[ редактировать ]4-Нитрохлорбензол является промежуточным продуктом при получении множества производных. Нитрование дает 2,4-динитрохлорбензол и 3,4-дихлорнитробензол . Восстановление металлическим железом дает 4-хлоранилин . Электроноакцепторная природа присоединенной нитрогруппы делает бензольное кольцо особенно восприимчивым к нуклеофильному ароматическому замещению , в отличие от родственного хлорбензола. Таким образом, сильные нуклеофилы гидроксид, метоксид , фторид и амид вытесняют хлорид с образованием соответственно 4-нитрофенола , 4-нитроанизола, 4-фторнитробензола и 4-нитроанилина . [ 2 ] [ 4 ]
Другое применение 4-нитрохлорбензола — его конденсация с анилином с получением 4-нитродифениламина. Восстановительное алкилирование нитрогруппы дает вторичные ариламины, которые являются полезными антиоксидантами для каучука.
Безопасность
[ редактировать ]США Национальный институт безопасности и гигиены труда считает 4-нитрохлорбензол потенциальным профессиональным канцерогеном. [ 5 ] Управлением по охране труда установлено предельно допустимая концентрация 1 мг/м. 3 Американская конференция правительственных специалистов по промышленной гигиене рекомендует предельно допустимую концентрацию в воздухе 0,64 мг/м. 3 в среднем за восемь часов. [ 6 ] [ 7 ]
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г Карманный справочник NIOSH по химическим опасностям. «#0452» . Национальный институт охраны труда и здоровья (NIOSH).
- ^ Перейти обратно: а б с Джеральд Бут (2007). «Нитросоединения ароматические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a17_411 . ISBN 978-3527306732 .
- ^ «Нитрование смешанных дигалогенбензолов» Сборник химических предприятий Нидерландов и Бельгии. Амстердам, 1915 год; стр. 204-235.
- ^ Брюстер, Рэй К.; Гренинг, Теодор (1934). «п-Нитродифениловый эфир». Органические синтезы . 14:66 . дои : 10.15227/orgsyn.014.0066 .
- ^ CDC - Непосредственно опасные для жизни и здоровья концентрации (IDLH): п-нитрохлорбензол.
- ^ CDC - Карманный справочник NIOSH по химическим опасностям
- ^ Департамент здравоохранения и обслуживания пожилых людей Нью-Джерси - Информационный бюллетень об опасных веществах