ПЛГА
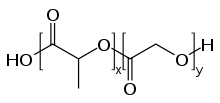
PLGA , PLG или поли(молочная- ко -гликолевая) кислота ( CAS : 26780-50-7 ) представляет собой сополимер , который используется во множестве терапевтических устройств, одобренных Управлением по контролю за продуктами и лекарствами (FDA), благодаря своей биоразлагаемости и биосовместимости. . [ 1 ] PLGA синтезируется посредством сополимеризации с раскрытием цикла двух разных мономеров , циклических димеров (1,4-диоксан-2,5-дионов) гликолевой кислоты и молочной кислоты . Полимеры могут быть синтезированы как в виде статистических, так и в виде блок-сополимеров, что придает полимеру дополнительные свойства. Обычные катализаторы, используемые при получении этого полимера, включают 2-этилгексаноат олова (II) олова (II) , алкоксиды или изопропоксид алюминия . Во время полимеризации последовательные мономерные звенья (гликолевой или молочной кислоты) соединяются в PLGA сложноэфирными связями линейный алифатический полиэфир . , образуя в качестве продукта [ 2 ]
Сополимер
[ редактировать ]В зависимости от соотношения лактида и гликолида, используемого для полимеризации, могут быть получены различные формы PLGA: их обычно идентифицируют по молярному соотношению используемых мономеров (например, PLGA 75:25 идентифицирует сополимер, состав которого составляет 75% молочной кислоты). кислота и 25% гликолевая кислота). Кристалличность PLGA будет варьироваться от полностью аморфной до полностью кристаллической в зависимости от блочной структуры и молярного соотношения. PLGA обычно имеют температуру стеклования в диапазоне 40–60 °C. PLGA можно растворять в широком спектре растворителей , в зависимости от состава. Полимеры с более высоким содержанием лактида можно растворить с использованием хлорированных растворителей, тогда как материалы с более высоким содержанием гликолида потребуют использования фторированных растворителей, таких как HFIP .
PLGA разлагается за счет гидролиза сложноэфирных связей в присутствии воды . Показано, что время деградации PLGA связано с соотношением мономеров, используемых в производстве: чем выше содержание гликолидных звеньев, тем меньше время, необходимое для деградации по сравнению с преимущественно лактидными материалами. Исключением из этого правила является сополимер с соотношением мономеров 50:50, который разлагается быстрее (около двух месяцев). Кроме того, полимеры, концевые группы которых блокированы сложными эфирами (в отличие от свободной карбоновой кислоты ), демонстрируют более длительный период полураспада. [ 3 ] Такая гибкость деградации сделала его удобным для изготовления многих медицинских устройств , таких как трансплантаты , шовный материал , имплантаты , протезы , пленки хирургического герметика, микро- и наночастицы . [ 4 ]
PLGA подвергается гидролизу в организме с образованием исходных мономеров: молочной кислоты и гликолевой кислоты. Эти два мономера в нормальных физиологических условиях являются побочными продуктами различных метаболических путей в организме. Молочная кислота метаболизируется в цикле трикарбоновых кислот и выводится через углекислый газ и воду . Гликолевая кислота метаболизируется таким же образом, а также выводится через почки. [ 5 ] Организм также может метаболизировать два мономера, что в случае с гликолевой кислотой производит небольшие количества токсичной щавелевой кислоты , хотя количества, образующиеся при обычном применении, незначительны, и существует минимальная системная токсичность, связанная с использованием PLGA для применения в биоматериалах . Однако сообщалось, что кислотная деградация PLGA снижает локальный pH до настолько низкого уровня, что создается автокаталитическая среда. [ 6 ] Было показано, что pH внутри микросферы может достигать 1,5. [ 7 ]
Биосовместимость
[ редактировать ]Обычно PLGA считается вполне биосовместимым. Его высокая биосовместимость обусловлена его составом, обусловленным ферментацией молочной и гликолевой кислот из сахаров, что делает их экологически чистыми и менее реактивными в организме. [ 8 ] PLGA также разлагается на нетоксичные и нереактивные продукты, что делает их весьма полезными для различных медицинских и фармацевтических применений.
Биосовместимость PLGA была протестирована как in vivo, так и in vitro. [ 9 ] Биосовместимость этого полимера обычно определяется продуктами, на которые он разлагается, а также скоростью распада на продукты разложения. Разложение PLGA происходит с помощью фермента, известного как эстераза , который образует молочную кислоту и гликолевую кислоту. Эти кислоты затем подвергаются циклу Кребса , где разлагаются на углекислый газ (CO 2 ) и воду ( Н 2 О ). [ 10 ] Эти побочные продукты затем удаляются из организма посредством клеточного дыхания и процесса пищеварения.
Хотя побочные продукты обычно не накапливаются в организме, бывают случаи, когда эти побочные продукты (молочная и гликолевая кислоты) могут быть опасны для организма при накоплении в высоких локальных концентрациях. [ 11 ] Также могут оставаться небольшие кусочки полимеров по мере их разложения, вызывая иммунный ответ макрофагов . Эти побочные эффекты можно уменьшить, используя более низкие концентрации полимера, чтобы он естественным образом высвобождался по всему организму.
Что еще следует учитывать в отношении биосовместимости PLGA, так это место, в котором полимер имплантируется или помещается в организм. В зависимости от того, где находится полимер, организм может иметь разные иммунные реакции. Например, в системах доставки лекарств (DDS) имплантаты PLGA и PLA с большой площадью поверхности и малым объемом инъекции могут увеличить вероятность иммунного ответа, поскольку полимеры разлагаются в организме.
Биоразлагаемость
[ редактировать ]Биодеградация PLGA делает его полезным во многих медицинских практиках. PLGA подвергается объемной деградации, то есть, когда катализатор, такой как вода, проникает в матрицу полимера. [ 12 ] Соотношение лактида и гликолида PLGA 75:25 может быть получено в виде микросфер, которые разлагаются в результате объемной эрозии. [ 12 ] Это обеспечивает равномерную деградацию по всему полимеру.
Другая инъекционная форма PLGA была разработана для разрушения систем. Эту форму можно использовать в Lupron Depot . Для этого PLGA смешивают с органическим растворителем, смешивающимся с водой, одобренным Управлением по контролю за продуктами и лекарствами (FDA). После смешивания PLGA с растворителем с выбранным лекарственным средством образуется гомогенный раствор или суспензия. При впрыскивании этой смеси PLGA затвердевает из-за нерастворимости в воде и заменяется водой. Медленно препарат выводится из раствора. Проблема, которая может возникнуть, заключается в том, что во время первоначальной инъекции лекарство может высвобождаться быстрыми порциями, а не постепенно. [ 12 ]
Примеры
[ редактировать ]Конкретные примеры использования PLGA включают:
- Синтетическая барьерная мембрана от Powerbone: Это устройство представляет собой рассасывающуюся синтетическую мембрану, которая действует как альтернатива политетрафторэтилену (ПТФЭ), который представляет собой синтетический полимер, часто используемый в зубных имплантатах и во многих других целях. [ 13 ] Синтетическая барьерная мембрана используется специально в зубных имплантатах и для направленной регенерации тканей (GTR), а также направленной регенерации кости (GBE). [ 14 ] Некоторые из них являются биоразлагаемыми мембранами, а другие нет, и обычно они связаны с большим количеством хирургических осложнений. В целом, эти мембраны важны для обеспечения биосовместимости, биобезопасности, барьерной функции и механических свойств имплантата. Они также обычно биоактивны, способствуя регенерации тканей вокруг места имплантации.
- Lupron Depot: это устройство для доставки лекарств, которое помогает лечить рак простаты и используется для лечения других типов подобных видов рака. Он также известен как лейпрорелин или лейпролид. PLGA используется в качестве ключевого компонента в этом препарате в форме микрочастиц для доставки препарата в организм в течение периода от 1 недели до 6 месяцев. [ 15 ] Этот препарат обычно используется в качестве альтернативы лучевой терапии и считается весьма эффективным, поскольку снижает уровень тестостерона в организме, замедляя последствия рака. [ 16 ] У этого препарата много побочных эффектов, включая потерю мышечной массы, приливы жара, усталость, остеопороз , рост ткани молочной железы и многие другие.
- Профилактическая доставка: это относится к профилактическому медицинскому обслуживанию, целью которого является предотвращение инфекций или других заболеваний. Одним из случаев профилактического родоразрешения с использованием PLGA является антибиотик ванкомицин, который обычно вводят после операции на головном мозге для предотвращения инфекций, вызванных бактериями, включая Staphylococcus aureus . [ 17 ]
См. также
[ редактировать ]- Поликапролактон
- Полигликолид
- Конъюгаты полимер-лекарственное средство
- Полимолочная кислота
- Поли-3-гидроксибутират
Ссылки
[ редактировать ]- ^ Абулатифех С.Р. (февраль 2023 г.). «Инъекционные депо PLGA/PLA длительного действия для ацетата лейпролида: успешный перенос от стенда к клинике». Доставка лекарств и трансляционные исследования . 13 (2): 520–530. дои : 10.1007/s13346-022-01228-0 . ПМИД 35976565 . S2CID 251622670 .
- ^ Астете С.Э., Саблиов С.М. (2006). «Синтез и характеристика наночастиц PLGA». Журнал биоматериаловедения. Полимерное издание . 17 (3): 247–289. дои : 10.1163/156856206775997322 . ПМИД 16689015 . S2CID 7607080 .
- ^ Самади Н., Аббадесса А., Ди Стефано А., ван Нострум К.Ф., Вермонден Т., Рахимиан С. и др. (декабрь 2013 г.). «Влияние лауриловой кэп-группы на высвобождение белка и деградацию частиц поли(D,L-молочной-когликолевой кислоты)». Журнал контролируемого выпуска . 172 (2): 436–443. дои : 10.1016/j.jconrel.2013.05.034 . ПМИД 23751568 .
- ^ Павот В., Берте М., Рессегье Ж., Легас С., Хандке Н., Гилберт С.К. и др. (декабрь 2014 г.). «Частицы поли(молочной кислоты) и поли(молочно-гликолевой кислоты) как универсальные платформы-носители для доставки вакцин». Наномедицина . 9 (17): 2703–2718. дои : 10.2217/nnm.14.156 . ПМИД 25529572 .
- ^ Кроттс Дж., Парк Т.Г. (2 июля 1998 г.). «Доставка белка из биоразлагаемых микросфер поли(молочной-ко-гликолевой кислоты): вопросы кинетики высвобождения и стабильности». Журнал микроинкапсуляции . 15 (6): 699–713. дои : 10.3109/02652049809008253 . ПМИД 9818948 .
- ^ Зольник Б.С., Берджесс-ди-джей (октябрь 2007 г.). «Влияние кислого pH на деградацию и высвобождение микросфер PLGA». Журнал контролируемого выпуска . 122 (3): 338–344. дои : 10.1016/j.jconrel.2007.05.034 . ПМИД 17644208 .
- ^ Фу К., Пак Д.В., Клибанов А.М., Лангер Р. (январь 2000 г.). «Визуальные свидетельства кислой среды внутри разлагающихся микросфер поли(молочно-гликолевой кислоты) (PLGA)». Фармацевтические исследования . 17 (1): 100–106. дои : 10.1023/А:1007582911958 . ПМИД 10714616 . S2CID 22378621 .
- ^ Эльмовафи Э.М., Тибони М., Солиман М.Е. (июль 2019 г.). «Биосовместимость, биодеградация и биомедицинское применение микро- и наночастиц поли(молочной кислоты)/поли(молочно-гликолевой кислоты)» . Журнал фармацевтических исследований . 49 (4): 347–380. дои : 10.1007/s40005-019-00439-x . ISSN 2093-6214 . S2CID 256338815 .
- ^ Мир М., Ахмед Н., Рехман А.У. (ноябрь 2017 г.). «Недавние применения наноструктур на основе PLGA для доставки лекарств». Коллоиды и поверхности. Б. Биоинтерфейсы . 159 : 217–231. дои : 10.1016/j.colsurfb.2017.07.038 . ПМИД 28797972 .
- ^ Мачачек Р., Лендлейн А. (март 2020 г.). «Фундаментальные сведения о деградации PLGA на основе исследований тонких пленок» . Журнал контролируемого выпуска . 319 : 276–284. дои : 10.1016/j.jconrel.2019.12.044 . ПМИД 31884098 . S2CID 209511941 .
- ^ Рамот И., Хаим-Зада М., Домб А.Дж., Ниска А. (декабрь 2016 г.). «Биосовместимость и безопасность PLA и его сополимеров». Обзоры расширенной доставки лекарств . Биоразлагаемые полимеры PLA. 107 : 153–162. дои : 10.1016/j.addr.2016.03.012 . ПМИД 27058154 .
- ^ Jump up to: а б с Внек Г.Е., Боулин Г.Л. (28 мая 2008 г.). Энциклопедия биоматериалов и биомедицинской инженерии . ЦРК Пресс. ISBN 978-1-4987-6143-7 .
- ^ «Синтетическая барьерная мембрана Powerbone (резорбирующая)» . Восстановление хирургическое . Проверено 30 апреля 2023 г.
- ^ Сасаки Дж.И., Абэ Г.Л., Ли А., Тонгтай П., Цубои Р., Коно Т., Имазато С. (май 2021 г.). «Барьерные мембраны для регенерации тканей в стоматологии» . Исследования биоматериалов в стоматологии . 8 (1): 54–63. дои : 10.1080/26415275.2021.1925556 . ПМЦ 8158285 . ПМИД 34104896 .
- ^ Парк К., Скидмор С., Хадар Дж., Гарнер Дж., Парк Х., Отте А. и др. (июнь 2019 г.). «Инъекционные составы PLGA длительного действия: анализ PLGA и понимание образования микрочастиц». Журнал контролируемого выпуска . 304 : 125–134. дои : 10.1016/j.jconrel.2019.05.003 . ПМИД 31071374 . S2CID 149444044 .
- ^ Флетчер Дж. (6 марта 2023 г.). Уолтон А. (ред.). «Люпрон (лейпролид ацетат) при раке простаты: чего ожидать» . www.medicalnewstoday.com . Проверено 30 апреля 2023 г.
- ^ Сяо Ц, Чжан Х, Ву С, Цюй Дж, Цинь Л, Ван С (2022). «Увеличенный почечный клиренс при тяжелых инфекциях – важный момент при дозировании ванкомицина: обзор повествования» . Границы в фармакологии . 13 : 835557. дои : 10.3389/fphar.2022.835557 . ПМЦ 8979486 . ПМИД 35387348 .
Внешние ссылки
[ редактировать ] СМИ, связанные с PLGA, на Викискладе?
СМИ, связанные с PLGA, на Викискладе?