Трифенилметильный радикал

| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Трифенилметил | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
ПабХим CID
|
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 19:15 H | |
| Молярная масса | 243.329 g·mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Трифенилметильный радикал (часто сокращенный до тритильного радикала ) представляет собой органическое соединение формулы (C 6 H 5 ) 3 C. Это стойкий радикал . Это был первый радикал , когда-либо описанный в органической химии . Из-за своей доступности тритильный радикал широко использовался. [ 1 ]
Приготовление и свойства
[ редактировать ]Его можно получить гомолизом трифенилметилхлорида 1 в таким металлом, как серебро или цинк, бензоле или диэтиловом эфире . Радикал 2 образует химическое равновесие с хиноидного типа димером 3 ( димером Гомберга ). В бензоле концентрация радикала составляет 2%. [ 2 ]
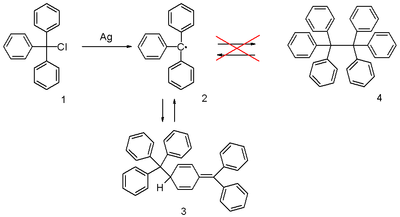
Растворы, содержащие радикал, имеют желтый цвет ; при повышении температуры раствора желтый цвет становится более интенсивным, так как равновесие смещается в пользу радикала (в соответствии с принципом Ле Шателье ).
На воздухе радикал быстро окисляется до перекиси , а цвет раствора меняется с желтого на бесцветный. Аналогично радикал реагирует с йодом с образованием трифенилметилйодида.
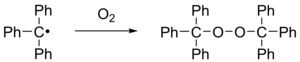
Хотя тритильный радикал образует хиноидный димер, его производные с соответствующей структурой замещения образуют димеры со структурой гексафенилэтана. Рентгеновские исследования дают длину связи 1,67 Å для гексакис(3,5-ди -т -бутилфенил)этана. Теоретические расчеты на очень высоком уровне теории показывают, что притяжение Ван-дер-Ваальса между трет -бутильными группами создает потенциальный минимум, отсутствующий в незамещенной молекуле. [ 3 ] [ 4 ] О других производных сообщалось как о хиноидном димере. [ 5 ]
История
[ редактировать ]Радикал был открыт Мозесом Гомбергом в 1900 году в Мичиганском университете . [ 6 ] [ 7 ] [ 8 ] Он попытался получить гексафенилэтан из трифенилметилхлорида и цинка в бензоле по реакции Вюрца и обнаружил, что продукт, судя по его поведению по отношению к йоду и кислороду, оказался гораздо более реакционноспособным, чем ожидалось. Обнаруженная структура была использована при разработке ЭПР -спектроскопии и подтверждена ею. [ 9 ] [ 10 ] [ 11 ]
Правильная хиноидная структура димера была предложена еще в 1904 году, но вскоре научное сообщество отказалось от этой структуры в пользу гексафенилэтана ( 4 ). [ 12 ] Впоследствии его повторное открытие продолжалось до 1968 года, когда исследователи из Свободного университета Амстердама опубликовали данные протонного ЯМР . [ 13 ]
См. также
[ редактировать ]- Трифенилметилгексафторфосфат
- Трифенилметан
- Триарилметановый краситель
- Трехвалентные радикалы группы 14
Ссылки
[ редактировать ]- ^ Тидвелл, Томас Т. (2010). «Триарилметил и родственные радикалы». Стабильные радикалы . стр. 1–31. дои : 10.1002/9780470666975.ch1 . ISBN 9780470666975 .
- ^ Смит, Майкл Б.; Марч, Джерри (2007), Продвинутая органическая химия: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 978-0-471-72091-1
- ^ Льюарс, Эррол (2008), «8. Гексафенилэтан», Modeling Marvels , Springer, Bibcode : 2008moma.book.....L
- ^ Гримме, Стефан; Шрайнер, Питер Р. (2011). «Стерическая скученность может стабилизировать лабильную молекулу: решение загадки гексафенилэтана». Angewandte Chemie, международное издание . 50 (52): 12639–12642. дои : 10.1002/anie.201103615 . ПМИД 22025456 .
- ^ Учимура, Ю.; Такеда, Т.; Катуно, Р.; Фудзивара, К.; Сузуки, Т. (2015). «Новый взгляд на загадку гексафенилэтана: образование α, o -димера». Angewandte Chemie, международное издание . 54 (13): 4010–4013. дои : 10.1002/anie.201500122 . ПМИД 25704856 .
- ^ Гомберг, М. (1900). «Пример трехвалентного углерода: трифенилметил» . Журнал Американского химического общества . 22 (11): 757–771. дои : 10.1021/ja02049a006 .
- ^ Гомберг, М. (1901). «О трехвалентном углероде». Журнал Американского химического общества . 23 (7): 496–502. дои : 10.1021/ja02033a015 . (Примечание: радикал еще называют кадикулой .)
- ^ Гомберг, М. (1902). «О трехвалентном углероде» . Журнал Американского химического общества . 24 (7): 597–628. дои : 10.1021/ja02021a001 .
- ^ Вайсман, С.И.; Соуден, Джон К. (1953). «Распределение электронов в трифенилметиле: сверхтонкая структура парамагнитного резонансного поглощения (C 6 H 5 ) 3 C 13* ". Журнал Американского химического общества . 75 (2): 503. doi : 10.1021/ja01098a522 .
- ^ Синклер, Дж.; Кивельсон, Д. (1968). «Исследование электронно-спиновым резонансом замещенных трифенилметильных радикалов». Журнал Американского химического общества . 90 (19): 5074–5080. дои : 10.1021/ja01021a004 .
- ^ «ЭПР-спектр трифенилметильного радикала» . Школа химии Бристольского университета . Проверено 5 августа 2018 г.
- ^ Макбрайд, Дж. М. (1974). «Загадка гексафенилэтана». Тетраэдр . 30 (14): 2009–2022. дои : 10.1016/S0040-4020(01)97332-6 .
- ^ Ланкамп, Х.; Наута, Западная Чехия; Маклин, К. (1968). «Новая интерпретация равновесия мономер-димер трифенилметил- и алкилзамещенных дифенилметил-радикалов в растворе». Буквы тетраэдра . 9 (2): 249–254. дои : 10.1016/S0040-4039(00)75598-5 .
Внешние ссылки
[ редактировать ]- Молекула месяца , июнь 1997 г.
- Трифенилметильный радикал: свойства и синтез