Гетерополиметаллат

К 5 [ИМо 6 О 24 ]· n H 2 O
Ag 7 [PV 12 O 36 ] n H 2 O
(NH 4 ) 4 [NiMo 6 O 24 H 6 ]·5H 2 O
К 3 [CrMo 6 O 24 H 6 ] · n H 2 O
(NH 4 ) 8 [CeMo 12 O 42 ]·8H 2 O
В химии гетерополиметаллаты полиоксометаллатов представляют собой подгруппу образуя , которые состоят из трех или более переходных металлов оксианионов , связанных вместе общими атомами кислорода, замкнутую трехмерную молекулярную структуру. В отличие от изополиметаллатов, которые содержат атомы металлов только одного типа, гетерополиметаллаты содержат разные оксианионы основных групп . Атомы металлов обычно представляют собой переходные металлы группы 6 (Mo, W) или, реже, группы 5 (V, Nb, Ta) в их высших степенях окисления . Обычно это диамагнитные анионы от бесцветного до оранжевого цвета. Для большинства гетерополиметаллатов W, Mo или V дополняются оксианионами основной группы фосфатом и силикатом . Существует множество исключений из этих общих утверждений, и класс соединений включает сотни примеров. [ 1 ] [ 2 ]
Структура
[ редактировать ]Определенные структурные мотивы повторяются. Например, ион Кеггина является общим как для молибдатов, так и для вольфраматов с различными центральными гетероатомами. Структуры Кеггина и Доусона имеют тетраэдрически -координированные гетероатомы, такие как P или Si , а структура Андерсона [ 3 ] имеет октаэдрический центральный атом, например алюминий .

|

|

| |
| Структура Страндберга, [HP 2 Mo 5 O 23 ] 4− | Структура кеггина , [ХМ 12 О 40 ] н − | Структура Доусона, [Х 2 М 18 О 62 ] н − | |
|

|

|

|
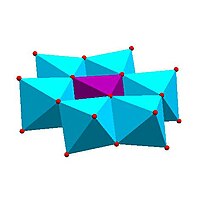
| структура Андерсона, [ХМ 6 О 24 ] н − | Структура Оллмана – Во, [ХМ 9 О 32 ] н − | Структура Уикли – Ямасе, [ХМ 10 О 36 ] н − | Структура Декстера – Сильвертона, [ХМ 12 О 42 ] н − |
Гетерополикислоты
[ редактировать ]Как правило, гетерополиметаллаты более термически устойчивы, чем гомополиметаллаты. Эта тенденция отражает стабилизирующее влияние тетраэдрического оксианиона, «склеивающего» оксокаркас переходного металла. Гетерополиметаллаты могут быть выделены в кислотной форме, что является отражением их прочности, тогда как гомополиметаллаты обычно не могут быть выделены. Примеры включают в себя: [ 4 ] [ 5 ]
- Кремневольфрамовая кислота , H 4 SiW 12 O 40 · n H 2 O
- фосфомолибденовая кислота , H 3 Mo 12 PO 40 · n H 2 O
- Фосфорновольфрамовая кислота , H 3 W 12 PO 40 · n H 2 O
Изомерия
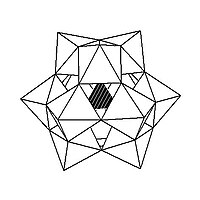
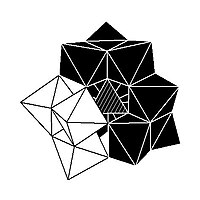
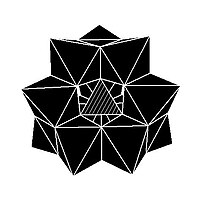
[ редактировать ]Структура Кеггина имеет 5 изомеров, которые получаются (концептуально) вращением одного или нескольких из четырех М 3 О 13 ед. через 60°. [ нужна ссылка ]
| а- [ХМ 12 О 40 ] н − | б- [ХМ 12 О 40 ] н − | с- [ХМ 12 О 40 ] н − | д- [ХМ 12 О 40 ] н − | Эм-м-м- [ХМ 12 О 40 ] н − |
|---|---|---|---|---|
|

|

|
|
|
Лакунарные структуры
[ редактировать ]Структура некоторых ПОМ получается из структуры более крупного ПОМ путем удаления одного или нескольких дополнительных атомов и сопутствующих им оксидных ионов, в результате чего образуется дефектная структура, называемая лакунарной структурой . Примером соединения с лакунарной структурой Доусона является Как 2 W 15 O 56 . [ 6 ] В 2014 году были зарегистрированы виды ванадатов со схожими селективными свойствами связывания металлов. [ 7 ]
Использование
[ редактировать ]
многократного использования Этот тип кислоты является распространенным кислотным катализатором в химических реакциях . [ 8 ]
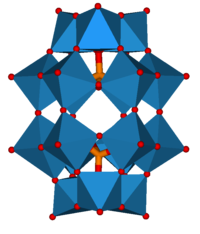
Гетерополикислоты широко используются в качестве гомогенных и гетерогенных катализаторов. [ 9 ] особенно те, которые основаны на структуре Кеггина , поскольку они могут обладать такими качествами, как хорошая термическая стабильность, высокая кислотность и высокая окислительная способность. Некоторые примеры катализа: [ 10 ]
- Гомогенный кислотный катализ
- гидролиз пропена с образованием пропан-2-ола путем H 3 PMo 12 O 40 и Х 3 ПВ 12 О 40
- Реакция Принса Х 3 ПВ 12 О 40
- полимеризация ТГФ Х 3 ПВ 12 О 40
- Гетерогенный кислотный катализ
- дегидратация пропан-2-ола до пропена и метанола до углеводородов путем Х 3 ПВ 12 О 40
- Преобразование гексана в 2-метилпентан (изогексан) путем H 3 PW 12 O 40 вкл. SiO 2
- Гомогенное окисление
- циклогексен + H 2 O 2 к адипиновой кислоте смешанными добавками Н 3 ПМо 6 В 6 О 40
- кетон от O 2 к кислоте и альдегиду смешанными добавками Н 5 ПМо 10 В 2 О 40
Гетерополикислоты уже давно используются в анализе и гистологии и являются компонентом многих реагентов, например, реагента Фолина-Чиокальтеу , фенольного реагента фолина, используемого в анализе белка Лоури , и ЭПТА, этаноловой фосфорновольфрамовой кислоты.
См. также
[ редактировать ]Цитаты
[ редактировать ]- ^ Гринвуд, штат Нью-Йорк; Эрншоу, А. (1997). Химия элементов (2-е изд.). Оксфорд: Баттерворт-Хайнеманн. ISBN 978-0-7506-3365-9 .
- ^ Поуп, Монтана (1983). Гетерополи- и изополиоксометаллаты . Нью-Йорк: Springer Verlag.
- ^ Блажевич, Амир; Ромпель, Аннет (январь 2016 г.). «Полиоксометаллат Андерсона-Эванса: от неорганических строительных блоков через гибридные органо-неорганические структуры к завтрашнему «Био-ПОМ» ». Обзоры координационной химии . 307 : 42–64. дои : 10.1016/j.ccr.2015.07.001 .
- ^ Диас, Дж.А.; Диас, SCL; Калиман, Э. (2014). «Полиоксометаллаты структуры кеггина». Структура кеггина Полиоксометаллаты . Неорганические синтезы. Том 36. с. 210-217. дои : 10.1002/9781118744994.ch39 . ISBN 9781118744994 .
- ^ Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, Нью-Йорк.
- ^ Мбомбекалле, ИМ; Кейта, Б.; Наджо, Л.; Берте, П.; Нойверт, Вашингтон; Хилл, CL; Риторто, доктор медицины; Андерсон, ТМ (2003). «Гетерополивольфраматы марганца. Синтез и эффекты гетероатомов в сэндвич-комплексах Уэллса-Доусона». Далтон Транс . 2003 (13): 2646–2650. дои : 10.1039/b304255c .
- ^ Кастнер, К.; Марграф, Дж. Т.; Кларк, Т.; Стреб, К. (2014). «Стратегия молекулярного заполнителя для доступа к семейству кластеров оксида ванадия, функционализированных переходными металлами». хим. Евро. Дж . 20 (38): 12269–12273. дои : 10.1002/chem.201403592 . ПМИД 25082170 .
- ^ Мизуно, Норитака; Мисоно, Макото (1998). «Гетерогенный катализ». Химические обзоры . 98 : 199–217. дои : 10.1021/cr960401q . ПМИД 11851503 .
- ^ Кожевников, ИВ (1998). «Катализ гетерополикислотами и многокомпонентными полиоксометаллатами в жидкофазных реакциях». Химические обзоры . 98 (1): 171–198. дои : 10.1021/cr960400y . ПМИД 11851502 .
- ^ «Оксидные катализаторы в химии твердого тела». Т Окухара, М Мисоно. Энциклопедия неорганической химии . Редактор Р. Брюс Кинг (1994). Джон Уайли и сыновья. ISBN 0-471-93620-0
Ссылки
[ редактировать ]- Коттон, Ф. Альберт ; Уилкинсон, Джеффри ; Мурильо, Карлос А.; Бохманн, Манфред (1999), Передовая неорганическая химия (6-е изд.), Нью-Йорк: Wiley-Interscience, ISBN 0-471-19957-5