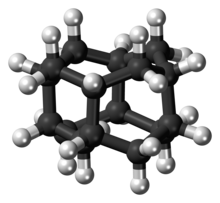
Диамантан

| |
| |
| Имена | |
|---|---|
| Название ИЮПАК
Пентацикло[7.3.1.1 4,12 .0 2,7 .0 6,11 ]тетрадекан
| |
| Другие имена
Конгрессан, диадамантан, декагидро-3,5,1,7-[1,2,3,4]бутантетраилнафталин
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| 1904934 | |
| КЭБ | |
| ХимическийПаук | |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 14 Ч 20 | |
| Молярная масса | 188.314 g·mol −1 |
| Появление | твердый белый кристалл |
| Плотность | 1,092 ± 0,06 г см −3 |
| Температура плавления | 244,73 ° С (472,51 ° F; 517,88 К) |
| Точка кипения | 269,5 ± 7,0 °С |
| трудно растворим (8,1 х 10 −4 г л −1 ) | |
| Растворимость в диэтиловом эфире | растворимый |
| войти P | 5.556 ± 0.228 |
| Давление пара | 0,0120 Торр |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
раздражитель, острая токсичность для водной флоры и фауны. |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 98,1 ° С (208,6 ° F; 371,2 К) |
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материалов |
| Структура | |
| Д 3д | |
| 0 Д | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Диамантан (также называемый конгрессаном ) — органическое соединение , входящее в группу алмазоидов . Это каркасные углеводороды, имеющие структуру, подобную субъединице решетки алмаза. Это бесцветное твердое вещество, которое было предметом исследований с момента его открытия в нефти и отделения от глубоких конденсатов природного газа. Алмазоиды, такие как диамантан, обладают необычными свойствами, включая низкую поверхностную энергию, высокую плотность, высокую гидрофобность и устойчивость к окислению. [ 1 ]
Происхождение и история
[ редактировать ]Диамантан встречается в природе в сырой нефти. В настоящее время предполагается, что адамантаны и диамантаны образовались в результате каталитических перегруппировок полициклических нафтеновых углеводородов. Несмотря на то, что алмазоиды, такие как диамантан, присутствуют в типичных нефтях лишь в следовых концентрациях, из-за их большой термодинамической стабильности они естественным образом концентрируются в результате катагенеза , становясь важными компонентами некоторых конденсатов природного газа, в том числе из формации Норфлет, Мексиканского залива США и Западной Европы. Канадский бассейн. [ 2 ]
Диамантан был выбран в качестве эмблемы Конгресса на лондонской встрече ИЮПАК в 1963 году и был показан в качестве украшения на обложка тезисов, программы и рекламных материалов. Участникам конгресса была поставлена задача синтезировать диамантан. Первое получение этого химического вещества было получено в 1965 году с выходом 1% путем изомеризации смеси фотодимеров норборнена, катализируемой галогенидом алюминия. Адамантан был первым, а «Конгрессан», как стал известен диамантан, был лишь вторым членом целого семейства соединений, известных как алмазоиды. Синтез третьего члена ряда в 1969 г. подчеркнул необходимость более общей схемы полутривиальной номенклатуры. Соединение было переименовано в «диамантан», а третий член обозначен как «триамантан». [ 3 ]
В 1966 году также было выделено диамантан из высококипящих фракций сырой нефти Годонина (из которого был открыт адамантан) и достигнуто значительное улучшение его выхода (до 10%). Хотя это позволило начать исследования в области химии диамантана, углеводород все еще было трудно получить в больших количествах. Затем диамантан стал так же доступен, как адамантан, и его химию стало легче изучать. [ 3 ]
Производство
[ редактировать ]Диамантан можно получить перегруппировкой различных пентациклических тетрадеканов, катализируемой кислотой Льюиса. Наилучший выход (84%) получается у транс-тетрагидро-Бинора-С. Удобная процедура синтеза включает перегруппировку гидрированного соединения Binor-S, которая дает диамантан с выходом ~ 70%. Другие более напряженные предшественники дают диамантан с меньшим выходом (1–47%) из-за диспропорционирования. [ 3 ]
Удобный путь синтеза начинается с димеризации норборнадиена ( 1 ), катализируемой смесью бромида кобальта - трифенилфосфина и эфирата трифторида бора . Полученный димер ( 2 ) гидрируют с получением изомеров тетрагидробинора-S ( 3a–3d ). В результате стерического взаимодействия преимущественно 3а и 3б образуются . Следующий этап — перегруппировка, которая происходит в горячем растворе циклогексана или сероуглерода с бромидом алюминия и образует основной продукт — диамантан ( 4 ). [ 4 ] [ 5 ] [ 6 ]

Диамантан можно получить термическим крекингом длинноцепочечных н- алканов. Считается, что механизм этого преобразования представляет собой добавление свободных радикалов. Хотя этот метод действительно дает алкилированный диамантан (т.е. монозамещенный, дизамещенный и тризамещенный метильными группами), производные адамантана также производятся в больших количествах из-за его большей термодинамической стабильности. Этот метод также дает гомологический ряд н -алканов с числом атомов углерода до 35, а также кокс. Предположение о возможности синтеза алмазоидных соединений путем термического крекинга требует дополнительной проверки. [ 7 ]
Характеристики
[ редактировать ]Диамантан принадлежит к семейству алмазоидов . Структуры этих членов представляют собой сегменты кристаллической решетки алмаза:

Из-за своей особой структуры температура плавления диамантана выше, чем у других углеводородов. Другим результатом является его высокая химическая и термическая стабильность.
| Энтальпия образования | Источник |
|---|---|
| [ 8 ] | |
| [ 8 ] |
Реакции
[ редактировать ]Диамантан можно нитровать обработкой тетрафторборатом нитрония (в нитрометане, не содержащем нитрила), с образованием смеси двух изомерных нитродиамантанов. [ 9 ]
Хлорирование хлоридом алюминия и ацетилхлоридом дает равные количества 1- и 4-хлордиамантана, тогда как использование хлорсульфоновой кислоты дает преимущественно 1-хлор-изомер. Гидролиз хлоридов дает соответствующие спирты, которые разделяются колоночной хроматографией на оксиде алюминия. [ 10 ]
Ссылки
[ редактировать ]- ^ Шрайнер, Питер; Фокин, Андрей; Фокина, Наталья; Ткаченко, Борислав; Даль, Джереми; Карлсон, Роберт (2011). «Синтез алмазоидных карбоновых кислот». Синтез . 2012 (2): 259. doi : 10.1055/s-0031-1289617 .
- ^ Даль, Дж. Э.; Лю, СГ; Карлсон, РМ (2002). «Выделение и структура высших алмазоидов, молекул алмаза нанометрового размера» . Наука . 299 (5603): 96–9. дои : 10.1126/science.1078239 . ПМИД 12459548 .
- ^ Перейти обратно: а б с Гунд, Тамара М.; Осава, Эйдзи; Уильямс, Ван Зандт; Шлейер, Пол В.Р. (1974). «Диамантан. I. Получение диамантана. Физические и спектральные свойства». Журнал органической химии . 39 (20): 2979. doi : 10.1021/jo00934a009 .
- ^ Гунд, ТМ; Осава, Э.; Ван Зандт, В. младший; Шлейер, П. против Р.: Диамантан. 1. Получение диамантана. Физические и спектральные свойства. В: Журнал органической химии , Band 39, Nr. 20, 1974, с. 2979–2987, doi:10.1021/jo00934a009 .
- ^ Гунд, ТМ; Осава, Э.; Ван Зандт, В. младший; Шлейер, П. против Шлейера. Р.: Удобная и высокопроизводительная подготовка алмазов (Конгрессан). В: Tetrahedron Letters , 1970, Том 11, No. 44, с. 3877–3880, doi:10.1016/S0040-4039(01)98613-7 .
- ^ Гунд, ТМ; Тилеке, В.; Шлейер, П. против. Р.: Диамантан: ПЕНТАЦИКЛ [7.3.1.1 4,12 .0 2,7 .0 6,11 ]ТЕТРАДЕКАН[Бутантетраилнафталин, 3,5,1,7-[1,2,3,4]-декагидро-]. В: Organic Syntheses , Band 53, 1973, S. 30, doi:10.15227/orgsyn.053.0030 .
- ^ Гордадзе Г.Н.; Гируц, М.В. (2008). «Синтез адамантановых и диамантановых углеводородов высокотемпературным крекингом высших н-алканов». Нефтехимия . 48 (6): 414. doi : 10.1134/S0965544108060029 .
- ^ Перейти обратно: а б Кларк, Т.; Нокс, ТМ; МакКерви, Массачусетс; Макл, Х.; Руни, Дж. Дж.: Термохимия веществ с мостиковыми кольцами. Энтальпии образования некоторых алмазоидных углеводородов и пергидрохинацена. Сравнение с данными эмпирических расчетов силового поля. В: Журнал Американского химического общества , Band 101, Nr. 9, 1979, с. 2404–2410, doi:10.1021/ja00503a028 .
- ^ Ола, Джорджия; Рамайя, П.; Рао, CB; Сэндфорд, Г.; Голам, Р.; Триведи, Нью-Джерси; Ола, Дж. А. (1993). «Нитрование адамантана и диамантана тетрафторборатом нитрония». Дж. Ам. хим. Соц . 115 (16): 7246–7249. дои : 10.1021/ja00069a024 .
- ^ Т. Кортни; Д.Е. Джонстон; М. А. МакКерви; Джей Джей Руни (1972). «Химия диамантана: синтез и некоторые реакции функционализации». Дж. Хим. Соц. (1): 2691–2696. дои : 10.1039/P19720002691 .




