Метилмагний хлорид
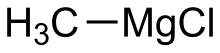
| |
| Имена | |
|---|---|
| Название ИЮПАК
хлорид(метил)магний
| |
| Другие имена
(хлормагнезио)метан
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.010.573 |
| Номер ЕС |
|
ПабХим CID
|
|
| НЕКОТОРЫЙ |
|
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| СН 3 MgCl | |
| Молярная масса | 74.79 g/mol |
| Появление | бесцветное твердое вещество |
| Реагирует с водой | |
| Растворимость | растворим в диэтиловом эфире и ТГФ |
| Опасности | |
| Безопасность и гигиена труда (OHS/OSH): | |
Основные опасности
|
Огнеопасно, Реагирует с водой |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х225 , Х250 , Х260 , Х314 | |
| P210 , P222 , P223 , P231+P232 , P233 , P240 , P241 , P242 , P243 , P260 , P264 , P280 , P301+P330+P331 , P302+ P334 , P303+P361+P353 , 4+П340 , П305+П351+ P338 , P310 , P321 , P335+P334 , P363 , P370+P378 , P402+P404 , P403+P235 , P405 , P422 , P501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | −17 ° C (1 ° F; 256 К) |
| Родственные соединения | |
Родственные соединения
|
Фенилмагний бромид , Дибутилмагний |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Метилмагнийхлорид представляет собой металлоорганическое соединение общей формулы CH 3 MgCl. Этот легковоспламеняющийся, бесцветный и чувствительный к влаге материал представляет собой простейший реактив Гриньяра и коммерчески доступен, обычно в виде раствора в тетрагидрофуране .
Синтез и реакции
[ редактировать ]По сравнению с более часто встречающимся метилмагнийбромидом. [1] и йодид метилмагния, хлорид метилмагния обладает преимуществами низкого эквивалентного веса и низкой стоимости. Его получают реакцией метилхлорида и магния в этиловом эфире . [2]

Как и большинство реагентов Гриньяра, метилмагнийхлорид сильно сольватируется эфирными растворителями за счет координации двух атомов кислорода с образованием тетраэдрически связанного магниевого центра.
Как и , он является синтетическим эквивалентом метилкарбаниона метиллитий синтона . Он реагирует с водой и другими протонными реагентами с образованием метана, например:
- CH 3 MgCl + ROH → CH 4 + MgCl(OR)
При обработке диоксаном эфирные растворы метилмагнийхлорида реагируют с образованием нерастворимого координационного полимера с формулой MgCl 2 (диоксан) 2 . В растворе остается диоксановый аддукт диметилмагния . В этом преобразовании используется равновесие Шленка , которое сдвигается вправо из-за осаждения галогенида магния: [3]
- 2 CH 3 MgCl + 2 диоксан → (CH 3 ) 2 Mg + MgCl 2 (диоксан) 2
См. также
[ редактировать ]Дальнейшее чтение
[ редактировать ]- Сакаи, Сёго; Джордан, К.Д. (1982). «Ab initio исследование структуры и частот колебаний реактива Гриньяра метилмагнийхлорида». Журнал Американского химического общества . 104 (14): 4019. doi : 10.1021/ja00378a047 .
Ссылки
[ редактировать ]- ^ Раймонд Пол; Оливье Риобе; Мишель Моми (1976). «(Е)-4-гексен-1-ол». Орг. Синтез. 55 : 62. дои : 10.15227/orgsyn.055.0062 .
- ^ Э. Р. Коберн (1947). «3-Пентен-2-ол». Орг. Синтез. 27:65 . дои : 10.15227/orgsyn.027.0065 .
- ^ Фишер, Рейнальд; Гёрлс, Хельмар; Мейзингер, Филипп Р.; Суксдорф, Регина; Вестерхаузен, Матиас (2019). «Взаимосвязь структура-растворимость 1,4-диоксановых комплексов ди(гидрокарбил)магния» . Химия – Европейский журнал . 25 (55): 12830–12841. дои : 10.1002/chem.201903120 . ПМК 7027550 . ПМИД 31328293 .
