ГОМЕР1
| ГОМЕР1 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | HOMER1 , HOMER, HOMER1A, HOMER1B, HOMER1C, SYN47, Ves-1, каркасный белок Гомера 1, каркасный белок Гомера 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | ОМИМ : 604798 ; МГИ : 1347345 ; Гомологен : 3155 ; Генные карты : ГОМЕР1 ; ОМА : ГОМЕР1 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Гомолог белка Homer 1 или Homer1 представляет собой нейрональный белок , который у человека кодируется HOMER1 геном . [5] [6] [7] Другие названия — Vesl и PSD-Zip45.
Структура
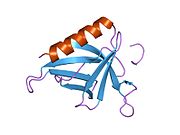
[ редактировать ]Homer1 Белок имеет N-концевой домен EVH1 , участвующий во взаимодействии белков, и C-концевой спиральный домен, участвующий в самоассоциации. Он состоит из двух основных вариантов сплайсинга : короткой формы (Homer1a) и длинной формы (Homer1b и c). Homer1a имеет только домен EVH1 и является мономерным, тогда как Homer1b и 1c имеют как EVH1, так и спирально-спиральные домены и являются тетрамерными. [8] [9] Спиральную спираль можно разделить на N-концевую половину и C-концевую половину. Предполагается, что N-концевая половина домена спиральной спирали будет параллельным димером, тогда как C-концевая половина представляет собой гибрид димерного и антипараллельного тетрамерного спирального домена. В целом, предполагается, что длинный Гомер будет иметь структуру, подобную гантеле, где две пары доменов EVH1 расположены по две стороны длинного (~ 50 нм) спирального домена. [9] есть Homer2 и Homer3 У млекопитающих помимо Homer1 , которые имеют схожую доменную структуру. Они также имеют схожие формы альтернативного сращивания.

Распределение тканей
[ редактировать ]Homer1 широко экспрессируется в центральной нервной системе , а также в периферических тканях, включая сердце , почки , яичники , яички и скелетные мышцы . Субклеточно в нейронах Homer1 концентрируется в постсинаптических структурах и составляет основную часть постсинаптической плотности .
Функция
[ редактировать ]Домен EVH1 взаимодействует с мотивом PPXXF. Этот мотив последовательности существует в метаботрофных глутаматных рецепторах группы 1 (mGluR1 и mGluR5), IP 3 рецепторах (IP 3 R), каналах семейства Shank , канонических каналах семейства временного рецепторного потенциала (TRPC) , дребрине , олигофренине , динамине 3 , CENTG1 и рианодиновом рецепторе . [5] [7] [10] [11] [12] [13] Предполагается, что благодаря своей тетрамерной структуре длинные формы Homer (такие как Homer1b и Homer1c) сшивают различные белки. Например, mGluR группы 1 перекрестно связан с его нижестоящим сигнальным рецептором IP3 . [10] Кроме того, предполагается, что посредством сшивания другого мультимерного белка Shank образуется ядро постсинаптической плотности . [9]
Примечательно, что экспрессия Homer1a индуцируется активностью нейронов, тогда как экспрессия Homer1b и 1c является конститутивной. Таким образом, Homer1a классифицируется как непосредственный ранний ген . Homer1a действует как естественная доминантно-негативная форма , которая блокирует взаимодействие между длинными формами и их белками-лигандами, конкурируя с сайтом связывания EVH1 на белках-лигандах. Таким образом, короткая форма Homer разъединяет передачу сигналов mGluR, а также сжимает структуру дендритных шипов . [6] [14] Таким образом, краткая форма Гомера считается частью механизма гомеостатической пластичности , который ослабляет реакцию нейронов, когда входная активность слишком высока. Длинная форма Homer1c играет роль в синаптической пластичности и стабилизации синаптических изменений во время долгосрочной потенциации . [15]
Сообщается, что спирально-спиральный домен взаимодействует с синтаксином13 и активирует Cdc42 . Взаимодействие с Cdc42 ингибирует активность Cdc42 по ремоделированию структуры дендритных отростков.
Быстрый антидепрессивный эффект
[ редактировать ]Homer1a переключает передачу сигналов mGluR5, чтобы увеличить активность рецептора AMPA для быстрого антидепрессивного действия при лишении сна. [16]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б с GRCh38: Версия Ensembl 89: ENSG00000152413 – Ensembl , май 2017 г.
- ^ Перейти обратно: а б с GRCm38: Ensembl, выпуск 89: ENSMUSG00000007617 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Перейти обратно: а б Сираиси-Ямагути Ю, Фуруичи Т (2007). «Белки семейства Гомера» . Геномная биология . 8 (2): 206. doi : 10.1186/gb-2007-8-2-206 . ПМК 1852408 . ПМИД 17316461 .
- ^ Перейти обратно: а б Ту Дж.К., Сяо Б., Юань Дж.П., Ланахан А.А., Леофферт К., Ли М. и др. (октябрь 1998 г.). «Гомер связывает новый богатый пролином мотив и связывает метаботропные рецепторы глутамата группы 1 с рецепторами IP3» . Нейрон . 21 (4): 717–726. дои : 10.1016/S0896-6273(00)80589-9 . ПМИД 9808459 . S2CID 2851554 .
- ^ Перейти обратно: а б «Ген Энтрез: Гомерный гомолог 1 HOMER1 (Дрозофила)» .
- ^ Хаяши М.К., Эймс Х.М., Хаяши Ю. (август 2006 г.). «Тетрамерная структура постсинаптического каркасного белка Гомера» . Журнал неврологии . 26 (33): 8492–8501. doi : 10.1523/JNEUROSCI.2731-06.2006 . ПМК 6674353 . ПМИД 16914674 .
- ^ Перейти обратно: а б с Хаяши М.К., Тан С., Верпелли С., Нараянан Р., Стернс М.Х., Сюй Р.М. и др. (апрель 2009 г.). «Белки постсинаптической плотности Гомера и Шэнка образуют полимерную сетевую структуру» . Клетка . 137 (1): 159–171. дои : 10.1016/j.cell.2009.01.050 . ПМК 2680917 . ПМИД 19345194 .
- ^ Перейти обратно: а б Сяо Б., Ту Дж.К., Петралия Р.С., Юань Дж.П., Доан А., Бредер К.Д. и др. (октябрь 1998 г.). «Гомер регулирует ассоциацию метаботропных глутаматных рецепторов группы 1 с поливалентными комплексами родственных Гомеру синаптических белков» . Нейрон . 21 (4): 707–716. дои : 10.1016/S0896-6273(00)80588-7 . ПМИД 9808458 . S2CID 16431031 .
- ^ Ронг Р., Ан Дж.Ю., Хуан Х., Нагата Е., Калман Д., Капп Дж.А. и др. (ноябрь 2003 г.). «Комплекс энхансер киназы PI3-Гомера соединяет mGluRI с киназой PI3, предотвращая апоптоз нейронов». Природная неврология . 6 (11): 1153–1161. дои : 10.1038/nn1134 . ПМИД 14528310 . S2CID 807407 .
- ^ Хван С.Ю., Вэй Дж., Вестхофф Дж.Х., Дункан Р.С., Одзава Ф., Вольпе П. и др. (август 2003 г.). «Дифференциальное функциональное взаимодействие двух изоформ белка Vesl/Homer с рианодиновым рецептором типа 1: новый механизм контроля внутриклеточной передачи сигналов кальция». Клеточный кальций . 34 (2): 177–184. дои : 10.1016/S0143-4160(03)00082-4 . ПМИД 12810060 .
- ^ Фэн В., Ту Дж., Ян Т., Вернон П.С., Аллен П.Д., Уорли П.Ф., Пессах И.Н. (ноябрь 2002 г.). «Гомер регулирует усиление комплекса каналов рианодинового рецептора 1-го типа» . Журнал биологической химии . 277 (47): 44722–44730. дои : 10.1074/jbc.M207675200 . ПМИД 12223488 .
- ^ Сала С., Футай К., Ямамото К., Уорли П.Ф., Хаяши Ю., Шэн М. (июль 2003 г.). «Ингибирование морфогенеза дендритных шипов и синаптической передачи с помощью индуцируемого активностью белка Homer1a» . Журнал неврологии . 23 (15): 6327–6337. doi : 10.1523/JNEUROSCI.23-15-06327.2003 . ПМК 6740555 . ПМИД 12867517 .
- ^ Мейер Д., Бонхёффер Т., Шойсс В. (апрель 2014 г.). «Баланс и стабильность синаптических структур при синаптической пластичности» . Нейрон . 82 (2): 430–443. дои : 10.1016/j.neuron.2014.02.031 . ПМИД 24742464 .
- ^ Альберт PR (октябрь 2019 г.). «Нацеливание на Homer1a для быстрого антидепрессивного эффекта» . Нейрон . 104 (2): 182–183. дои : 10.1016/j.neuron.2019.10.003 . PMID 31647890 . S2CID 204837754 .
Дальнейшее чтение
[ редактировать ]- Сяо Б., Ту Дж.К., Уорли П.Ф. (июнь 2000 г.). «Гомер: связь между нейронной активностью и функцией рецепторов глутамата». Современное мнение в нейробиологии . 10 (3): 370–374. дои : 10.1016/S0959-4388(00)00087-8 . ПМИД 10851183 . S2CID 8699597 .
- Маруяма К., Сугано С. (январь 1994 г.). «Олиго-кэпирование: простой метод замены кэп-структуры эукариотических мРНК олигорибонуклеотидами». Джин . 138 (1–2): 171–174. дои : 10.1016/0378-1119(94)90802-8 . ПМИД 8125298 .
- Хиллиер Л.Д., Леннон Дж., Беккер М., Бональдо М.Ф., Кьяпелли Б., Чиссо С. и др. (сентябрь 1996 г.). «Создание и анализ 280 000 меток экспрессируемых последовательностей человека» . Геномные исследования . 6 (9): 807–828. дои : 10.1101/гр.6.9.807 . ПМИД 8889549 .
- Брейкман П.Р., Ланахан А.А., О'Брайен Р., Рош К., Барнс К.А., Хуганир Р.Л., Уорли П.Ф. (март 1997 г.). «Гомер: белок, который избирательно связывает метаботропные рецепторы глутамата». Природа . 386 (6622): 284–288. Бибкод : 1997Natur.386..284B . дои : 10.1038/386284a0 . ПМИД 9069287 . S2CID 4346579 .
- Сузуки Ю, Ёситомо-Накагава К, Маруяма К, Суяма А, Сугано С (октябрь 1997 г.). «Создание и характеристика библиотеки кДНК, обогащенной по полной длине и по 5'-концу». Джин . 200 (1–2): 149–156. дои : 10.1016/S0378-1119(97)00411-3 . ПМИД 9373149 .
- Ту Дж.К., Сяо Б., Нейсбитт С., Юань Дж.П., Петралия Р.С., Брейкман П. и др. (июль 1999 г.). «Связывание комплексов mGluR/Homer и PSD-95 с семейством белков постсинаптической плотности Shank» . Нейрон . 23 (3): 583–592. дои : 10.1016/S0896-6273(00)80810-7 . ПМИД 10433269 . S2CID 16429070 .
- Рош К.В., Ту Дж.К., Петралия Р.С., Сяо Б., Вентольд Р.Дж., Уорли П.Ф. (сентябрь 1999 г.). «Гомер 1b регулирует передачу метаботропных глутаматных рецепторов группы I» . Журнал биологической химии . 274 (36): 25953–25957. дои : 10.1074/jbc.274.36.25953 . PMID 10464340 .
- Минаками Р., Като А., Сугияма Х. (июнь 2000 г.). «Взаимодействие Vesl-1L/Homer 1c с синтаксином 13». Связь с биохимическими и биофизическими исследованиями . 272 (2): 466–471. дои : 10.1006/bbrc.2000.2777 . ПМИД 10833436 .
- Анго Ф., Презо Л., Мюллер Т., Ту Дж.К., Сяо Б., Уорли П.Ф. и др. (июнь 2001 г.). «Агонист-независимая активация метаботропных глутаматных рецепторов внутриклеточным белком Гомер». Природа . 411 (6840): 962–965. дои : 10.1038/35082096 . ПМИД 11418862 . S2CID 4417727 .
- Вистов Г., Бернштейн С.Л., Вятт М.К., Фарисс Р.Н., Бехал А., Тачман Дж.В. и др. (июнь 2002 г.). «Анализ выраженных меток последовательностей РПЭ/сосудистой оболочки человека для проекта NEIBank: более 6000 неизбыточных транскриптов, новые гены и варианты сплайсинга». Молекулярное видение . 8 : 205–220. ПМИД 12107410 .
- Фэн В., Ту Дж., Ян Т., Вернон П.С., Аллен П.Д., Уорли П.Ф., Пессах И.Н. (ноябрь 2002 г.). «Гомер регулирует усиление комплекса каналов рианодинового рецептора 1-го типа» . Журнал биологической химии . 277 (47): 44722–44730. дои : 10.1074/jbc.M207675200 . ПМИД 12223488 .
- Хван С.Ю., Вэй Дж., Вестхофф Дж.Х., Дункан Р.С., Одзава Ф., Вольпе П. и др. (август 2003 г.). «Дифференциальное функциональное взаимодействие двух изоформ белка Vesl/Homer с рианодиновым рецептором типа 1: новый механизм контроля внутриклеточной передачи сигналов кальция». Клеточный кальций . 34 (2): 177–184. дои : 10.1016/S0143-4160(03)00082-4 . ПМИД 12810060 .
- Нортон Н., Уильямс Х.Дж., Уильямс Н.М., Сперлок Г., Заммит С., Джонс Г. и др. (июль 2003 г.). «Скрининг мутаций семейства генов Гомера и анализ ассоциаций при шизофрении». Американский журнал медицинской генетики. Часть B. Нейропсихиатрическая генетика . 120Б (1): 18–21. дои : 10.1002/ajmg.b.20032 . ПМИД 12815733 . S2CID 25053099 .
- Вестхофф Дж. Х., Хван С. Ю., Дункан Р. С., Одзава Ф., Вольпе П., Инокучи К., Коулен П. (сентябрь 2003 г.). «Белки Vesl/Homer регулируют функцию рианодинового рецептора типа 2 и передачу сигналов внутриклеточного кальция». Клеточный кальций . 34 (3): 261–269. дои : 10.1016/S0143-4160(03)00112-X . ПМИД 12887973 .
- Юань Дж.П., Киселев К., Шин Д.М., Чен Дж., Щейников Н., Кан Ш. и др. (сентябрь 2003 г.). «Гомер связывает каналы семейства TRPC и необходим для открытия TRPC1 рецепторами IP3» . Клетка . 114 (6): 777–789. дои : 10.1016/S0092-8674(03)00716-5 . ПМИД 14505576 . S2CID 10552676 .
- Ронг Р., Ан Дж.Ю., Хуан Х., Нагата Е., Калман Д., Капп Дж.А. и др. (ноябрь 2003 г.). «Комплекс энхансер киназы PI3-Гомера соединяет mGluRI с киназой PI3, предотвращая апоптоз нейронов». Природная неврология . 6 (11): 1153–1161. дои : 10.1038/nn1134 . ПМИД 14528310 . S2CID 807407 .