Ральф Л. Бринстер
Ральф Л. Бринстер | |
|---|---|
 Бринстер в октябре 2011 года | |
| Рожденный | 10 марта 1932 г. [1] |
| Национальность | Американский |
| Альма-матер | Университет Рутгерса (бакалавр наук, 1953 г.) Пенсильванский университет (VMD, 1960) (доктор философии, 1964) |
| Награды | Гран-при Шарля-Леопольда Майера , Франция Премия March of Dimes в области биологии развития , США Премия Вольфа в области медицины , ISR Международная премия Фонда Гайрднера , Канада Национальная медаль науки , США |
| Научная карьера | |
| Поля | Генетика ; Эмбриология ; Генная инженерия |
| Учреждения | Школа ветеринарной медицины Пенсильванского университета |
Ральф Лоуренс Бринстер [2] (родился 10 марта 1932 г.) — американский генетик , лауреат Национальной медали науки и Ричарда Кинга Меллона профессор репродуктивной физиологии в Школе ветеринарной медицины Пенсильванского университета. [3]
Молодость образование и
Ральф Л. Бринстер вырос на небольшой ферме в Сидар-Гроув, штат Нью-Джерси, где его родители разводили чистокровных животных. [3] Он изучал зоотехнику на бакалавриате в Сельскохозяйственной школе Кука Университета Рутгерса , Нью-Брансуик, штат Нью-Джерси, и получил степень бакалавра в 1953 году. Пока он учился в колледже, начался корейский конфликт, и он пошел добровольцем на службу. Он был вторым лейтенантом ВВС США в Корее в последний год боевых действий, а после назначения в армию США находился к северу от Сеула в составе армейского батальона. Он вернулся с военной службы и получил степень VMD ( Veterinariae Medicinae Doctoris ) (1960) и докторскую степень. Доктор физиологии (1964) Пенсильванского университета .
исследований Влияние
Ральф Бринстер признан одним из основоположников области млекопитающих трансгенеза . [4] [5] [6] Он известен в научном сообществе своими революционными исследованиями в области раннего развития эмбрионов, дифференцировки эмбриональных клеток , механизмов генного контроля и стволовых клеток . биологии [5] [7] [8] Вклад Бринстера в наши знания и понимание зародышевой линии млекопитающих был поистине выдающимся и был признан на самом высоком уровне. Нет учёного, который внес бы больший вклад в понимание генетической модификации млекопитающих и зародышевых клеток — наиболее важных клеток для личности и выживания любого вида. Зародышевые клетки лежат в основе непрерывности видов и отвечают за размножение особей с различным генетическим содержанием, что имеет решающее значение для эволюционной конкуренции. В частности, генетический состав этих клеток определяет их важность. Основополагающие исследования Бринстера по стратегиям манипулирования яйцеклетками млекопитающих и его новаторские исследования сперматогониальных стволовых клеток сегодня являются основой для всех исследований в этой области, включая спорный потенциал модификации зародышевой линии человека.
Некоторые полагают, что «экспериментальное генетическое манипулирование зародышевой линией животных, первоначально путем пронуклеарной инъекции клонированной ДНК в зиготы, представляет собой одну из наиболее значительных вех в истории человеческой цивилизации», Берингер и др. в работе «Манипулирование мышиным эмбрионом» (Колд-Спринг-Харбор). Laboratory Press, стр. 14, 2014). Модификация зародышевой линии существовала на протяжении сотен миллионов лет и способствовала эволюции видов посредством взаимодействия с окружающей средой. Целенаправленная модификация зародышевой линии человеком началась около 10 000 лет назад на плодородном полумесяце Юго-Западной Азии. одомашнивание растений и животных, дающее начало сельскому хозяйству и современной цивилизации. Первоначальную концепцию одомашнивания диких видов можно рассматривать как первое из четырех важных достижений во вмешательстве человека в эволюционную модификацию зародышевой линии, и многие считают ее началом современного человека. Последующее осознание того, что отбор и выведение желаемых фенотипов приведет к ценным изменениям в одомашненных видах, символизирует второе достижение. Идентификация и характеристика наследственных элементов, начавшаяся с исследований Менделя и продолжающаяся сегодня секвенированием геномов, представляет собой третье важное достижение. Эти три концептуальных достижения часто считаются основой сельского хозяйства и современной цивилизации. Экспериментальное добавление или модификация отдельных последовательностей ДНК и генов в зародышевой линии, известное как трансгенез, является примером четвертого уникального концептуального достижения в целенаправленной модификации человеком зародышевой линии. Таким образом, создание трансгенных животных представляет собой экстраординарное, творческое развитие в историческом взаимодействии человека с другими видами и имеет огромное значение в биологии и медицине (см. Внешние ссылки на Зал почета NICHD 2003 г. и Коллоквиум 2012 г. ниже).
В 1960-е годы Бринстер стал пионером в разработке методов манипулирования эмбрионами мышей , и его методы сделали мышь основной генетической моделью для понимания основ биологии человека и болезней. [5] [6] Его исследования заложили экспериментальную основу для прогресса в генетической модификации зародышевой линии у ряда видов, что произвело революцию в биологии, медицине и сельском хозяйстве. [7]
Его индекс Хирша , широко используемый расчет для оценки воздействия исследований, в Web of Science Citations на 2022 год равен 127, что является одним из самых высоких показателей за всю историю в области наук о жизни. Его d-индекс составляет 133 в Research.com , где он занял 152-е место в мире и 112-е место в США среди лучших ученых на 2022 год.
История исследований [ править ]

Культура яиц млекопитающих эмбрионов и
В то время как доктор философии. Кандидат в 1960-х годах Бринстер разработал первую надежную систему культивирования in vitro ранних эмбрионов млекопитающих . Его первоначальные исследования проводились на оплодотворенных яйцах мышей. В 1963 году он описал метод культивирования, состоящий из микрокапель среды под маслом, который остается основным методом культивирования яиц млекопитающих всех видов, включая человеческие яйца, во время экстракорпорального оплодотворения. В течение следующих 10 лет Бринстер изучил многие аспекты метаболизма яиц мышей и определил характеристики, общие для яиц всех видов млекопитающих. На основе этих исследований он разработал питательную среду и стратегии манипулирования эмбрионами, которые являются основой всех сред для культивирования яиц и методов манипуляций, используемых сегодня. Он опубликовал более 60 статей в общей области метаболизма и культивирования яиц и является ученым, заложившим основу для последующих исследований, связанных с культурой яиц млекопитающих. Его исследования предоставили надежный метод манипулирования всеми стадиями преимплантационного развития у мышей и других видов млекопитающих (см. рисунок 1). [10] [9]
Эти методы сохранились до наших дней и составляют основу для всех экспериментов с эмбрионами млекопитающих, включая трансгенных животных, исследования эмбриональных стволовых клеток, экстракорпоральное оплодотворение человека и млекопитающих, клонирование млекопитающих и нокаут- технологии.
Его стратегии культивирования in vitro и манипуляций с яйцеклетками напрямую способствовали основополагающим методам современной науки, таким как расщепление эмбрионов, интрацитоплазматическая инъекция спермы, ядерная трансплантация и трансплантация митохондрий в яйцеклетки, среди прочего, которые выполняются in vitro с использованием методов, практически не изменившихся с тех пор, как они были введены Бринстер.
Этот «метод Бринстера» манипуляций с эмбрионами настолько распространен в современной биологии, что другие ученые редко цитируют эту работу в текущих публикациях. [10] [9]

Инъекция стволовых клеток в эмбрионы мышей позволила создать первый прототип животного . трансгенного
Бринстер использовал основы своих стратегий культивирования и манипуляций для изучения методов изменения генетического состава развивающихся эмбрионов и их зародышевых клеток. В начале 1970-х годов он ввел стволовые клетки в эмбрионы (бластоцисты) в серии творческих экспериментов, которые имели огромное значение и изменили представление ученых о возможности модификации генов зародышевой линии. Он был первым ученым, продемонстрировавшим, что чужеродные клетки тератокарциномы могут объединяться с нативными клетками бластоцисты с образованием взрослых «химерных» мышей, продемонстрировав возможность этого нового подхода к изменению генетического характера мышей (рис. 2). [11] Введение чужеродных клеток и новых генов этим химерным мышам привело к появлению первых прототипов трансгенных животных. [8] Кроме того, это открытие стимулировало поиск эмбриональных стволовых клеток и в конечном итоге привело к созданию «нокаутной мыши».

гигантская Трансгенез и мышь
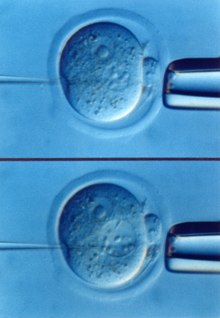
Профессор Бринстер был первым ученым, который микроинъецировал оплодотворенные яйцеклетки с РНК и ДНК, и был в авангарде области применения этих методов микроинъекций для создания трансгенных мышей. [4] [6] [14] [15] Прямая инъекция оплодотворенных яиц мышей, впервые предложенная Бринстером, была первым подходом к рутинной экспериментальной модификации зародышевой линии и послужила основой для всех последующих методов (рис. 3). [13]
Затем Бринстер сотрудничал с Ричардом Пальмитером , выдающимся молекулярным биологом из Вашингтонского университета, чтобы стать пионером и разработать перенос чужеродных генов млекопитающим, и они использовали эти методы для выяснения активности и функции многих генов. Их плодотворные эксперименты катализировали мировую революцию в генной инженерии в 1980-х годах. [14] [15] [16] Трансгенных мышей сегодня используют каждый день в тысячах лабораторий по всему миру для изучения самых разных явлений: от биологии рака и сердечно-сосудистых заболеваний до выпадения волос и аномального поведения. Их эксперименты впервые показали, что новые гены могут быть введены в зародышевую линию млекопитающих с потенциалом повышения устойчивости к болезням, ускорения роста и производства жизненно важных белков, таких как факторы свертывания крови, необходимые больным гемофилией . Возможно, их самым известным экспериментом было создание «Гигантской/Супер-Мыши», который катализировал интерес в научном сообществе и широкой общественности к огромному потенциалу разрабатываемой трансгенной технологии и положил начало генетической революции в биологии. , медицина и сельское хозяйство (рис. 4). [12] Кроме того, они предоставили первое доказательство экспрессии трансгенов , первый пример рака, возникающего из-за трансгена, и первое доказательство целенаправленной интеграции ДНК посредством инъекции яйцеклетки. [17] [18] Вместе Бринстер и Пальмитер разработали многие из первых животных моделей заболеваний человека в 1980-х годах. Их партнерство также привело к появлению первых трансгенных кроликов, овец и свиней. [19]
Это трансконтинентальное сотрудничество создало объем работ, которые легли в основу научного прогресса в области генетической модификации посредством трансгенеза, гомологичной рекомбинации или методов «нокаута» и клонирования; а стратегии культивирования яиц и манипуляций были необходимы для этих экспериментов Бринстера и Пальмитера, а также для всех других ученых, работающих с яйцами и эмбрионами всех видов. Методы культивирования яиц и инъекции, разработанные Бринстером, служат основой системы генетической модификации CRISPR/Cas9 , которая в настоящее время используется для всех типов генных изменений у всех видов.

Короче говоря, техника инъекции яйцеклеток Бринстера была первой, использованной для получения трансгенных животных, и в настоящее время является основным методом внесения всех генетических изменений у всех видов.
спермы Модификация генов

В последние годы Бринстер продолжал развивать область биологии стволовых клеток, сделав серию катализирующих трансформационных открытий с использованием стволовых клеток мужской зародышевой линии, называемых сперматогониальными стволовыми клетками (SSC). Сперматогониальные стволовые клетки в семенниках — единственные клетки взрослого организма, которые делятся на протяжении всей жизни и передают гены следующему поколению, что делает их мощным ресурсом для модификации генов любого вида млекопитающих. В элегантных экспериментах, опубликованных в 1994 году, Бринстер продемонстрировал, что эти стволовые клетки можно трансплантировать из семенника фертильного мужчины в семенник бесплодного мужчины, где они устанавливают сперматогенез и производят сперматозоиды донорского гаплотипа (рис. 5). [20] [22] Он также продемонстрировал, что этот метод применим ко всем исследованным видам млекопитающих, включая человека. [21] В настоящее время ученые расширяют культуру и трансплантацию сперматогониальных стволовых клеток мальчикам препубертатного возраста, проходящим лечение от рака, чтобы сохранить их фертильность (рис. 6). [21] Способность собирать, культивировать, генетически модифицировать, замораживать и трансплантировать сперматогониальные стволовые клетки не только позволит провести сложную генетическую модификацию, но и сделает отдельных мужчин биологически бессмертными. Более того, текущие исследования показывают, что вскоре станет возможным преобразовать соматическую клетку в зародышевую клетку, особенно в SSC, что будет иметь огромное значение с научной точки зрения и для лечения клинически важных проблем с фертильностью. [20]
Каждый из этих четырех революционных вкладов положил начало целым областям научных исследований.
Фундаментальное и огромное значение революционных экспериментов Ральфа Бринстера, лежащих в основе модификации зародышевой линии, иллюстрируется осознанием того, что ни один уровень описания генетического кода не позволит понять, как он функционирует, без возможности экспериментально модифицировать код и изучить результат in vivo. Эти эксперименты по модификации зародышевой линии у млекопитающих сегодня основаны на основополагающих работах Бринстера, включая разработку яичной культуры и стратегий манипулирования яйцами, демонстрацию того, что бластоцисты могут быть колонизированы чужеродными стволовыми клетками, способность яиц выживать при прямой инъекции РНК. и ДНК, а также методы модификации сперматогониальных стволовых клеток. Вклад Ральфа Бринстера в этой области не имеет себе равных, и его часто называют «отцом трансгенеза».


научное признание Большое
В 2003 году Бринстер был удостоен премии Вольфа в области медицины и был отмечен за «разработку процедур манипулирования яйцеклетками и эмбрионами мышей, которые сделали возможным трансгенез и его применение на мышах». Бринстер, первый ученый, осуществивший микроинъекцию оплодотворенных яйцеклеток (с РНК), был в авангарде применения этих методов для создания трансгенных мышей». [4] Важно отметить, что первые трансгенные животные любого вида были созданы путем прямой инъекции генов в яйца мышей, что было основным методом создания трансгенных животных с момента его описания. Более того, развитие подхода CRISPR/Cas9 теперь сделало прямую инъекцию яиц предпочтительным вариантом модификации зародышевой линии практически во всех обстоятельствах и у всех видов. В 2006 году Бринстер получил международную премию Канадского фонда Гейрднера за новаторские открытия в области модификации зародышевой линии у млекопитающих. [5] Частично цитата гласила: «Размах его вклада не имеет себе равных в этой области». Совсем недавно Бринстер был награжден Национальной медалью науки 2010 года — высшей наградой, присуждаемой правительством США ученым и инженерам, от президента Барака Обамы за его выдающийся вклад в генетическую модификацию зародышевой линии. С момента учреждения награды в 1962 году Бринстер был первым ветеринаром в Соединенных Штатах и восьмым ученым из Пенсильванского университета, получившим Национальную медаль науки. [7] [23]
Академическая карьера [ править ]
Бринстер провел всю свою академическую карьеру в Школе ветеринарной медицины Пенсильванского университета; с 1956 по 1960 год в качестве студента-ветеринара, с 1960 по 1964 год в качестве постдокторанта и кандидата наук, а затем продолжил работу в качестве преподавателя. [24] Он был назначен доцентом в 1966 году, профессором в 1970 году и профессором репродуктивной физиологии Ричарда Кинга Меллона в 1975 году, и эту должность он занимает до сих пор. В 1969 году он основал Программу подготовки ученых-ветеринаров-медиков, первую и единственную комбинированную программу VMD (DVM)/PhD, финансируемую Национальными институтами здравоохранения, и занимал должность ее директора до 1984 года. С 1969 года программа подготовила более 100 выпускников комбинированных степеней. которые занимают многие руководящие должности по всей стране. С 1997 по 2007 год он был научным руководителем Центра трансгенеза животных и исследования зародышевых клеток Школы ветеринарной медицины. С 2007 по 2008 год он был содиректором-основателем Института регенеративной медицины Пенсильванского университета, одной из ведущих программ в мире. Он обучил более 50 докторантов и постдокторантов в своей лаборатории и преподавал физиологию профессиональным студентам Школы ветеринарной медицины каждый год с 1964 по 2020 год. Пенсильвания в знак признания выдающегося научного вклада Бринстера. [25]
Личная история [ править ]
В 1961 году Бринстер женился на Элейн Реддинг, дипломированной медсестре и выпускнице Школы медсестер Филадельфийской больницы общего профиля, и в настоящее время они проживают в Гладвине, штат Пенсильвания. У них четверо детей. Лорен Р. Бринстер получила степень VMD в Школе ветеринарной медицины Пенсильванского университета. Она ветеринарный патологоанатом в Национальном институте здравоохранения, Бетесда, Мэриленд. Кристен А. Бринстер получила степень доктора юридических наук на юридическом факультете Университета Балтимора . Она является судебным адвокатом и управляющим партнером-основателем компании Sutherland & Brinster, штат Пенсильвания, штат Мэриленд. Дерек Р. Бринстер получил степень доктора медицины в Медицинской школе Перельмана Пенсильванского университета . Он является профессором сердечно-сосудистой и торакальной хирургии и директором отделения хирургии аорты в Northwell Health, Нью-Йорк, штат Нью-Йорк. Клейтон Дж. Бринстер получил степень доктора медицины в Медицинской школе Перельмана Пенсильванского университета. Он является директором Центра заболеваний аорты и доцентом кафедры сосудистой и эндоваскулярной хирургии Медицинского центра Чикагского университета в Чикаго, штат Иллинойс. В 2021 году семья учредила премию Элейн Реддинг Бринстер в области науки и медицины в знак признания огромного вклада Элейн в достижения семьи. Премия и медальон в размере 100 000 долларов будут вручаться ежегодно выдающемуся ученому из любой страны по решению Совета директоров. Институт регенеративной медицины Пенсильванского университета во время ежегодного симпозиума Ральфа Л. Бринстера.
Награды и почести [ править ]
- 1960–1961 Член Американской ветеринарно-медицинской ассоциации, Пенсильванский университет, Высшая школа искусств и наук.
- 1961–1964 Стипендиат Пенсильванского плана Пенсильванский университет, Высшая школа искусств и наук
- Премия 1983 года в области биологических и медицинских наук Нью-Йоркской академии наук.
- 1984 Лектор Общества Харви
- 1986 г. Член Американской академии искусств и наук. [2]
- 1986 Член Института медицины Национальной академии наук.
- 1987 г. отмечен Международным симпозиумом Центра клеточных наук У. Элтона Джонса.
- 1987 Член Национальной академии наук .
- 1989 г. Член Американской ассоциации развития науки.
- Премия Министерства сельского хозяйства США за выдающиеся заслуги 1989 года.
- Приглашенный лектор Нобелевского симпозиума 1991 г., Стокгольм, Швеция.
- 1992 г., член Американской академии микробиологии.
- 1992 Лекция Фонда Хуана Марча, Мадрид, Испания.
- Премия пионера 1992 года Международного общества переноса эмбрионов.
- 1994 Гран-при Шарля-Леопольда Майера, высшая награда Французской академии наук (с Ричардом Пальмитером)
- 1994 Почетный доктор Медицинского университета Страны Басков, Испания.
- Премия выпускникам 1995 года за заслуги перед Пенсильванским университетом, факультет ветеринарной медицины
- Премия March of Dimes 1996 года в области биологии развития с Беатрис Минц (год открытия) [24]
- Премия Бауэра 1997 года и премия за достижения в науке Института Франклина [26]
- Премия Карла Хартмана 1997 года Общества изучения репродукции. [6]
- 1997 Медаль Джона Скотта за научные достижения Городские фонды Филадельфии [27]
- 1998 г. отмечен специальным выпуском Festschrift, посвященным доктору Бринстеру и всемирному влиянию его вклада; Международный журнал биологии развития
- Премия 1998 года «Пионер в области репродуктивных исследований» Национальный институт здоровья детей и человеческого развития
- 1999 Премия Джорджа Хаммеля Кука выдающимся выпускникам Рутгерса, Государственный университет Нью-Джерси [28]
- 2000 Чарльтонская лекция Медицинский факультет Университета Тафтса
- 2000 г. Степень почетного доктора наук Рутгерса, Государственный университет Нью-Джерси.
- 2001 Премия Эрнста В. Бертнера Онкологический центр имени доктора медицины Андерсона Техасского университета в знак признания новаторского вклада в исследования рака.
- 2002 г. Высоко цитируемый исследователь (1980–2000 гг.), Назначен Институтом научной информации. Примерно 1 из 1000 авторов относится к этой категории.
- 2003 г. Премия Вольфа в области медицины , Израиль «за разработку процедур манипулирования яйцеклетками и эмбрионами мышей, которые сделали возможным трансгенез и его применение на мышах». с Марио Капечки и Оливером Смитисом [4]
- 2003 г. Избран в Зал почета Национального института здоровья детей и человеческого развития (всего 15 членов)
- , 2006 г. Международная премия Фонда Гайрднера , Канада, «за новаторские открытия в области модификации зародышевой линии млекопитающих». [5]
- США, 2010 г. Национальная медаль науки «за фундаментальный вклад в разработку и использование трансгенных мышей». [7]
- 2011 года за выдающиеся заслуги. Международного общества трансгенных технологий Премия [29]
- Премия 2012 года за заслуги перед жизнью. От выпускников Школы ветеринарной медицины Пенсильванского университета.
- Премия 2012 года за выдающиеся достижения в области териогенологии. От Фонда териогенологии от имени Американского колледжа териогенологов и Общества териогенологии.
- 2015 г. Почетный доктор права Университета Калгари, Канада.
- 2015 Член Американского физиологического общества.
- 2017 г. – звание почетного профессора президента Ральфа Л. Бринстера, Пенсильванский университет. [25]
- 2019 «Границы исследований зародышевых клеток». Симпозиум Бринстера по трансплантации сперматогониальных стволовых клеток, посвященный 25-летию, Школа ветеринарной медицины Пенсильванского университета.
В популярной культуре [ править ]
В широко известном романе Зэди Смит « Белые зубы » большое место занимает генетически модифицированная мышь «Futuremouse», основанная на трансгенных экспериментах Пальмитера и Бринстера в 1980-х годах.
В 2017 году доктора Бринстера запечатлела в своей лаборатории художница-портретистка Мэри Уайт . Мэри Уайт недавно была награждена золотой медалью Портретного общества Америки в честь «пожизненной преданности совершенству, а также в знак признания выдающихся работ, которые служат развитию и развитию изобразительного искусства портретной и фигуративной живописи в Америке». [30]
Ссылки [ править ]
- ^ Ральф Бринстер . Национальный фонд медалей в области науки и технологий. 2010 . Проверено 7 февраля 2019 г.
- ^ Jump up to: Перейти обратно: а б «Книга участников, 1780–2010: Глава B» (PDF) . Американская академия искусств и наук . Проверено 16 апреля 2011 г.
- ^ Jump up to: Перейти обратно: а б Донна Лойл (1 ноября 2012 г.). «Исследователь из Пенсильванского университета делится результатами 50-летнего изучения зародышевой линии млекопитающих» . Журнал ДВМ .
- ^ Jump up to: Перейти обратно: а б с д «Ральф Л. Бринстер, лауреат премии Вольфа в области медицины - 2003 г.» . Фонд Волка. Проверено 7 февраля 2019 г.
- ^ Jump up to: Перейти обратно: а б с д и «Ральф Л. Бринстер» . Фонд Гайрднера. Проверено 7 февраля 2019 г.
- ^ Jump up to: Перейти обратно: а б с д «Премия Карла Г. Хартмана 1997 года имени Ральфа Л. Бринстера» (PDF) . 15 марта 2004 г. Проверено 7 февраля 2019 г.
- ^ Jump up to: Перейти обратно: а б с д «Президент Обама чествует лучших ученых и новаторов страны» . Белый дом. 27 сентября 2011 г. Проверено 7 февраля 2019 г.
- ^ Jump up to: Перейти обратно: а б Аречага, Хуан; Культура эмбрионов, стволовые клетки и экспериментальная модификация эмбрионального генома; Интервью с профессором Ральфом Бринстером ; Межд. Дж. Дев. Биол. 42: 861-877 (1998)
- ^ Jump up to: Перейти обратно: а б с Бринстер, Р.Л. Метод культивирования in vitro мышиных яйцеклеток из двухклеточных в бластоцисты . Exp Cell Res.1963; 32: 205-208.
- ^ Jump up to: Перейти обратно: а б Молот РЭ. Яичная культура: основы. Int J Dev Biol. 1998;42(7):833-9. ПМИД 9853812.
- ^ Jump up to: Перейти обратно: а б Бринстер, Р.Л. Влияние клеток, перенесенных в бластоцисты мыши, на последующее развитие. Дж. Эксп. Мед. 1974 год; 140: 1049-1056.
- ^ Jump up to: Перейти обратно: а б Пальмитер Р.Д., Бринстер Р.Л., Хаммер Р.Э., Трумбауэр М.Э., Розенфельд М.Г., Бирнберг Н.К. и Эванс Р.М. Резкий рост мышей, которые развиваются из яиц, которым микроинъецировали слитые гены металлотионеина и гормона роста. Природа. 1982 год; 300: 611-615.
- ^ Jump up to: Перейти обратно: а б Бринстер Р.Л. и Пальмитер Р.Д. Введение генов в зародышевую линию животных. В: Серия 80 лекций Харви. Нью-Йорк: Алан Р. Лисс, Inc.; 1986. 1-38.
- ^ Jump up to: Перейти обратно: а б Бринстер Р.Л., Чен Х.Ю., Трумбауэр М.Э. и Аварбок М.Р. Трансляция информационной РНК глобина яйцеклеткой мыши. Природа. 1980 год; 283: 499-501.
- ^ Jump up to: Перейти обратно: а б Бринстер Р.Л., Чен Х.Ю. и Трумбауэр М.Е. Мышиные ооциты транскрибируют инъецированный ген 5S РНК Xenopus. Наука. 1981 год; 211: 396-398.
- ^ Бринстер, Р.Л., Чен, Х.Ю., Трумбауэр, М.Э., Сенеар, А.В., Уоррен, Р. и Пальмитер, Р.Д. Соматическая экспрессия тимидинкиназы герпеса у мышей после инъекции слитого гена в яйца . Клетка. 1981 год; 27: 223-231.
- ^ Бринстер, Р.Л., Чен, Х.Ю., Мессинг, А., Ван Дайк, Т., Левин, А.Дж. и Пальмитер, Р.Д. У трансгенных мышей, несущих гены Т-антигена SV40, развиваются характерные опухоли головного мозга. Клетка. 1984 год; 37: 367-379.
- ^ Бринстер Р.Л., Браун Р.Э., Ло Д., Аварбок М.А., Орам Ф. и Пальмитер Р.Д. Целенаправленная коррекция гена Ea класса II с помощью микроинъекции ДНК в мышиные яйца . Учеб. Натл. акад. наук. США. 1989 год; 86: 7087-7091.
- ^ Хаммер, Роберт Э.; Пурсел, Вернон Г.; Рексроуд, Кэрд Э.; Уолл, Роберт Дж.; Болт, Дуглас Дж.; Эберт, Карл М.; Пальмитер, Ричард Д.; Бринстер, Ральф Л. (1985). «Производство трансгенных кроликов, овец и свиней методом микроинъекции». Природа. 315 (6021): 680–683. Бибкод:1985Natur.315..680H. дои: 10.1038/315680a0. PMID 3892305. S2CID 4354002.
- ^ Jump up to: Перейти обратно: а б с Кубота Х. и Бринстер Р.Л. Сперматогониальные стволовые клетки. Биол. Репродукция. 2018 март; 99 (0) Специальный выпуск к 50-летию: 1-23. DOI: 10.1093/biolre/ioy077; ПМИД 29617903
- ^ Jump up to: Перейти обратно: а б с Бринстер, Р.Л. Мужские стволовые клетки зародышевой линии: от мышей к мужчинам. Наука. апрель 2007 г.; 316:404-405
- ^ Бринстер, Р.Л., и Аварбок, М.Р. Передача донорского гаплотипа по зародышевой линии после трансплантации сперматогониев. Учеб. Натл. акад. наук. США. 1994 год; 91: 11303-11307.
- ^ Ральф Бринстер . Национальный фонд медалей в области науки и технологий. 2010. Проверено 7 февраля 2019 года.
- ^ Jump up to: Перейти обратно: а б «История лауреатов премии» (PDF) . Проверено 7 февраля 2019 г.
- ^ Jump up to: Перейти обратно: а б «Подарок в размере 3 миллионов долларов для учреждения звания почетного профессора президента Ральфа Л. Бринстера» . Альманах Пенсильванского университета . Том. 63, нет. 30. 11 апреля 2017.
- ^ «Ральф Л. Бринстер | Премия Бауэра 1997 года и премия за достижения в науке» . 15 января 2014 года . Проверено 7 февраля 2019 г.
- ^ «Премия Джона Скотта» . Проверено 7 февраля 2019 г.
- ^ «История выпускника: Ральф Бринстер (AG '53): ветеринар и революционер в области здравоохранения» . Университет Рутгерса. 24 февраля 2014 года . Проверено 7 февраля 2019 г.
- ^ «Программа и тезисы 10-го совещания по трансгенным технологиям (TT2011): Гранд-курорт TradeWinds Island, Сент-Пит-Бич, Флорида, США, 24–26 октября 2011 г.» . Трансгенные исследования . 20 (5): 1139–1189. 1 октября 2011 г. doi : 10.1007/s11248-011-9540-8 . ISSN 0962-8819 .
- ^ «Искусство вкратце» . Почта и курьер . 7 мая 2016 г. Проверено 26 марта 2017 г.
Внешние ссылки [ править ]
- Ссылка на веб-сайт: http://www.vet.upenn.edu/research/research-laboratories/research-laboratory/brinster-laboratory-of-reproductive-psyology
- Ссылка на лекцию о Национальной медали науки Бринстера: https://www.youtube.com/watch?v=nLmVlFRBUZ8
- Ссылка на церемонию вручения Национальной медали науки Бринстера: https://www.youtube.com/watch?v=mOuBjuUQyJI
- Ссылка на коллоквиум NICHD, декабрь 2012 г., лекция № 5: http://videocast.nih.gov/summary.asp?Live=12182&bhcp=1 ; Краткое изложение исследования 20 мин.
- Ссылка на вводную лекцию в Зал почета NICHD 2003 г., продолжительность 1 час 5 мин.: NIH VideoCast — введение в Зал почета к 40-летию NICHD ; Автобиография 20 мин.
- Премия Вольфа в области медицины в 2002/3 г. (подробно)
- 1932 рождения
- Американские генетики
- Персонал ВВС США во время Корейской войны
- Члены Американской академии искусств и наук
- Живые люди
- Члены Национальной академии наук США
- Люди из Сидар-Гроув, Нью-Джерси
- Выпускники Университета Рутгерса
- Офицеры ВВС США
- Выпускники факультета ветеринарной медицины Пенсильванского университета
- Преподаватель Пенсильванского университета
- Лауреаты премии Вольфа в области медицины
- Военные из Нью-Джерси
- Члены Национальной Медицинской Академии