Миниген
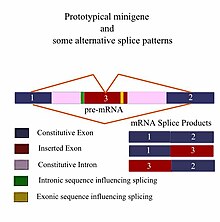
Миниген представляет собой минимальный фрагмент гена, который включает экзон и контрольные области, необходимые для экспрессии гена таким же образом, как фрагмент гена дикого типа . Это миниген в самом базовом смысле. Можно сконструировать более сложные минигены, содержащие несколько экзонов и интронов . Минигены предоставляют ценный инструмент для исследователей, оценивающих сплайсинга закономерности как в экспериментах по биохимической оценке in vivo , так и in vitro . [ 1 ] [ 2 ] В частности, минигены используются в качестве репортерных векторов сплайсинга (также называемых векторами захвата экзонов ) и действуют как зонд для определения того, какие факторы важны для результатов сплайсинга. Их можно сконструировать, чтобы проверить, как цис-регуляторные элементы (эффекты РНК) и трансрегуляторные элементы (ассоциированные белки / факторы сплайсинга ) влияют на экспрессию генов. [ 3 ]
История
[ редактировать ]Минигены были впервые описаны как соматическая сборка сегментов ДНК и состояли из участков ДНК, которые, как известно, кодируют белок, и фланкирующих участков, необходимых для экспрессии белка. Этот термин был впервые использован в статье 1977 года для описания клонирования двух минигенов, предназначенных для экспрессии пептида. [ 4 ]
Сплайсинг РНК был открыт в конце 1970-х годов при изучении аденовирусов, которые проникают в млекопитающих и размножаются внутри них. Исследователи идентифицировали молекулы РНК, содержащие последовательности из несмежных частей генома вируса. Это открытие привело к выводу о существовании регуляторных механизмов, влияющих на зрелую РНК и гены, которые она экспрессирует. [ 5 ] Использование минигенов в качестве вектора, сообщающего о сплайсинге, для изучения эффектов регуляции сплайсинга РНК естественным образом последовало и остается основным применением минигенов на сегодняшний день.
Типы
[ редактировать ]Чтобы обеспечить хорошую модель минигена, фрагмент гена должен содержать все необходимые элементы, чтобы гарантировать, что он демонстрирует те же альтернативного сплайсинга (AS) паттерны , что и ген дикого типа , т. е. длина фрагмента должна включать все расположенные выше и ниже по ходу транскрипции. последовательности, которые могут повлиять на его сплайсинг. [ 1 ] [ 2 ] Поэтому большинство проектов минигенов начинаются с тщательного in silico анализа требований эксперимента, прежде чем проводиться какая-либо «мокрая» лабораторная работа. [ 6 ] С появлением биоинформатики и широким распространением компьютеров теперь существует несколько хороших программ для идентификации цис-действующих контрольных областей, которые влияют на результаты сплайсинга гена. [ 7 ] [ 8 ] а продвинутые программы могут даже учитывать результаты сплайсинга в различных типах тканей. [ 9 ] Различия в минигенах обычно отражаются на конечном размере фрагмента, который, в свою очередь, отражает сложность самого минигена. Количество чужеродных элементов ДНК (экзонов и интронов), вставленных в конститутивные экзоны и интроны данного фрагмента, варьируется в зависимости от типа эксперимента и искомой информации. Типичный эксперимент может включать минигены дикого типа , которые, как ожидается, будут нормально экспрессировать гены в сравнительном эксперименте с генетически сконструированными аллельными вариациями , которые заменяют ген дикого типа и клонируются в те же фланкирующие последовательности, что и исходный фрагмент. Эксперименты такого типа помогают определить влияние различных мутаций на сплайсинг пре-мРНК . [ 3 ]
Строительство
[ редактировать ]После выбора подходящего геномного фрагмента (шаг 1) экзоны и интроны фрагмента могут быть вставлены и амплифицированы вместе с фланкирующими конститутивными экзонами и интронами исходного гена с помощью ПЦР . Праймеры для ПЦР могут быть выбраны так, чтобы они оставляли « липкие концы » на 3'-смысловых и антисмысловых цепях (Шаг 2). Эти «липкие концы» можно легко включить в вектор TOPO путем лигирования с коммерчески доступным источником, к которому уже прикреплена лигаза на момент включения. [ 10 ] (Шаг 3). Последующие векторы TOPO можно трансфицировать в клетки E.coli (шаг 4). После инкубации общую РНК можно извлечь из бактериальных колоний и проанализировать с помощью RT-PCR для количественной оценки соотношения включения/исключения экзонов (шаг 5). Миниген можно трансфицировать в различные типы клеток с различными факторами сплайсинга для проверки транс-действующих элементов (шаг 6). Экспрессированные гены или белки, которые они кодируют, можно проанализировать для оценки компонентов сплайсинга и их эффектов с помощью различных методов, включая гибридизацию или эксклюзионную хроматографию . [ 1 ] [ 2 ]

Использование
[ редактировать ]По оценкам, ошибки сплайсинга РНК встречаются в трети генетических заболеваний. [ нужна ссылка ] Чтобы понять патогенез и определить потенциальные цели терапевтического вмешательства при этих заболеваниях, важно объяснить задействованные элементы сплайсинга. [ 11 ] Определение полного набора компонентов, участвующих в сплайсинге, представляет множество проблем из-за обилия альтернативного сплайсинга, который встречается в большинстве генов человека, и специфичности, с которой сплайсинг осуществляется in vivo . [ 2 ] Сплайсинг четко осуществляется от типа клеток к типу клеток и на разных стадиях клеточного развития. Следовательно, очень важно, чтобы любые предположения in vitro или биоинформатические о регуляции сплайсинга были подтверждены in vivo . [ 12 ] Минигены используются для выявления цис -регуляторных элементов, транс -регуляторных элементов и других регуляторов преждевременного сплайсинга РНК in vivo . [ 2 ] Минигены были применены для изучения широкого спектра генетических заболеваний из-за вышеупомянутого обилия альтернативно сплайсированных генов, а также специфичности и вариаций, наблюдаемых в регуляции сплайсинга. [ 1 ] [ 2 ] [ 12 ] Ниже приведены примеры использования минигенов при различных заболеваниях. Хотя это не исчерпывающий список, он дает лучшее понимание того, как используются минигены.
Эндокринные заболевания
[ редактировать ]Ошибки сплайсинга РНК могут иметь серьезные последствия для функционирования белков, включая гормоны, выделяемые эндокринной системой . Такое воздействие на гормоны было идентифицировано как причина многих эндокринных нарушений, включая патологические состояния, связанные с щитовидной железой, рахит , гиперинсулинемическую гипогликемию и врожденную гиперплазию надпочечников . [ 13 ] Одним из конкретных примеров ошибки сплайсинга, вызывающей эндокринное заболевание, которое изучалось с использованием минигенов, является тип дефицита гормона роста , называемый изолированным дефицитом гормона роста (IGHD), заболевание, которое приводит к задержке роста. ИГГД типа II представляет собой аутосомно-доминантную форму, вызываемую мутацией в промежуточной последовательности (IVS), прилегающей к экзону 3 гена, кодирующего гормон роста 1, гена GH-1. Эта мутированная форма IVS3 приводит к пропуску экзона 3 в продукте мРНК. мРНК (-E3) кодирует усеченную форму гормона роста, которая затем ингибирует нормальную секрецию гормона роста. Минигены были использованы для определения того, что точечная мутация в энхансере сплайсинга интронов (ISE), встроенном в IVS3, виновата в пропуске E3. Более того, было установлено, что на функцию ISE влияет ближайший передвижной элемент переменного тока , показывая, что эта конкретная ошибка сращивания вызвана транс-действующим фактором. [ 14 ]
Нейродегенеративные заболевания
[ редактировать ]Накопление тау-белка связано с нейродегенеративными заболеваниями, включая болезни Альцгеймера и Паркинсона, а также другие таупатии . [ 15 ] Изоформы тау-белка создаются путем альтернативного сплайсинга экзонов 2, 3 и 10. Регуляция сплайсинга тау зависит от стадии развития, физиологии и местоположения. Ошибки при сплайсинге тау могут возникать как в экзонах, так и в интронах и, в зависимости от ошибки, приводить к изменениям в структуре белка или потере функции. [ 16 ] Агрегация этих аномальных тау-белков напрямую коррелирует с патогенезом и прогрессированием заболевания. Минигены использовались несколькими исследователями, чтобы помочь понять регуляторные компоненты, ответственные за сплайсинг мРНК гена TAU. [ 15 ] [ 16 ] [ 17 ]
Рак
[ редактировать ]Рак — сложное гетерогенное заболевание, которое может быть наследственным или возникать в результате воздействия окружающей среды. [ 18 ] Минигены используются, чтобы помочь онкологам понять роль пре-мРНК сплайсинга в различных типах рака. Особый интерес представляют специфичные для рака генетические мутации, которые нарушают нормальные события сплайсинга, в том числе те, которые затрагивают компоненты сплайсосом и РНК-связывающие белки, такие как гетерогенные ядерные рибонуклеочастицы (hnRNP) , белки, богатые серином/аргинином (SR) и малые рибонуклеопротеины (snRNP) . [ 19 ] [ 20 ] Белки, кодируемые аберрантно сплайсированными пре-мРНК, функционально различны и способствуют характерным аномалиям, проявляемым раковыми клетками, включая их способность пролиферировать, инвазировать и подвергаться ангиогенезу, а также метастазированию. [ 20 ] Минигены помогают исследователям выявлять генетические мутации при раке, которые приводят к ошибкам сплайсинга, и определять последующие эффекты, которые эти ошибки сплайсинга оказывают на экспрессию генов. [ 21 ] Используя знания, полученные в ходе исследований с использованием минигенов, онкологи предложили тесты, предназначенные для обнаружения продуктов аномальной экспрессии генов в диагностических целях. [ 22 ] перспектива использования минигенов в качестве иммунотерапии рака . Кроме того, изучается [ 23 ] [ 24 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д Стосс, О; Стоилов П; Хартманн, AM; Нейлер, О; Штамм, С. (декабрь 1999 г.). «Минигенный подход in vivo для анализа тканеспецифического сплайсинга». Исследования мозга. Протоколы исследования мозга . 4 (3): 383–94. дои : 10.1016/s1385-299x(99)00043-4 . ПМИД 10592349 .
- ^ Перейти обратно: а б с д и ж Купер, Томас А. (декабрь 2005 г.). «Использование минигенных систем для анализа альтернативных элементов сплайсинга». Методы . 37 (4): 331–340. дои : 10.1016/j.ymeth.2005.07.015 . ПМИД 16314262 .
- ^ Перейти обратно: а б Девиат, ЛР; Перес, Б; Угарте, М. (2012). «Минигены для подтверждения мутаций пропуска экзона». Пропуск экзонов . Методы Мол. Биол. Том. 867. стр. 37–47. дои : 10.1007/978-1-61779-767-5_3 . ISBN 978-1-61779-766-8 . ПМИД 22454053 .
- ^ Пунян, М.С.; МакКомас, WW; Нуссбаум, Алабама (1977). «Химический синтез двух дезоксирибододекануклеотидов для прикрепления концов рестрикции к искусственному минигену». Джин . 1 (5–6): 357–72. дои : 10.1016/0378-1119(77)90040-3 . ПМИД 590743 .
- ^ Клэнси, С. (2008). «Сплайсинг РНК: интроны, экзоны и сплайсосомы». Природное образование . 1 (31).
- ^ Бердж, Кристофер. «Программное обеспечение лаборатории Берджа» . Архивировано из оригинала 30 марта 2019 года . Проверено 7 мая 2014 г.
- ^ Дивина, Петр; Квитковикова, Андреа; Буратти, Эмануэле; Вореховский, Игорь (14 января 2009 г.). «Ab initio предсказание индуцированной мутацией активации скрытого сайта сплайсинга и пропуска экзона» . Европейский журнал генетики человека . 17 (6): 759–765. дои : 10.1038/ejhg.2008.257 . ПМК 2947103 . ПМИД 19142208 .
- ^ Гродецка, Люси; Локерова, Павла; Равчукова, Барбора; Буратти, Эмануэле; Баралле, Франсиско Э.; Душек, Ладислав; Фрайбергер, Томас; Спилианакис, Харалампос Бабис (21 февраля 2014 г.). «Мутации первого нуклеотида экзона при сплайсинге: оценка инструментов прогнозирования in silico» . ПЛОС ОДИН . 9 (2): e89570. Бибкод : 2014PLoSO...989570G . дои : 10.1371/journal.pone.0089570 . ПМЦ 3931810 . ПМИД 24586880 .
- ^ Бараш, Джозеф; Ковбой-Гарсия, Джордж; Гонсалес-Валлинас, Джон; Сюн, Хуэй; Гао, Вэйцзюнь; Ли, Лео Дж.; Фрей, Брендан Дж. (2013). «АВИСПА: веб-инструмент для прогнозирования и анализа альтернативного сплайсинга» . Геномная биология . 14 (10): Р1 дои : 10.1186/gb-2013-14-10-r114 . ПМК 4014802 . ПМИД 24156756 .
- ^ «Этапы создания вектора ТОПО» . Науки о жизни . Проверено 7 мая 2014 г.
- ^ Лим, Киан; Хуат; Феррарис, Лусиана; Филлу, Мадлен Э.; Рафаэль, Бенджамин Дж.; Фэйрбратер, Уильям Г. (2011). «Использование позиционного распределения для идентификации элементов сплайсинга и прогнозирования дефектов обработки пре-мРНК в генах человека» . Труды Национальной академии наук . 108 (27): 11093–6. Бибкод : 2011PNAS..10811093H . дои : 10.1073/pnas.1101135108 . ПМК 3131313 . ПМИД 21685335 .
- ^ Перейти обратно: а б Штамм, Стефан. «Stamms-lab.net» . Архивировано из оригинала 9 декабря 2013 года . Проверено 26 марта 2014 г.
- ^ Розария де Миранда, Элизабет (2009). «Влияние вариантов сплайсинга на нормальную физиологию и патологические состояния щитовидной железы» . Метабол эндокринолов Arq Bras . 53 (6): 709–714. дои : 10.1590/S0004-27302009000600003 . ПМИД 19893912 .
- ^ Муллис, ЧП (2010). «Генетика изолированного дефицита гормона роста» . J Clin Res Pediatr Эндокринол . 2 (2): 52–62. дои : 10.4274/jcrpe.v2i2.52 . ПМК 3014602 . ПМИД 21274339 .
- ^ Перейти обратно: а б Кар, Амар; Фусими, Кадзуо; Чжоу, Сяохун; Рэй, Паял; Ши, Чен; Чен, Сяопин; Лю, Жижэнь; Чен, Она; Ву, Джейн Ю. (2011). «РНК-геликаза p68 (DDX5) регулирует сплайсинг тау-экзона 10 путем модуляции структуры «стебель-петля» в 5'-сайте сплайсинга» . Мол. Клетка. Биол . 31 (9): 1812–1821. дои : 10.1128/MCB.01149-10 . ПМК 3133221 . ПМИД 21343338 .
- ^ Перейти обратно: а б Родригес-Мартин, Тереза; Карен Энтони; Мариано А. Гарсиа-Бланко; С. Гэри Мэнсфилд; Брайан Х. Андертон; Жан-Марк Галло (2009). «Коррекция неправильного сплайсинга тау, вызванного мутациями MAPT FTDP-17, путем опосредованного сплайсосомами транссплайсинга РНК» . Хум Мол Жене . 18 (17): 3266–3273. дои : 10.1093/hmg/ddp264 . ПМК 2722988 . ПМИД 19498037 .
- ^ Анфосси, М; Вуоно, Р; Малетта, Р; Вирди, К; Мирабелли, М; Колао, Р; Пуччо, Дж; Бернарди, Л; Франжипан, Ф; Галло, М; Джерачитано, С; Томаино, К; Курсио, SA; Заннино, Г; Ламенца, Ф; Дайкартс, К; Спиллантини, MG; Лоссо, Массачусетс; Бруни, AC (2011). «Составная гетерозиготность двух новых мутаций MAPT при лобно-височной деменции». Нейробиол Старение . 32 (4): 757.e1–757.e11. doi : 10.1016/j.neurobiolaging.2010.12.013 . ПМИД 21295377 . S2CID 5176440 .
- ^ Раджан, П.; Эллиотт, диджей; Робсон, Китай; Люнг, Хай (август 2009 г.). «Альтернативный сплайсинг и биологическая гетерогенность при раке простаты». Нат преподобный Урол . 6 (8): 454–460. дои : 10.1038/nrurol.2009.125 . ПМИД 19657379 . S2CID 30664940 .
- ^ Адлер, А.С.; МакКлеланд, ML; Да, С; Яйлаоглу, М; Хусейн, С; Косино, Э; Хиноны, Г; Модрусан, З; Сешагири, С; Торрес, Э; Чопра, В.С.; Хейли, Б; Чжан, З; Блэквуд, EM; Сингх, М; Юнттила, М; Стефан, JP; Лю, Дж; Пау, Г; Фирон, скорая помощь; Цзян, З; Файрштейн, Р. (май 2014 г.). «Интегративный анализ рака толстой кишки выявил важную функцию PRPF6 в росте опухоли» . Генс Дев . 28 (10): 1068–84. дои : 10.1101/gad.237206.113 . ПМК 4035536 . ПМИД 24788092 .
- ^ Перейти обратно: а б Го, Ронг; Юн Ли; Цзинин Нин; Дэн Сан; Ляньцзюнь Линь; Синьминь Лю (2013). «HnRNP A1/A2 и SF2/ASF регулируют альтернативный сплайсинг регуляторного фактора интерферона-3 и влияют на иммуномодулирующие функции в клетках немелкоклеточного рака легких человека» . ПЛОС ОДИН . 8 (4): e62729. Бибкод : 2013PLoSO...862729G . дои : 10.1371/journal.pone.0062729 . ПМЦ 3639176 . ПМИД 23658645 .
- ^ Кислота, Альберт; Дэвид Дж. Санс; Мерседес Дюран; Младенческое море; Люсия Перес-Каборнеро; Кристина Майнер; Эладио А. Веласко (2012). «Комплексный функциональный анализ сплайсинга вариантов ДНК гена BRCA2 гибридными минигенами» . рака молочной железы Исследования 14 (3):R8 дои : 10.1186/bcr3202 . ПМЦ 3446350 . ПМИД 22632462 .
- ^ Ди Джакомо, Д.; Гэйлдрат, П; Абули, А; Абдат, Дж; Фребур, Т; Тоси, М; Мартинс, А (2013). «Функциональный анализ большого набора вариантов экзона 7 BRCA2 подчеркивает прогностическую ценность показателей гексамеров при обнаружении изменений экзонных регуляторных элементов сплайсинга» . Хм. Мутат . 34 (11): 1547–57. дои : 10.1002/humu.22428 . ПМИД 23983145 . S2CID 22874730 .
- ^ Даниотти, Хосе Л.; Альдо А. Вилкес; Ванина Торрес Демикелис; Фернандо М. Руджеро; Макарена Родригес-Уокер (2013). «Гликозилирование гликолипидов при раке: основа разработки новых терапевтических подходов» . Передний Онкол . 3 : 306. doi : 10.3389/fonc.2013.00306 . ПМЦ 3867695 . ПМИД 24392350 .
- ^ Аурисиккио, Л; Фридман А; Багчи, А; Скарселли, Э; Ла Моника, Север; Силиберто, Дж. (январь 2014 г.). «Новый минигенный каркас для терапевтических противораковых вакцин» . Онкоиммунология . 3 (1): e27529. дои : 10.4161/onci.27529 . ПМК 4002591 . ПМИД 24790791 .
Дальнейшее чтение
[ редактировать ]- «Альтернативный сплайсинг пре-мРНК: теория и протоколы», Стефан Штамм, Крис Смит и Рейнхард Люрманн. ISBN 978-3527326068
- «Молекулярная диагностика, второе издание», под ред. Джордж П. Патринос и Вильгельм Ансорж ISBN 0123745373
- «ДНК-вакцины» под редакцией Хильдегун Эртль ISBN 1461349257
- «Альтернативный сплайсинг и болезни (прогресс в молекулярной и субклеточной биологии)» Филиппа Жантера ISBN 3540344489
Внешние ссылки
[ редактировать ]- Веб-страница Стефана Штамма в Университете Кентукки . Хороший обзор исследований минигенов.
- Лаборатория Кристофера Берджа на веб-сайте Массачусетского технологического института. Архивировано 30 марта 2019 г. на Wayback Machine . Хороший сайт для теоретического анализа сплайсинга.
- Браузер генома UCSC . Большая база данных для получения информации о генах.