Мезосоединение
Мезосоединение представляет или мезоизомер собой оптически неактивный изомер в наборе стереоизомеров , по крайней мере два из которых являются оптически активными. [1] [2] Это означает, что, несмотря на наличие двух или более стереоцентров , молекула не является хиральной . Мезосоединение можно накладывать на свое зеркальное изображение (не путать с наложением, поскольку любые два объекта могут накладываться друг на друга независимо от того, являются ли они одинаковыми). Два объекта могут быть наложены друг на друга, если все аспекты объектов совпадают и при анализе поляриметром не возникают показания «(+)» или «(-) » . [3] Название происходит от греческого mésos, что означает «средний».
Например, винная кислота может существовать в виде любого из трех стереоизомеров, изображенных ниже в проекции Фишера . Из четырех цветных изображений вверху диаграммы первые два представляют мезосоединение (изомеры 2R , 3S и 2S , 3R эквивалентны ), за которыми следует оптически активная пара левовинной кислоты (L-( R,R )-(+)-винная кислота) и декстровинная кислота (D-( S,S )-(-)-винная кислота). Мезосоединение разделено пополам внутренней плоскостью симметрии , которой нет у негомезо-изомеров (обозначено буквой X). То есть при отражении мезосоединения через плоскость зеркала, перпендикулярную экрану, получается та же самая стереохимия; это не относится к немезовинной кислоте, [3] который генерирует другой энантиомер . Мезосоединение не следует путать с рацемической смесью двух оптически активных соединений в соотношении 50:50, хотя ни одно из них не будет вращать свет в поляриметре .
Требуется, чтобы два стереоцентра в мезосоединении имели по крайней мере два общих заместителя (хотя наличие этой характеристики не обязательно означает, что соединение является мезо). Например, в 2,4-пентандиоле и второй, и четвертый атомы углерода, являющиеся стереоцентрами, имеют все четыре общих заместителя.

Поскольку мезоизомер имеет накладываемое зеркальное отображение, соединение с n хиральными центрами не может достичь теоретического максимума 2. н стереоизомеры, если один из стереоизомеров является мезо. [4]
Мезоизомер не обязательно должен иметь зеркальную плоскость. Он может иметь инверсионную или роторно-рефлексную симметрию, такую как S 4 . Например, существует два мезоизомера 1,4-дифтор-2,5-дихлорциклогексана, но ни один из них не имеет зеркальной плоскости, а также есть два мезоизомера 1,2,3,4-тетрафторспиропентана (см. Рисунок).
Циклические мезосоединения
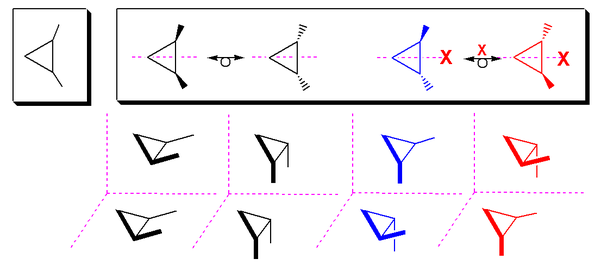
[ редактировать ]1,2-замещенный циклопропан имеет мезоцис - изомер (молекула имеет зеркальную плоскость) и два транс -энантиомера:
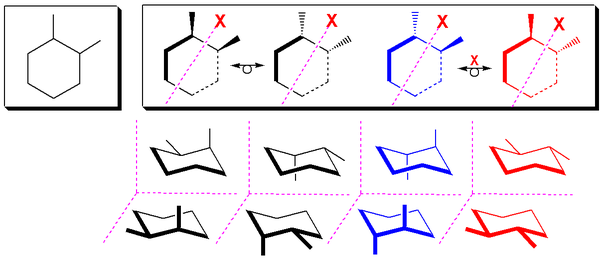
Два цис-стереоизомера 1,2-замещенных циклогексанов в большинстве случаев ведут себя как мезосоединения при комнатной температуре. При комнатной температуре большинство 1,2-дизамещенных циклогексанов подвергаются быстрому переворачиванию кольца (за исключением колец с объемными заместителями), и в результате два цис-стереоизомера ведут себя химически идентично с хиральными реагентами. [5] Однако при низких температурах это не так, поскольку энергию активации переворота кольца невозможно преодолеть, и поэтому они ведут себя как энантиомеры. Примечателен также тот факт, что при перевороте кольца циклогексана абсолютные конфигурации стереоцентров не изменяются.
Ссылки
[ редактировать ]- ^ Олт, Аддисон (2008). «Значение Мезо». Журнал химического образования . 85 (3): 441. Бибкод : 2008JChEd..85..441A . дои : 10.1021/ed085p441 . ISSN 0021-9584 .
- ^ ИЮПАК , Сборник химической терминологии , 2-е изд. («Золотая книга») (1997). Интернет-исправленная версия: (2006–) « Мезосоединение ». дои : 10.1351/goldbook.M03839
- ^ Перейти обратно: а б Макмерри, Джон (2008). Органическая химия (7-е изд.) . Томсон. стр. 305–7. ISBN 978-0-495-11258-7 .
- ^ Брюс, Паула. Органическая химия. 2007. Пирсон Прентис Холл. Река Аппер-Седл, штат Нью-Джерси.
- ^ Воллхардт, К. Питер К. Органическая химия: структура и функции, Четвертое изд. 2003. WH Freeman and Co. Нью-Йорк. стр. 187.