Углекислый газ
 | |
| Имена | |
|---|---|
| Название ИЮПАК пентаоксан-6-он | |
| Идентификаторы | |
3D model ( JSmol ) | |
ПабХим CID | |
| Характеристики | |
| СО 6 | |
| Молярная масса | 108.005 g·mol −1 |
| Родственные соединения | |
Родственные соединения | Пятиокись углерода Четырехокись углерода Гексасульфид углерода |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
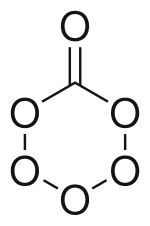
Углекислый газ или гексаоксид углерода — это оксид углерода с необычно большим количеством кислорода. [1] Молекула была получена и изучена при криогенных температурах. Молекула важна в химии атмосферы и при изучении холодных льдов во внешней Солнечной системе и межзвездном пространстве. [2] Вещество могло образоваться и присутствовать на Ганимеде или Тритоне , спутниках внешней Солнечной системы. Молекула состоит из шестичленного кольца с пятью атомами кислорода и одним атомом углерода, а также одного атома кислорода с двойной связью с углеродом. [1]
Форма
[ редактировать ]Наблюдаемая молекула имеет симметрию C s . Кольцо представляет собой не плоский шестиугольник, а сморщенное, с длиной сторон и углами, немного отличающимися от обычного шестиугольника (120 °). При движении по кольцу, начиная от связи углерод-кислород, межатомные расстояния составляют C–O: 1,362 Å O–O 1,491 Å, O–O 1,391 Å, O–O 1,391 Å, O–O 1,491 Å и O–C 1,362. О. Углы между связями составляют: О–С–О 120,4°, С–О–О 115,7°, О–О–О 105,9° и противоположная от углерода О–О–О 104,1°. Для двойной связи углерод-кислород длина составляет 1,185 Å, а угол между одинарными связями составляет 119,6°. [1]
Формирование
[ редактировать ]В эксперименте гексоксид углерода образовался путем облучения твердого диоксида углерода электронами с энергией 5000 эВ при 10 К в вакууме. Реакция протекает путем отрыва атомарного кислорода от углекислого газа:
Затем атомарный кислород реагирует с диоксидом углерода с образованием триоксида углерода , и аналогичные реакции происходят с образованием ряда кольцевых оксидов четырехокиси углерода и пятиокиси углерода , что в конечном итоге приводит к образованию гексоксида углерода. [1] в экзотермической реакции. [2]
- СО 2 + О → О 2 СО
- О 2 СО + О → О 3 СО
- О 3 СО + О → О 4 СО
- O 4 CO + O → O 5 CO ΔH = −145,2 кДж моль −1 [2]
Характеристики
[ редактировать ]Углекислый газ стабилен до 60 К. [1] Колебательные инфракрасные волновые числа включают наиболее заметные ν 1 = 1876 см. −1 для наиболее распространенного изотополога 12 С 16 О6 . [1]
Другие изомеры
[ редактировать ]Другими возможными изомерами гексоксида углерода являются форма C 2 с пяти- и трехчленным кольцом и форма D 2d с двумя четырехчленными кольцами. Изомер D 2d O 3 CO 3 имеет расчетную длину связи C–O 1,391 Å и длину O–O 1,469 Å. Валентный угол O–C–O составляет 94,1°. Однако эти два изомера не наблюдались. [2]
Эквивалентный гексасульфид углерода также известен из исследований матрицы инертного газа. Он имеет симметрию C 2 с тем же расположением атомов, что и гексоксид. [3]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж Джеймисон, Кори С.; Александр М. Мебель; Ральф И. Кайзер (2008). «Первое обнаружение C s симметричного изомера гексаоксида углерода (CO 6 ) при 10 К». Письма по химической физике . 450 (4–6): 312–317. Бибкод : 2008CPL...450..312J . дои : 10.1016/j.cplett.2007.11.052 . ISSN 0009-2614 .
- ^ Jump up to: а б с д Кайзер, Ральф И.; Александр М. Мебель (2008). «Об образовании высших оксидов углерода в экстремальных условиях». Письма по химической физике . 465 (1–3): 1–9. Бибкод : 2008CPL...465....1K . дои : 10.1016/j.cplett.2008.07.076 . ISSN 0009-2614 .
- ^ Майти, Сураджит; Ким, Ю.С.; Кайзер, Ральф И.; Линь, Хун Мао; Сунь, Бянь Цзянь; Чанг, AHH (июль 2013 г.). «Об обнаружении сульфидов углерода высших порядков (CS x ; x = 4–6) в низкотемпературных сероуглеродных льдах». Письма по химической физике . 577 : 42–47. Бибкод : 2013CPL...577...42M . дои : 10.1016/j.cplett.2013.05.039 .