Аллилацетат

| |

| |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК
Проп-2-енилацетат [ 1 ] | |
| Другие имена
2-пропенилацетат
Аллилацетат | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХЭМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.008.851 |
| Номер ЕС |
|
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 2333 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 5 Н 8 О 2 | |
| Молярная масса | 100.117 g·mol −1 |
| Появление | Бесцветная жидкость |
| Плотность | 0,928 г/см 3 |
| Точка кипения | 103 ° С (217 ° F; 376 К) |
| слабо растворим | |
| -56.7·10 −6 см 3 /моль | |
| Опасности | |
| СГС Маркировка : | |
  
| |
| Опасность | |
| Х225 , Х301 , Х312 , Х319 , Х330 | |
| P210 , P233 , P240 , P241 , P242 , P243 , P260 , P264 , P270 , P271 , P280 , P284 , P301+P310 , P302+P352 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P312 , P320 , P321 , P322 , P330 , P337+P313 , P363 , P370+P378 , P403+P233 , P403+P235 , P405 , P501 | |
| 374 ° С (705 ° F, 647 К) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Аллилацетат представляет собой органическое соединение формулы C 3 H 5 OC(O)CH 3 . Эта бесцветная жидкость является предшественником особенно аллилового спирта , который является полезным промышленным промежуточным продуктом. Это ацетатный эфир аллилового спирта.
Подготовка
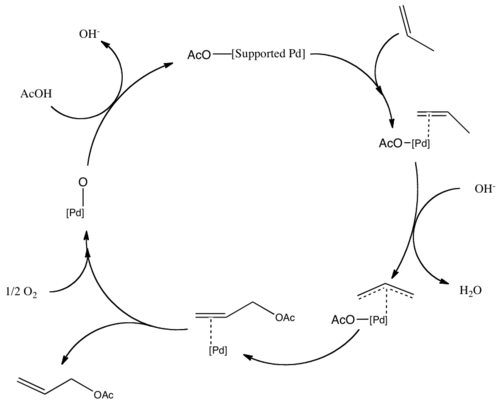
[ редактировать ]Аллилацетат получают в промышленности газофазной реакцией пропена в присутствии уксусной кислоты с использованием палладиевого катализатора : [ 2 ] [ 3 ]
- C 3 H 6 + CH 3 COOH + ½ O 2 → CH 2 =CHCH 2 OCOCH 3 + H 2 O
Этот метод выгоден, потому что пропен является недорогим и экологически чистым химикатом . Аллиловый спирт также производится в основном из аллилхлорида, но производство путем гидролиза аллилацетата позволяет избежать использования хлора, и поэтому его использование увеличивается.
Винилацетат производят аналогично, используя этилен вместо пропена. Эти реакции являются примерами ацетоксилирования. Затем палладиевый центр повторно окисляется присутствующим O 2 . Механизм ацетоксилирования следует аналогичному пути: пропен образует π-аллильную связь на палладии. [ 4 ]
Реакции и применение
[ редактировать ]Аллилацетат гидролизуется до аллилового спирта :
- CH 2 =CHCH 2 OCOCH 3 + H 2 O → CH 2 =CHCH 2 OH + CH 3 COOH
Аллиловый спирт является предшественником некоторых специальных полимеров, главным образом олиф . Аллиловый спирт также является предшественником синтетического глицерина . При эпоксидировании перекисью водорода образуется глицидол , который гидролизуется до глицерина.
- CH 2 =CHCH 2 OH + HOOH → CH 2 OCHCH 2 OH + H 2 O
- CH 2 OCHCH 2 OH + H 2 O → C 3 H 5 (OH) 3
Синтетический глицерин обычно используется в косметике и туалетных принадлежностях, тогда как глицерин, образующийся в результате гидролиза жиров, используется в пищевых продуктах. [ 5 ]
Реакции замещения
[ редактировать ]Замещение ацетатной группы в аллилацетате с использованием хлористого водорода дает аллилхлорид . Реакция с цианистым водородом на медном катализаторе дает аллилцианид . [ 6 ]
- CH 2 =CHCH 2 OCOCH 3 + HCl → CH 2 =CHCH 2 Cl + CH 3 COOH
- CH 2 =CHCH 2 OCOCH 3 + HCN → CH 2 =CHCH 2 CN + CH 3 COOH
Аллилхлорид обычно получают непосредственно хлорированием пропена.
Ссылки
[ редактировать ]- ^ «Аллилацетат» .
- ^ Гарольд Виткофф; Б.Г. Рубен; Джеффри С. Плоткин (2004). Промышленные органические химикаты ( отрывок из Google Books ) . Джон Уайли и сыновья. п. 212. ИСБН 978-0-471-54036-6 .
- ^ Людгер Крелинг; Юрген Крей; Джеральд Джейкобсон; Иоганн Гролиг; Леопольд Микше (2002). «Аллиловые соединения». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a01_425 . ISBN 978-3527306732 .
- ^ г-н Черчилль; Р. Мейсон (1964). «Молекулярная структура ацетата π-аллилпалладия» . Природа . 204 (4960): 777. Бибкод : 1964Natur.204..777C . дои : 10.1038/204777a0 .
- ^ Х.А. Виткофф; Б.Г. Рубен; Дж. С. Плоткин (2004). «Химические вещества и полимеры из пропилена». Промышленные органические химикаты . Джон Уайли и сыновья. стр. 195–214 . ISBN 978-0-471-44385-8 .
- ^ Людгер Кралинг; и др. (2000). «Аллиловые соединения». Энциклопедия промышленной химии Ульмана . дои : 10.1002/14356007.a01_425 . ISBN 9783527303854 .