Сенсоры малых молекул

Маломолекулярные датчики — эффективный способ обнаружения присутствия ионов металлов в растворе. [1] Хотя существует множество типов, большинство сенсоров на малых молекулах содержат субъединицу, которая избирательно связывается с металлом, что, в свою очередь, вызывает изменение флуоресцентной субъединицы. датчика малых молекул Это изменение можно наблюдать в спектре , который можно отслеживать с помощью системы обнаружения, такой как микроскоп или фотодиод . [2] Для различных применений существуют разные зонды, каждый из которых имеет разные константы диссоциации по отношению к конкретному металлу, разные флуоресцентные свойства и чувствительность. Они показывают большие перспективы как способ исследования биологических процессов путем мониторинга ионов металлов в низких концентрациях в биологических системах. Поскольку они по определению малы и часто способны проникать в биологические системы, они подходят для многих применений, для которых другие, более традиционные методы биосенсорства менее эффективны или не подходят. [3]
Использование
[ редактировать ]
Ионы металлов необходимы практически для всех биологических систем, и поэтому изучение их концентраций с помощью эффективных зондов весьма полезно. Поскольку ионы металлов играют ключевую роль в причинах рака , диабета и других заболеваний, их мониторинг с помощью зондов, которые могут дать представление об их концентрациях с пространственным и временным разрешением, представляет большой интерес для научного сообщества. [3] Существует множество применений датчиков малых молекул. Показано, что с их помощью можно эффективно различать допустимые и вредные концентрации ртути в рыбе . [4] Кроме того, поскольку некоторые типы нейронов во время своей работы поглощают цинк, эти зонды можно использовать для отслеживания активности мозга и служить эффективной альтернативой функциональной МРТ . [5] Можно также отслеживать и количественно оценивать рост клеток , таких как фибробласты , которые поглощают ионы металлов в процессе своего построения. [3] Многочисленные другие биологические процессы можно отслеживать с помощью датчиков малых молекул, поскольку многие из них меняют концентрации металлов по мере их возникновения, которые затем можно отслеживать. Тем не менее, датчик должен быть адаптирован к конкретной среде и требованиям к чувствительности. В зависимости от применения металлосенсор должен быть селективным в отношении определенного типа металла и особенно должен иметь возможность связывать целевой металл с большим сродством, чем металлы, которые естественным образом существуют в высоких концентрациях внутри ячейки. Кроме того, они должны обеспечивать ответ с сильной модуляцией спектра флуоресценции и, следовательно, обеспечивать высокое соотношение сигнал/шум . Наконец, очень важно, чтобы датчик не был токсичным для биологической системы, в которой он используется. [3]
Механизмы обнаружения
[ редактировать ]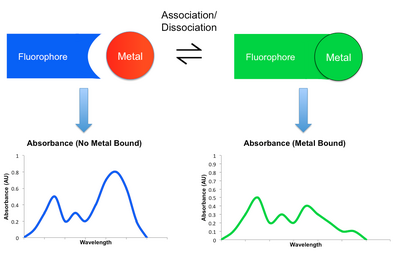
Большинство механизмов обнаружения, задействованных в сенсорах малых молекул, включают некоторую модуляцию флуоресцентного поведения сенсорной молекулы при связывании целевого металла. Когда металл координируется с таким датчиком, он может либо усиливать, либо уменьшать исходное флуоресцентное излучение. Первый известен как эффект усиления флуоресценции хелатирования (CHEF), а второй — эффект тушения усиления хелатирования (CHEQ). Изменяя интенсивность излучения на разных длинах волн, результирующий флуоресцентный спектр может ослабляться, усиливаться или сдвигаться при связывании и диссоциации металла. Этот сдвиг в спектрах можно отслеживать с помощью детектора, такого как микроскоп или фотодиод. [2] [6] Ниже перечислены некоторые примеры механизмов, с помощью которых модулируется излучение. Их участие в CHEQ или CHEF зависит от рассматриваемого датчика металлов и малых молекул.
Первичные механизмы обнаружения
[ редактировать ]- Тушение парамагнитной флуоресценции , создание новых электронных состояний при связывании парамагнитного атома металла. [2]
- Фотоиндуцированный перенос электрона (ПЭТ) — блокировка состояния с более низкой энергией из-за связывания атома металла. [2]
- Фотоиндуцированный перенос заряда (PCT) , модуляция энергетических уровней в комплексе путем переноса заряда внутри сопряженной пи-системы . [2]
- Резонансная передача энергии флуоресценции (FRET) , [2] переход экситона от донора к акцептору, модулирующий спектр излучения. [2] [7]
- Образование эксимера/эксиплекса — образование состояния, представляющего собой гибрид основного и возбужденного состояний. Он обладает новыми флуоресцентными свойствами. [2]
- Хемодозиметры — комплексы, которые вступают в необратимые реакции с другими видами при связывании металла с образованием новых соединений с новыми флуоресцентными спектрами. [2]
Флуорофоры
[ редактировать ]

Флуорофоры необходимы для измерения процесса связывания металла и, косвенно, концентрации металла. Существует много типов, каждый из которых имеет разные свойства, которые делают их полезными для разных применений. Некоторые из них работают как небольшие металлические сенсоры полностью сами по себе, в то время как другие должны образовывать комплекс с субъединицей, которая может хелатировать или связывать ион металла. родамин Например, претерпевает конформационные изменения при связывании иона металла. При этом он переключается между бесцветной, нефлуоресцентной спироциклической формой на флуоресцентную розовую открытую циклическую форму. [2] [8] хинолина Разработаны сенсоры на основе , образующие люминесцентные комплексы с Cd(II) и флуоресцентные с Zn(II). Предполагается, что он функционирует путем изменения своего нижнего люминесцентного состояния с n – π * на π – π * при координации с металлом. [2] [9] [10] Когда DNS-группа дансила связывается с металлом, она теряет сульфонамидный водород, вызывая тушение флуоресценции посредством механизма ПЭТ или обратного ПЭТ, при котором электрон переносится либо к связанному металлу, либо от него. [11]
Примеры
[ редактировать ]Цинк
[ редактировать ]Цинк — один из наиболее распространенных ионов металлов в биологических системах. [6] Маломолекулярные сенсоры для него включают в себя:
- ZX1, соединение, содержащее цинксвязывающую субъединицу дипиколиламина (DPA), которая имеет большее сродство к цинку, чем другие виды, обнаруженные в растворе, такие как Ca и Mg. [12]
- Зинпир-1 (ZP1), соединение, содержащее флуоресцентное соединение дихлорфлуоресцеина , связанное с двумя видами 2-пиколамина (ДПА), которые связывают Zn (II). ZP1 является частью семейства сенсоров цинка, известного как серия Zinpyr, члены которого являются вариантами ZP1, обеспечивающими определенное сродство и профили флуоресценции. [3]
- Сенсоры ZnAF-1, которые содержат донор арила и акцептор ксантенона и имеют большое изменение флуоресценции при связывании Zn (II). Их использовали для изучения поглощения Zn(II) пирамидными нейронами CA3. [3] [5]
- GFZnP: Новое семейство флуоресцентных хемосенсоров GFP из 12 членов было создано для обнаружения Zn2+ в биологических образцах с помощью двухфотонной микроскопии. Это комбинация 8-аминохинолинового мотива и хромофорной единицы GFP, что приводит к усилению флуоресцентного ответа на Zn2+. Наиболее эффективными членами являются GFZnP ED, GFZnP Pic и GFZnP dipic. GFZnP легко синтезируются и коммерчески доступны, что делает их одними из наиболее доступных двухфотонных сенсоров Zn2+. Спектроскопическая характеристика семейства зондов подчеркивает их яркое флуоресцентное излучение (ε x Φ > 200) при λem = 520 нм при возбуждении светом λex = 450 нм. Сечение 2P-действия зондов достигает δ´Φcomp > 5 Гс при λex, 2P=900 нм, с увеличением до 200 раз, что делает их одними из лучших двухфотонных зондов для Zn2+. члены семейства сенсоров, особенно GFZnP ED, GFZnP Pic и GFZnP dipic, демонстрируют высокую селективность в отношении Zn2+ со сродством в наномолярном (нМ) диапазоне, отличную растворимость в воде и удобство использования в широком диапазоне pH (pH > 6). . Применимость выбранных зондов была продемонстрирована с помощью эпифлуоресцентной и 2P-микроскопии на культивируемых клетках и срезах мозга. Эта работа расширяет набор эффективных двухфотонных датчиков цинка новым ценным семейством. [13]
- GFZnP OMe: Опубликован альтернативный флуоресцентный датчик Zn2+ на основе GFP для двухфотонной микроскопии и связанных с ней биологических и микроскопических приложений. Он состоит из каркаса из 8-метоксихинолина. Он имеет превосходные фотофизические характеристики, включая 37-кратное усиление флуоресценции при l(ex) = 440 нм и l(em) = 505 нм. Двухфотонное сечение достигает 73 Гм при длине волны 880 нм. [14]
- GFZnP BIPY: селективный флуоресцентный хемосенсор Zn2+ с хелаторным фрагментом 2,2'-бипиридина. Он был эффективен в физиологически значимом диапазоне pH и имеет превосходные фотофизические характеристики, включая 53-кратное усиление флуоресценции с максимумами возбуждения и эмиссии при 422 нм и 492 нм соответственно. Сообщается о высоком двухфотонном сечении 3,0 GM при длине волны 840 нм, а также об превосходной селективности по ионам металлов. Эксперименты in vitro на культуре клеток HEK 293 были проведены с использованием двухфотонной микроскопии, демонстрирующей применимость. [15]
Медь
[ редактировать ]Медь является биологически важным металлом, который необходимо обнаружить. Для него разработано множество датчиков, в том числе:
- CTAP-1, сенсор, который реагирует в УФ-области, когда Cu(I) связывается с мотивом азатетратиакрауна, который, в свою очередь, возбуждает пиразолина прикрепленный краситель на основе . Чтобы использовать зонд, его возбуждают при длине волны 365 нм. Если он связан с Cu, то интенсивность его флуоресценции увеличится. CTAP-1 эффективен, поскольку имеет большую модуляцию спектра при связывании Cu и селективен при связывании Cu по сравнению с другими металлами. [3] [6]
- Медный сенсор-1 (CS1), который содержит богатый тиоэфиром мотив, который связывается с Cu(I), вызывая возбуждение бор-дипиррометенового красителя ( BODIPY ) в видимой области. Зонд обладает хорошей селективностью в отношении Cu(I) по сравнению с щелочноземельными металлами , Cu(II) и металлами d-блока . [3] [6]
Железо
[ редактировать ]Железо широко используется в биологических системах, и этот факт хорошо известен благодаря его роли в гемоглобине . Для этого существует множество датчиков малых молекул, в том числе:
- Прирен-TEMPO, в котором связывание железа с TEMPO тушит флуоресценцию пирена, когда Fe (II) не связан. Однако после связывания TEMPO снижается, и пирен восстанавливает флуоресценцию. Этот зонд ограничен тем, что аналогичный ответ может быть вызван нежелательными свободными радикалами и что его можно использовать только в кислом растворе. [6] [16]
- DansSQ, в котором связывание Fe(II) увеличивает флуоресценцию при 460 нм. Он состоит из дансильной группы, связанной со стирилхинолином, и действует за счет нарушения внутримолекулярного переноса заряда при связывании Fe (II). Его ограничения заключаются в том, что он растворяется только в ацетонитриле в 10% H 2 O. [6]
Кобальт
[ редактировать ]Были созданы датчики кобальта , которые используют разрыв связей CO с помощью Co(II) во флуоресцентном зонде, известном как Cobalt Probe 1 (CP1). [17]
Меркурий
[ редактировать ]Ртуть является токсичным тяжелым металлом , и поэтому важно иметь возможность обнаружить ее в биологических системах. Датчики включают в себя:
- Ртутные сенсоры (МС) — семейство сенсоров, содержащих комплексы флуоресцеина и нафтофлуоресцеина. Зонд MS1 увеличивает свою эмиссию при связывании Hg(II), сохраняя при этом большое сродство к ртути по сравнению с ионами других тяжелых металлов. [3]
- Сенсор S3 основан на комплексе BODIPY , флуоресценция которого значительно увеличивается при связывании Hg(II). [3] [18]
- В MF1 используется мягкий тиоэфирный хелатор Hg(II), связанный с флуоресцеинподобным репортером ксантенона. Он имеет хороший контраст при связывании ртути и хорошую селективность. MF1 настолько чувствителен, что его предложили использовать для проверки рыбы на токсичные уровни ртути. [3] [4]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Томат, Элиза; Липпард, Стивен Дж (апрель 2010 г.). «Визуализация подвижного цинка в биологии» . Современное мнение в области химической биологии . 14 (2): 225–230. дои : 10.1016/j.cbpa.2009.12.010 . ПМЦ 2847655 . ПМИД 20097117 .
- ^ Перейти обратно: а б с д и ж г час я дж к Формика, Мауро; Фуси, Вьери; Георгий, Лука; Микелони, Мауро (январь 2012 г.). «Новые флуоресцентные хемосенсоры для ионов металлов в растворе». Обзоры координационной химии . 256 (1–2): 170–192. дои : 10.1016/j.ccr.2011.09.010 .
- ^ Перейти обратно: а б с д и ж г час я дж к Домайль, Дилан В.; Que, Эмили Л; Чанг, Кристофер Дж (март 2008 г.). «Синтетические флуоресцентные сенсоры для изучения клеточной биологии металлов». Химическая биология природы . 4 (3): 168–175. дои : 10.1038/nchembio.69 . ПМИД 18277978 .
- ^ Перейти обратно: а б Юн, Сонхо; Альберс, Аарон Э.; Вонг, Одри П.; Чанг, Кристофер Дж. (ноябрь 2005 г.). «Проверка уровня ртути в рыбах с помощью селективного флуоресцентного хемосенсора». Журнал Американского химического общества . 127 (46): 16030–16031. дои : 10.1021/ja0557987 . ПМИД 16287282 .
- ^ Перейти обратно: а б Хирано, Томоя; Кикучи, Казуя; Урано, Ясутеру; Хигучи, Цунехико; Нагано, Тецуо (декабрь 2000 г.). «Молекулы флуоресцентного сенсора с высокой селективностью по цинку, подходящие для биологических применений». Журнал Американского химического общества . 122 (49): 12399–12400. дои : 10.1021/ja002467f .
- ^ Перейти обратно: а б с д и ж Картер, Кайл П.; Янг, Александра М.; Палмер, Эми Э. (23 апреля 2014 г.). «Флуоресцентные датчики для измерения ионов металлов в живых системах» . Химические обзоры . 114 (8): 4564–4601. дои : 10.1021/cr400546e . ПМК 4096685 . ПМИД 24588137 .
- ^ «Резонансный перенос энергии флуоресценции» . Калифорнийский университет в Дэвисе, Чемвики . Калифорнийский университет в Дэвисе. 2 октября 2013 года . Проверено 12 марта 2015 г.
- ^ Мун, Кён Су; Ян, Ён-Гын; Джи, Сынхи; Тэ, Джинсунг (июнь 2010 г.). «Аминоксисвязанный гидроксамат родамина как флуоресцентный хемосенсор Fe3+ в водных средах». Буквы тетраэдра . 51 (25): 3290–3293. дои : 10.1016/j.tetlet.2010.04.068 .
- ^ Сюэ, Гопин; Брэдшоу, Джеральд С; Далли, Н.Кент; Сэвидж, Пол Б; Изатт, Рид М; Проди, Лука; Монтальти, Марко; Заккерони, Нельси (июнь 2002 г.). «Синтез азакраун-эфиров с побочными соединениями на основе хинолина в качестве потенциальных флуорофоров цинка (II)». Тетраэдр . 58 (24): 4809–4815. дои : 10.1016/S0040-4020(02)00451-9 .
- ^ Миямото, Ре; Каваками, Джун; Такахаши, Сюко; Ито, Сюндзи; Нагаки, Масахико; Китара, Харуо (2006). «Зависимое от времени DFT-исследование механизма эмиссии производных 8-гидроксихинолина в качестве флуоресцентных хемосенсоров для ионов металлов» . Журнал компьютерной химии, Япония . 5 (1): 19–22. дои : 10.2477/jccj.5.19 .
- ^ Фаббрицци, Луиджи; Личелли, Маурицио; Паллавичини, Пьерсандро; Перотти, Анджело; Сакки, Донателла (17 октября 1994 г.). «Флуоресцентный датчик на основе антрацена для ионов переходных металлов». Angewandte Chemie International Edition на английском языке . 33 (19): 1975–1977. дои : 10.1002/anie.199419751 .
- ^ Пан, Энхуэй; Чжан, Сяо-ань; Хуан, Чжэнь; Крезель, Артур; Чжао, Мин; Тинберг, Кристин Э.; Липпард, Стивен Дж.; Макнамара, Джеймс О. (сентябрь 2011 г.). «Везикулярный цинк способствует пресинаптической и ингибирует постсинаптическую долговременную потенциацию синапса CA3 мшистого волокна» . Нейрон . 71 (6): 1116–1126. дои : 10.1016/j.neuron.2011.07.019 . ПМК 3184234 . ПМИД 21943607 .
- ^ Чомос, Аттила; Ковач, Эрвин; Мадарас, Миклош; Федор, Флора; Фулоп, Анна; Катона, Гергели; Балаж Й., Рожа; Мучи, Золтан (1 января 2024 г.). «Двухфотонные флуоресцентные хемосенсоры на основе GFP-хромофора для обнаружения Zn2+ в биологических образцах – от проектирования до применения». Датчики и аккумуляторы B . 398 (1): 134753. doi : 10.1016/j.snb.2023.134753 .
 В эту статью включен текст из этого источника, доступного по лицензии CC BY 3.0 .
В эту статью включен текст из этого источника, доступного по лицензии CC BY 3.0 . - ^ Чомос, Аттила; Мадарас, Миклош; Турцель, Габор; Лаванда, кустарник; Бодор, Андреа; Матушкак, Анетт; Катона, Грегори; Ковач, Эрвин; Розса, Балаж Дж.; Мукси, Золтан (3 июня 2024 г.). «GFP вдохновил флуоресцентный молекулярный сенсор на основе 8-метоксихинолина для обнаружения Zn2+ с помощью двухфотонной микроскопии» . Химия: Европейский журнал . 30 (31): e202400009. дои : 10.1002/chem.202400009 . ПМИД 38446718 .
- ^ Чомос, Аттила; Мадарас, Миклош; Турцель, Габор; Чери, Левенте; Катона, Грегори; и др. (январь 2024 г.). «Молекулярный гибрид хромофора GFP и 2,2'-бипиридина: доступный датчик для обнаружения Zn2+ с помощью флуоресцентной микроскопии» . Международный журнал молекулярных наук . 25 (6): 3504. doi : 10.3390/ijms25063504 . ISSN 1422-0067 . ПМЦ 10971390 . ПМИД 38542479 .
 В эту статью включен текст из этого источника, доступного по лицензии CC BY 4.0 .
В эту статью включен текст из этого источника, доступного по лицензии CC BY 4.0 . - ^ Чен, Джин-Лонг; Чжо, Шу-Цзюань; У, Юй-Цин; Клык, Клык; Ли, Линг; Чжу, Чан-Цин (февраль 2006 г.). «Высокоселективное определение железа (II) за счет его усиления флуоресценции пирен-тетраметилпиперидинила (TEMPO) в качестве зонда спин-флуоресценции». Spectrochimica Acta Часть A: Молекулярная и биомолекулярная спектроскопия . 63 (2): 438–443. Бибкод : 2006AcSpA..63..438C . дои : 10.1016/j.saa.2005.04.057 . ПМИД 15996513 .
- ^ Ау-Юнг, Хо Ю; Нью, Элизабет Дж.; Чанг, Кристофер Дж. (2012). «Флуоресцентный зонд на основе селективной реакции для обнаружения кобальта в живых клетках». Химические коммуникации . 48 (43): 5268–70. дои : 10.1039/c2cc31681a . ПМИД 22531796 .
- ^ Го, Сянфэн; Цянь, Сюйхун; Цзя, Лихуа (март 2004 г.). «Высокоселективный и чувствительный флуоресцентный хемосенсор для ртути в водном растворе нейтрального буфера». Журнал Американского химического общества . 126 (8): 2272–2273. дои : 10.1021/ja037604y . ПМИД 14982408 .